将 配制成 悬浊液,向其中滴加 的 溶液。 ( 代表 、 或 )随加入 溶液体积( )的变化关系如图所示。
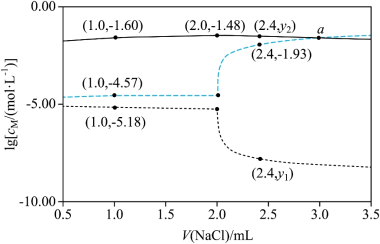
下列叙述正确的是( )
| A. |
交点a处: |
| B. |
|
| C. |
时, 不变 |
| D. |
, |
科学家使用 研制了一种 可充电电池(如图所示)。电池工作一段时间后, 电极上检测到 和少量 。下列叙述正确的是( )
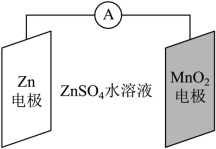
| A. |
充电时, 向阳极方向迁移 |
| B. |
充电时,会发生反应 |
| C. |
放电时,正极反应有 |
| D. |
放电时, 电极质量减少 , 电极生成了 |
W、X、Y、Z为原子序数依次增大的短周期元素。W和X原子序数之和等于 的核外电子数,化合物 可用作化学电源的电解质。下列叙述正确的是( )
| A. |
X和Z属于同一主族 |
| B. |
非属性: |
| C. |
气态氢化物的稳定性: |
| D. |
原子半径: |
四瓶无色溶液 、 、 、 ,它们之间的反应关系如图所示。其中a、b、c、d代表四种溶液,e和g为无色气体,f为白色沉淀。下列叙述正确的是( )
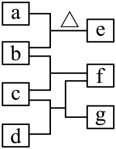
| A. |
a呈弱碱性 |
| B. |
f可溶于过量的b中 |
| C. |
c中通入过量的e可得到无色溶液 |
| D. |
b和d反应生成的沉淀不溶于稀硝酸 |
我国化学工作者开发了一种回收利用聚乳酸( )高分子材料的方法,其转化路线如下所示。
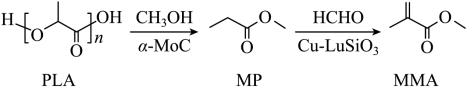
下列叙述错误的是( )
| A. |
在碱性条件下可发生降解反应 |
| B. |
的化学名称是丙酸甲酯 |
| C. |
的同分异构体中含羧基的有 种 |
| D. |
可加聚生成高分子 |
下列过程对应的离子方程式正确的是( )
| A. |
用氢氟酸刻蚀玻璃: |
| B. |
用三氯化铁溶液刻制覆铜电路板: |
| C. |
用硫代硫酸钠溶液脱氯: |
| D. |
用碳酸钠溶液浸泡锅炉水垢中的硫酸钙: |
人类对能源的利用经历了柴薪、煤炭和石油时期,现正向新能源方向高质量发展。下列有关能源的叙述错误的是( )
| A. |
木材与煤均含有碳元素 |
B. |
石油裂化可生产汽油 |
| C. |
燃料电池将热能转化为电能 |
D. |
太阳能光解水可制氢 |
二氧化碳加氢制甲烷过程中的主要反应为
在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列说法正确的是( )
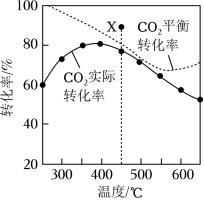
| A. |
反应 的焓变 |
| B. |
的平衡选择性随着温度的升高而增加 |
| C. |
用该催化剂催化二氧化碳反应的最佳温度范围约为 |
| D. |
时,提高 的值或增大压强,均能使 平衡转化率达到 点的值 |
室温下,用含少量 的MnSO4溶液制备 的过程如题图所示。已知 , 。下列说法正确的是( )
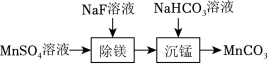
| A. |
溶液中: |
| B. |
“除镁”得到的上层清液中: |
| C. |
溶液中: |
| D. |
“沉锰”后的滤液中: |
室温下,探究 溶液的性质,下列实验方案能达到探究目的的是( )
|
选项 |
探究目的 |
实验方案 |
|
A |
溶液中是否含有 |
向 溶液中滴加几滴新制氯水,再滴加 溶液,观察溶液颜色变化 |
|
B |
是否有还原性 |
向 溶液中滴加几滴酸性 溶液,观察溶液颜色变化 |
|
C |
是否水解 |
向 溶液中滴加 滴酚酞试液,观察溶液颜色变化 |
|
D |
能否催化 分解 |
向 溶液中滴加几滴 溶液,观察气泡产生情况 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
金属硫化物( )催化反应 ,既可以除去天然气中的 ,又可以获得 。下列说法正确的是( )
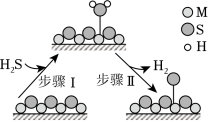
| A. |
该反应的 |
| B. |
该反应的平衡常数 |
| C. |
题图所示的反应机理中,步骤Ⅰ可理解为 中带部分负电荷的 与催化剂中的 之间发生作用 |
| D. |
该反应中每消耗 ,转移电子的数目约为 |
化合物 是合成药物非奈利酮的重要中间体,其合成路线如图:

下列说法正确的是( )
| A. |
不能与 溶液发生显色反应 |
| B. |
中的含氧官能团分别是酯基、羧基 |
| C. |
最多能与 发生加成反应 |
| D. |
可用饱和 溶液和 银氨溶液进行鉴别 |
氮及其化合物的转化具有重要应用。下列说法不正确的是( )
| A. |
实验室探究稀硝酸与铜反应的气态产物:
(稀) |
| B. |
工业制硝酸过程中的物质转化:
|
| C. |
汽车尾气催化转化器中发生的主要反应:
|
| D. |
实验室制备少量
的原理:
|
阅读下列材料,完成下面小题。
氢元素及其化合物在自然界广泛存在且具有重要应用。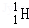 、
、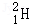 、
、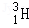 是氢元素的3种核素,基态
原子
的核外电子排布,使得
既可以形成
又可以形成
,还能形成
等重要化合物;水煤气法、电解水、光催化分解水都能获得
,如水煤气法制氢反应中,
与足量
反应生成
和
吸收
的热量。
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在催化剂作用下与
反应可得到
。我国科学家在氢气的制备和应用等方面都取得了重大成果。
是氢元素的3种核素,基态
原子
的核外电子排布,使得
既可以形成
又可以形成
,还能形成
等重要化合物;水煤气法、电解水、光催化分解水都能获得
,如水煤气法制氢反应中,
与足量
反应生成
和
吸收
的热量。
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在催化剂作用下与
反应可得到
。我国科学家在氢气的制备和应用等方面都取得了重大成果。
(1)下列说法正确的是( )
| A. |
|
| B. |
和 的中心原子轨道杂化类型均为 |
| C. |
分子中的化学键均为极性共价键 |
| D. |
晶体中存在 与 之间的强烈相互作用 |
(2)下列化学反应表示正确的是( )
| A. |
水煤气法制氢: |
| B. |
催化加氢生成
的反应:
|
| C. |
电解水制氢的阳极反应: |
| D. |
与水反应: |
(3)下列物质结构与性质或物质性质与用途具有对应关系的是( )
| A. |
具有还原性,可作为氢氧燃料电池的燃料 |
| B. |
氨极易溶于水,液氨可用作制冷剂 |
| C. |
分子之间形成氢键, 的热稳定性比 的高 |
| D. |
中的 原子与 形成配位键, 具有还原性 |