二氧化碳加氢制甲烷过程中的主要反应为
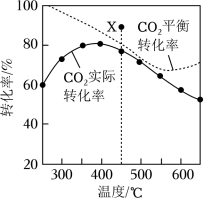
在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列说法正确的是( )
| A. |
反应 的焓变 |
| B. |
的平衡选择性随着温度的升高而增加 |
| C. |
用该催化剂催化二氧化碳反应的最佳温度范围约为 |
| D. |
时,提高 的值或增大压强,均能使 平衡转化率达到 点的值 |
二氧化碳加氢制甲烷过程中的主要反应为
在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列说法正确的是( )

| A. |
反应 的焓变 |
| B. |
的平衡选择性随着温度的升高而增加 |
| C. |
用该催化剂催化二氧化碳反应的最佳温度范围约为 |
| D. |
时,提高 的值或增大压强,均能使 平衡转化率达到 点的值 |