2023年全国统一高考化学试卷(江苏卷)
我国提出2060年实现碳中和的目标,体现了大国担当。碳中和中的碳是指( )
| A. |
碳原子 |
B. |
二氧化碳 |
C. |
碳元素 |
D. |
含碳物质 |
反应 应用于石油开采。下列说法正确的是( )
| A. |
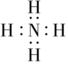
的电子式为 |
| B. |
中N元素的化合价为 |
| C. |
分子中存在 键 |
| D. |
为非极性分子 |
元素 位于周期表中 族。下列说法正确的是( )
| A. |
原子半径: |
| B. |
第一电离能: |
| C. |
碳单质、晶体硅、 均为共价晶体 |
| D. |
可在周期表中元素 附近寻找新半导体材料 |
阅读下列材料,完成下面小题。
氢元素及其化合物在自然界广泛存在且具有重要应用。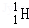 、
、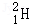 、
、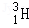 是氢元素的3种核素,基态
原子
的核外电子排布,使得
既可以形成
又可以形成
,还能形成
等重要化合物;水煤气法、电解水、光催化分解水都能获得
,如水煤气法制氢反应中,
与足量
反应生成
和
吸收
的热量。
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在催化剂作用下与
反应可得到
。我国科学家在氢气的制备和应用等方面都取得了重大成果。
是氢元素的3种核素,基态
原子
的核外电子排布,使得
既可以形成
又可以形成
,还能形成
等重要化合物;水煤气法、电解水、光催化分解水都能获得
,如水煤气法制氢反应中,
与足量
反应生成
和
吸收
的热量。
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在催化剂作用下与
反应可得到
。我国科学家在氢气的制备和应用等方面都取得了重大成果。
(1)下列说法正确的是( )
| A. |
|
| B. |
和 的中心原子轨道杂化类型均为 |
| C. |
分子中的化学键均为极性共价键 |
| D. |
晶体中存在 与 之间的强烈相互作用 |
(2)下列化学反应表示正确的是( )
| A. |
水煤气法制氢: |
| B. |
催化加氢生成
的反应:
|
| C. |
电解水制氢的阳极反应: |
| D. |
与水反应: |
(3)下列物质结构与性质或物质性质与用途具有对应关系的是( )
| A. |
具有还原性,可作为氢氧燃料电池的燃料 |
| B. |
氨极易溶于水,液氨可用作制冷剂 |
| C. |
分子之间形成氢键, 的热稳定性比 的高 |
| D. |
中的 原子与 形成配位键, 具有还原性 |
氮及其化合物的转化具有重要应用。下列说法不正确的是( )
| A. |
实验室探究稀硝酸与铜反应的气态产物:
(稀) |
| B. |
工业制硝酸过程中的物质转化:
|
| C. |
汽车尾气催化转化器中发生的主要反应:
|
| D. |
实验室制备少量
的原理:
|
化合物 是合成药物非奈利酮的重要中间体,其合成路线如图:

下列说法正确的是( )
| A. |
不能与 溶液发生显色反应 |
| B. |
中的含氧官能团分别是酯基、羧基 |
| C. |
最多能与 发生加成反应 |
| D. |
可用饱和 溶液和 银氨溶液进行鉴别 |
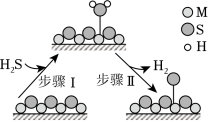
金属硫化物( )催化反应 ,既可以除去天然气中的 ,又可以获得 。下列说法正确的是( )
| A. |
该反应的 |
| B. |
该反应的平衡常数 |
| C. |
题图所示的反应机理中,步骤Ⅰ可理解为 中带部分负电荷的 与催化剂中的 之间发生作用 |
| D. |
该反应中每消耗 ,转移电子的数目约为 |
室温下,探究 溶液的性质,下列实验方案能达到探究目的的是( )
|
选项 |
探究目的 |
实验方案 |
|
A |
溶液中是否含有 |
向 溶液中滴加几滴新制氯水,再滴加 溶液,观察溶液颜色变化 |
|
B |
是否有还原性 |
向 溶液中滴加几滴酸性 溶液,观察溶液颜色变化 |
|
C |
是否水解 |
向 溶液中滴加 滴酚酞试液,观察溶液颜色变化 |
|
D |
能否催化 分解 |
向 溶液中滴加几滴 溶液,观察气泡产生情况 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
室温下,用含少量 的MnSO4溶液制备 的过程如题图所示。已知 , 。下列说法正确的是( )
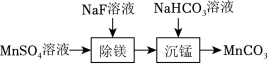
| A. |
溶液中: |
| B. |
“除镁”得到的上层清液中: |
| C. |
溶液中: |
| D. |
“沉锰”后的滤液中: |
二氧化碳加氢制甲烷过程中的主要反应为
在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列说法正确的是( )
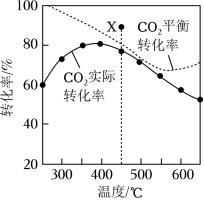
| A. |
反应 的焓变 |
| B. |
的平衡选择性随着温度的升高而增加 |
| C. |
用该催化剂催化二氧化碳反应的最佳温度范围约为 |
| D. |
时,提高 的值或增大压强,均能使 平衡转化率达到 点的值 |
催化剂能催化 脱除烟气中的 ,反应为 。
(1)催化剂的制备。将预先制备的一定量的 粉末置于 的水中,在搅拌下加入一定量的 溶液,经蒸发、焙烧等工序得到颗粒状 催化剂。在水溶液中 水解为 沉淀的离子方程式为__________;反应选用 溶液而不选用 溶液的原因是__________。
(2)催化剂的应用。将一定物质的量浓度的 (其余为 )气体匀速通过装有 催化剂的反应器,测得 的转化率随温度的变化如题图所示。反应温度在 范围内, 转化率随温度变化不明显的原因是__________;反应温度高于 , 转化率下降,除因为进入反应器的 被还原的量减少外,还有__________(用化学方程式表示)。
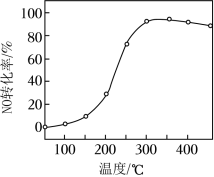
(3)废催化剂的回收。回收 废催化剂并制备 的过程可表示为
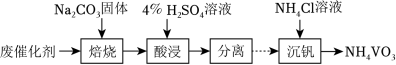
①酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有__________。
②通过萃取可分离钒和钨,在得到的钒酸中含有 。已知 具有八元环结构,其结构式可表示为__________。
③向 的 溶液中加入过量的 溶液,生成 沉淀。已知: ,加过量 溶液的目的是__________。
化合物 是鞘氨醇激酶抑制剂,其合成路线如图:
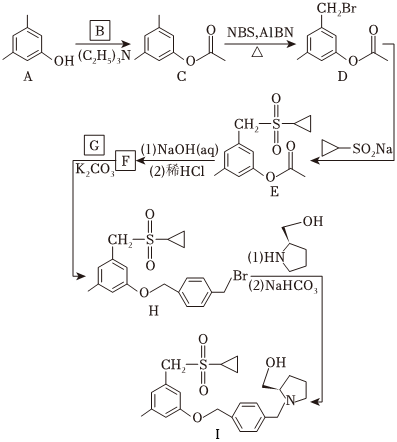
(1)化合物A的酸性比环己醇的_____(填“强”或“弱”或“无差别”)。
(2)B的分子式为 ,可由乙酸与 反应合成,B的结构简式为_____。
(3)A→C中加入 是为了结构反应中产生的_____(填化学式)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:_____。碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使 酸性 溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有 个峰。
(5)G的分子式为 ,F→H的反应类型为_____。
(6)写出以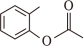 、
、 和
为原料制备
和
为原料制备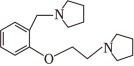 的合成路线流程图(须用
和
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(须用
和
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
实验室模拟“镁法工业烟气脱硫”并制备 ,其实验过程可表示为
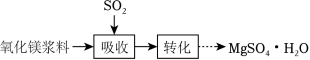
(1)在搅拌下向氧化镁浆料中匀速缓慢通入 气体,生成 ,反应为 ,其平衡常数 与 的代数关系式为 __________;下列实验操作一定能提高氧化镁浆料吸收 效率的有_____(填序号)。
| A. |
水浴加热氧化镁浆料 |
| B. |
加快搅拌速率 |
| C. |
降低通入 气体的速率 |
| D. |
通过多孔球泡向氧化镁浆料中通 |
(2)在催化剂作用下 被 氧化为 。已知 的溶解度为 , 氧化溶液中 的离子方程式为__________;在其他条件相同时,以负载钴的分子筛为催化剂,浆料中 被 氧化的速率随 的变化如题图甲所示。在 范围内,pH增大,浆料中 的氧化速率增大,其主要原因是__________。
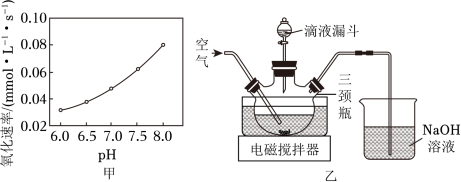
(3)制取 晶体。在如题图乙所示的实验装置中,搅拌下,使一定量的 浆料与 溶液充分反应。 浆料与 溶液的加料方式是__________;补充完整制取 晶体的实验方案:向含有少量 的 溶液中,_______________。(已知: 在 时完全转化为氢氧化物沉淀;室温下从 饱和溶液中结晶出 , 在 下干燥得到 ,实验中需要使用 粉末)
空气中 含量的控制和 资源利用具有重要意义。
(1)燃煤烟气中 的捕集可通过如图所示的物质转化实现。

“吸收”后所得的 溶液与石灰乳反应的化学方程式为__________;载人航天器内,常用 固体而很少用 固体吸收空气中的 ,其原因是__________。
(2)合成尿素 是利用 的途径之一。尿素合成主要通过下列反应实现
反应Ⅰ:
反应Ⅱ:
①密闭体系中反应Ⅰ的平衡常数( )与温度的关系如图甲所示,反应Ⅰ的 _____(填“ ”或“ ”或“ ”)。
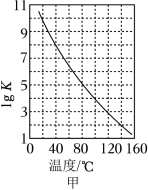
②反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲[ ]和尿素转化为氰酸铵( )等副反应。尿素生产中实际投入 和 的物质的量之比为 ,其实际投料比值远大于理论值的原因是_______________。
(3)催化电解吸收 的 溶液可将 转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率( )随电解电压的变化如图乙所示。
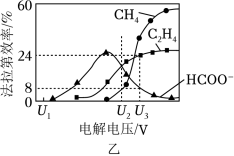
其中, , 表示电解生成还原产物 所转移电子的物质的量, 表示法拉第常数。
①当电解电压为 时,电解过程中含碳还原产物的 为 ,阴极主要还原产物为_____(填化学式)。
②当电解电压为 时,阴极由 生成 的电极反应式为__________。
③当电解电压为 时,电解生成的 和 的物质的量之比为_____(写出计算过程)。
 制取
制取
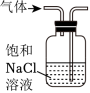 除去
中的
除去
中的
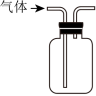 收集
收集
 吸收尾气中的
吸收尾气中的
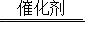
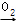

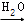


 粤公网安备 44130202000953号
粤公网安备 44130202000953号