常温下,某溶液中由水电离的c (H+)=1×10-13mol·L-1,该溶液可能是( )
①氯化铵水溶液 ②硝酸钠水溶液 ③硫酸水溶液 ④氢氧化钠水溶液
| A.①④ | B.①② | C.②③ | D.③④ |
下列溶液中的氯离子数目与50 mL 1 mol·L-1的FeCl3溶液中氯离子数目相等的是( )
| A.50 mL 1.5 mol·L-1的FeCl2溶液 | B.100 mL 3 mol·L-1的NH4Cl溶液 |
| C.75 mL 3 mol·L-1的KCl溶液 | D.50 mL 2 mol·L-1的CaCl2溶液 |
某学生的实验报告所列出的下列数据中合理的是
| A.用10mL量筒量取7.13mL稀盐酸 |
| B.用托盘天平称量25.20g NaCl |
| C.用广泛pH试纸测得某溶液的pH为2.3 |
| D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL |
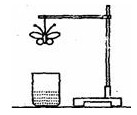
某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种无色试剂,挂在铁架台上(保持湿润)。另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图)。过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是
| |
|
取pH=4的某电解质溶液 1.00L ,用 Pt电极进行电解,经过一段时间后,测得溶液的pH=1,且阴阳两极产物的物质的量之比为2:1,则该电解质溶液是
| A.盐酸 | B.氯化钾溶液 | C.硝酸银溶液 | D.硫酸铜溶液 |
将0.2mol·L-1HCN溶液和0.1mol·L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是( )
| A.c (HCN)<c (CN-) | B.c (Na+) = c (CN-) |
| C.c (HCN)-c (CN-)=c (OH-) | D.c (HCN)+c (CN-)=0.1mol·L-1 |
下列事实不能用勒夏特利原理来解释的是
| A.增大压强,有利于SO2和O2反应生成SO3 |
| B.热的纯碱溶液去油污能力较强 |
| C.加催化剂使N2和H2在一定条件下转化为NH3 |
| D.常温下pH=3的H2SO4溶液中水的电离程度小于pH=3的NH4Cl溶液中水的电离程度 |
右图是向100mL的盐酸中逐滴加入NaOH溶液时,混合溶液的pH变化图像,根据图像得出的结论正确的是
| A.原盐酸溶液的浓度为0.1mol/L |
| B.加入的NaOH溶液的浓度为0.1mol/L |
| C.至滴定终点用去NaOH为0.01mo1 |
| D.pH=12时,共加入NaOH溶液100mL |
量取25.00mL硫酸溶液,可选用的仪器是
| A.50mL量筒 | B.25mL量筒 |
| C.50mL碱式滴定管 | D.50mL酸式滴定管 |
下列说法正确的是
| A.向50 mL 1 mol·L-1的盐酸中加入烧碱,水的KW不变 |
| B.NH4Cl和NH3·H2O混合液中,二者对对方的平衡都起了抑制作用 |
| C.有两种弱酸HX和HY且酸性HX>HY,则体积和浓度相同的NaX和NaY溶液中有c(Y-)>c(X-)>c(OH-)>c(H+) |
| D.常温0.1mol·L-1 HA溶液中C(OH-)/ c(H+)=10-8,则0.01 mol·L-1HA溶液中c(H+)=1×10-4mol·L-1 |
下列关于盐酸与醋酸两种稀溶液的说法中正确的是( )
| A.相同浓度的两溶液中[H+]相同 |
| B.100 mL 0.1mol/L的两溶液能中和等物质的量的氢氧化钠 |
| C.pH=3的两溶液稀释100倍,pH都为5 |
| D.两溶液中分别加入少量对应的钠盐,[H+]都明显减小 |
关于常温下pH = 12的NaOH溶液,下列说法错误的是
| A.c(OH-) =c(Na+) + c(H+) |
| B.由水电离出的c(OH-) = 1.0×10-12 mol·L-1 |
| C.与等体积pH = 2的醋酸混合后所得溶液显碱性 |
| D.与等体积0.01 mol·L-1氯化铵溶液混合后所得溶液中:c(Na+)> c(NH4+) |
三种正盐的混合溶液中含有0.2mol K+、0.25mol Zn2+、0.4mol Cl-和SO42-,则SO42-的物质的量为( )
| A.0.1mol | B.0.15mol | C.0.3mol | D.0.5mol |