湖南省湘西州部分高中高二1月期末联考化学试卷
下列物质既能导电又属电解质的是( )
| A.硝酸钾溶液 | B.硫酸铜晶体 |
| C.熔融的氯化钠 | D.无水乙醇 |
把1mL0.1mol/L的H2SO4加水稀释制成2L溶液,在此溶液中由水电离产生的H+,其浓度接近于( )
A.1×10 mol/L mol/L |
B.1×10 mol/L mol/L |
C.1×10 mol/L mol/L |
D.1×10 mol/L mol/L |
温度一定时,用水稀释0.1摩/升氨水时,溶液中随着水量的增加而减小的是( )
| A.c(OH-)/c(NH3·H2O) | B.c(NH3·H2O)/c(OH-) |
| C.c(H+)和c(OH-)的乘积 | D.OH-的物质的量 |
在室温下等体积的酸和碱的溶液,混合后pH值一定小于7的是( )
| A.pH=3的硝酸与pH=11的氢氧化钾溶液 |
| B.pH=3的盐酸与pH=11的氨水 |
| C.pH=3的硫酸与pH=11的氢氧化钠溶液 |
| D.pH=3的醋酸与pH=11的氢氧化钡溶液 |
锰锌干电池在放电时总反应方程式可以表示为:Zn(s)+2MnO2+2NH4+=Zn2++Mn2O3(s)+2NH3+H2O,在此电池放电时正极(碳棒)上发生反应的物质是( )
| A.Zn | B.碳 | C.MnO2和NH4+ | D.Zn和NH3 |
下列说法正确的是( )
A.8.4克NaHCO3晶体中含有0.1molHCO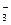 离子。 离子。 |
B.0.1mol/LNaHCO3溶液中HCO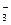 浓度为0.1mol/L。 浓度为0.1mol/L。 |
C.NaHCO3溶液中:c(Na+)=2c(CO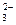 )+c(HCO )+c(HCO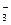 )+c(H2CO3)。 )+c(H2CO3)。 |
D.NaHCO3溶液中:c(OH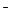 )= c(CO )= c(CO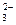 )+c(H2CO3) )+c(H2CO3) |
在铁制品上镀一定厚度的锌层,以下设计方案正确的是 ( )
| A.锌作阳极,铁制品作阴极,溶液中含有锌离子 |
| B.锌作阴极,铁制品作阳极,溶液中含有锌离子 |
| C.锌作阳极,铁制品作阴极,溶液中含有亚铁离子 |
| D.锌作阴极,铁制品作阳极,溶液中含有亚铁 |
下列溶液一定呈中性的是( )
| A.c(H+)=10-7mol/L的溶液 | B.pH=7的溶液 |
C.c(H+)/c(OH )=10-14的溶液 )=10-14的溶液 |
D.氨水与氯化铵的混合液中c(NH4+)=c(Cl ) ) |
常温下,某溶液中由水电离的c (H+)=1×10-13mol·L-1,该溶液可能是( )
①氯化铵水溶液 ②硝酸钠水溶液 ③硫酸水溶液 ④氢氧化钠水溶液
| A.①④ | B.①② | C.②③ | D.③④ |
有A、B、C、D四种金属。将A与B用导线连接起来浸入电解质溶液中,B不易腐蚀。将A、D分别投入等浓度盐酸溶液中,D比A反应剧烈。将铜浸入B的盐溶液中,无明显变化。如果把铜浸入C的盐溶液中,有金属C析出。据此判断它们的活动性由强到弱的顺序是( )
A.D>C>A>B B.D>A>B>C C.D>B>A>C D.B>A>D>C
已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。关于标有“+”的接线柱,下列说法中正确的是( )
| A.充电时作阳极,放电时作负极 | B.充电时作阳极,放电时作正极 |
| C.充电时作阴极,放电时作负极 | D.充电时作阴极,放电时作正极 |
用石墨作电极,电解1 mol/L下列物质的溶液,溶液的pH保持不变的是( )
| A.HCl | B.NaOH | C.Na2SO4 | D.NaCl |
将分别盛有熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾.镁.铝的物质的量之比为 ( )
| A.1∶2∶3 | B.3∶2∶1 |
| C.6∶3∶1 | D.6∶3∶2 |
把Ca(OH)2固体放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2 (s) Ca2+(aq)+2OH-(aq)。当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是( )
Ca2+(aq)+2OH-(aq)。当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是( )
| A.溶液的pH增大 | B.溶液的pH不变 |
| C.溶液中Ca2+数目增多 | D.溶液中c(Ca2+)增大 |
将等质量的两份锌粉a和b,分别加入两个盛过量的稀硫酸的烧杯中,并向加入a的烧杯中再加入少量CuO粉末。下列各图表示氢气体积V(H2)与反应时间t的关系,其中正确的是 ( ) 
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是( )
| A.由Al.Cu.稀H2SO4组成原电池,其负极反应式为:Al - 3eˉ=Al3+ |
| B.由Mg.Al.NaOH溶液组成原电池,其负极反应式为: Al - 3eˉ+ 4OHˉ=AlO2ˉ+ 2H2O |
| C.由Fe.Cu.FeCl3溶液组成原电池,其负极反应式为:Cu - 2eˉ=Cu2+ |
| D.由Al.Cu.浓硝酸组成原电池,其负极反应式为:Cu - 2eˉ=Cu2+ |
已知铅蓄电池放电时发生如下反应:负极:Pb+SO42— -2e— =PbSO4,
正极:PbO2 + 4H+ + SO42— + 2e— = PbSO4 + 2H2O。实验室用铅蓄电池作电源,用惰性电极电解CuSO4溶液,当阴极析出2.4g铜时,铅蓄电池内消耗H2SO4物质的量至少是
| A.0.050mol | B.0.075mol |
| C.0.20mol | D.0.40mol |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn +2K2FeO4 +8H2O 3Zn(OH)2 +2Fe(OH)3 + 4KOH,下列叙述不正确的是( )
3Zn(OH)2 +2Fe(OH)3 + 4KOH,下列叙述不正确的是( )
| A.放电时负极反应为:Zn – 2e- + 2OH- = Zn(OH)2 |
| B.充电时阳极反应为:Fe(OH)3 - 3e- + 5OH- = FeO42- + 4H2O |
| C.放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
D.放电时正极附近溶液的碱性增强 |
在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11,若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液体积之和,则Ba(OH)2溶液与NaHSO4溶液体积之比是( )
| A.1:9 | B.1:1 |
| C.1:2 | D.1:4 |
将等物质的量的K2SO4、NaCl、Ba(NO3)2、AgNO3混合均匀后,置于容器中,加入足量的水,搅拌,静置,过滤。取滤液,用铂电极电解一段时间,则两极区析出的氧化产物和还原产物的质量比为( )
| A.35.5︰108 | B.108︰71 | C.8︰1 | D.1︰2 |
一种新型燃料电池,一极通入空气,另一极通入丁烷气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料的说法正确的是
| A.在熔融电解质中,O2-由负极移向正极 |
| B.电池的总反应是:C4H10 + 13O2 → 4CO2 + 5H2O |
| C.通入空气的一极是正极,电极反应为:O2 + 4e- =2O2- |
| D.通入丁烷的一极是正极,电极反应为:C4H10 + 26e- +13O2- =4CO2↑+ 5 H2O |
在1LK2SO4和CuSO4的混合溶液中,c(SO42-)="2.0" mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标准状况)气体,则原溶液中K+的物质的量浓度为( )
| A.2.0 mol·L-1 | B.1.5 mol·L-1 | C.1.0 mol·L-1 | D.0.5 mol·L-1 |
用Pt电极电解KCl和CuSO4的混合溶液,当电路中通过0.4mol电子的电量时,阴阳两极都产生0.14mol的气体,若电解后溶液体积为40L,则电解后溶液的pH为( )
| A.1 | B.3 | C.7 | D.11 |
T℃时,有甲.乙两个密闭容器,甲容器的体积为1L,乙容器的体积为2L,分别向甲.乙两容器中加入6mol A和3mol B,发生反应如下:
3A(g)+b B(g)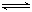 3C(g)+2D(g),(b为
3C(g)+2D(g),(b为 3的正整数) 。
3的正整数) 。
4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;
t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。
根据题给的信息回答下列问题:
(1)甲容器中反应的平均速率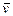 (B)= 。
(B)= 。
(2)在温度T℃时,该反应的化学平衡常数为__________________.
由下表数据可知该反应为______________(填“吸热”“放热”)反应。
化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(3)T℃时,在另一个体积与乙相同的丙容器中,为了达到平衡时B的浓度仍然为0.8mol/L,起始时,向丙容器中加入C、D的物质的量分别为3mol.2mol,则还需加入A.B的物质的量分别是___________.___________。
某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A==H++HA .
.
HA
 H++A2-,回答下列问题:
H++A2-,回答下列问题:
(1)Na2A溶液呈 (填“酸性”.“中性”或“碱性”),理由是:
(用离子方程式说明)
NaHA溶液呈 (填“酸性”.“中性”或“碱性”),理由是:
。
(2)已知0.1mol/LNaHA溶液的pH=2,则0.1mol/L的H2A溶液中氢离子的物质的量浓度 0.11mol/L(填“<”.“>”或“=”)理由是:
______ 。
(3)0.1mol/LNaHA溶液中各种离子浓度由大到小的顺序是:
。
(1)如下图所示,A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,C.D为电解槽,其电极材料见图,电解质溶液:C装置中溶液为AgNO3溶液,D装置的溶液为Cu(NO3)2溶液,。关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向d端移动,则电源a端为 极,通电一段时间后,观察到滤纸c端出现的现象是: ;
(2)打开K1,关闭K2,通电一段时间后,D装置中Cu极的电极反应式为 。C装置中右端Pt电极上的电极反应式为: 。C装置中总反应方程式为: 。
(3)假定C.D装置中电解质溶液足量,电解一段时间后,C装置中溶液的pH值
(填“变大”.“变小”或“不变”,下同),D装置中溶液的pH值 。
某学生欲用已知物质的量浓度的HCl测定未知浓度的NaOH溶液,将HCl置于滴定管,氢氧化钠溶液置于锥形瓶,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定未知浓度的NaOH溶液,滴定到终点时锥形瓶中颜色变化为 。
(2)下列操作中可能无法会怎样影响所测NaOH溶液浓度(填偏大.偏小或不影响)
A.酸式滴定管未用标准浓度的HCl润洗就直接注入标准盐酸
B.读数时,开始平视,结束时俯视 液面
液面
(3)某学生根据3次实验记录有关数据如下:
| 滴定次数 |
待测NaOH溶液体积(mL) |
0.1000mol/L HCl溶液的体积(mL) |
|
| 滴定前刻度 |
滴定后刻度 |
||
| 第一次 |
25.00 |
0.00 |
26.11 |
| 第二次 |
25.00 |
1.56 |
30.30 |
| 第三次 |
25.00 |
0.22 |
26.31 |
请选择合理的数据计算NaOH溶液的物质的量浓度:c(NaOH)=________________。
在25℃时,用石墨电极电解 ,
, 溶液。5min后,在一个石墨电极上有6.4g Cu生成。试回答:
溶液。5min后,在一个石墨电极上有6.4g Cu生成。试回答:
(1)转移电子的物质的量,得到 的体积(标准状况),溶液的
的体积(标准状况),溶液的 ?
?
2)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差多少?电解液的 是否变化? (相对原子质量 Cu:64)
是否变化? (相对原子质量 Cu:64)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号