锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
| A.充电时电极a连接电源的负极 |
| B.放电时负极的电极反应式为Zn—2e-=Zn2+ |
| C.放电时左侧电解质储罐中的离子总浓度增大 |
| D.阳离子交换膜可阻止Br2与Zn直接发生反应 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O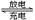 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
关于该电池的说法正确的是
| A.放电时,Zn作负极,发生还原反应 |
| B.放电时,K2FeO4附近溶液pH减小 |
| C.充电时,锌极附近溶液pH减小 |
| D.充电时,阳极电极反应为:Fe(OH)3-3e-+5OH-===FeO42-+4H2O |
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e-→X+2H+。下列说法中正确的是
| A.电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O |
| B.另一极的电极反应式为:O2 + 4e- + 2H2O = 4OH- |
| C.乙醇在正极发生反应,电子经过外电路流向负极 |
| D.电池内部H+由正极向负极移动 |
锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应式是2Zn+O2==2ZnO。下列有关它的说法正确的是
| A.锌为电池负极,发生氧化反应 |
| B.电解质溶液是酸性溶液 |
| C.电池工作时,氧气与锌直接化合,生成氧化锌 |
| D.负极发生的反应是:Zn-2e-+H2O=ZnO+2H+ |
下列关于燃料电池的说法正确的是
| A.燃料电池是通过燃烧方式将化学能转换为电能 |
| B.氢氧燃料电池中,通入氢气的一极为正极 |
| C.氢氧燃料电池是一种环境友好电池 |
| D.燃料电池的能量转化率可达100% |
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成燃料电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是
| A.每消耗1molCH4可以向外电路转移4mol电子 |
| B.负极上CH4失去电子,电极反应式为CH4+10OH—=CO32—+7H2O+8e— |
| C.负极上是O2获得电子,电极反应式为:O2+2H2O+4e—=4OH— |
| D.电池放电后,溶液pH不断升高 |
一种使用阴离子交换膜(只也许阴离子通过)的铜锌电池结构如下图:
以下选项两栏内容正确且相关联的是
| 选项 |
操作与现象 |
解释与推论 |
| A |
电池放电时化学能转化为电能 |
Zn(s) + Cu2+(aq) = Zn2+ + Cu(s) △H>0 |
| B |
该电池充电时铜棒变细 |
两电极区溶液颜色都变深 |
| C |
该电池放电时铜棒是电池正极 |
Cl-通过交换膜从左(铜棒区)向右(锌棒区)移动 |
| D |
该电池充电时a接电源正极 |
电极反应Cu2++2e- = Cu |
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见下图。下列说法正确的是
| A.此电池在常温时也能工作 |
| B.正极电极反应式为:O2+2CO2+4e﹣=2CO32﹣ |
| C.CO32﹣向正极移动 |
| D.a为CH4,b为CO2 |
一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是
A.反应CH4+H2O 3H2+CO,每消耗1molCH4转移12mol 电子 3H2+CO,每消耗1molCH4转移12mol 电子 |
| B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O |
| C.电池工作时,CO32-向电极B移动 |
| D.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
某模拟"人工树叶"电化学实验装置如图所示,该装置能将和
转化为
和燃料(
)。下列说法正确的是()

| A. | 该装置将化学能转化为光能和电能 |
| B. |
该装置工作时,
|
| C. |
每生成
|
| D. |
|
海洋电池,是以铝合金为电池负极,金属(Pt、Fe)网为正极,科学家把正极制成仿鱼鳃的网状结构。用海水为电解质溶液,它靠海水中的溶解氧与铝反应产生电能的。海水中只含有0.5%的溶解氧。不放入海洋时,铝极就不会在空气中被氧化,可以长期储存。用时,把电池放入海水中,便可供电, 电池设计使用周期可长达一年以上,避免经常交换电池的麻烦。即使更换,也只是换一块铝合金板,电池总反应式:4Al+3O2十6H2O=4Al(OH)3↓下列说法错误的是
| A.负极铝被氧化 |
| B.海水温度升高,电池反应速率可能加快 |
| C.正极制成仿鱼鳃的网状结构的目的是增大正极材料和氧气接触面积 |
| D.正极电极反应式为O2+4H+ +4e-=2H2O |
铅蓄电池在现代生活中有广泛应用,其电极材料是Pb 和PbO2,电解液是H2SO4溶液。现用铅蓄电池电解饱和硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法不正确的是
| A.蓄电池放电时,电路中每转移2 mol电子,最多有1 molPbO2被还原 |
| B.电解池的阳极反应式为:4OH--4e-=2H2O+O2↑ |
| C.电解后,c(Na2SO4)不变,且溶液中有晶体析出 |
| D.蓄电池中每生成1mol H2O,电解池中就消耗1mol H2O |
一种基于酸性燃料电池原理设计的酒精检测仪,电池反应的化学方程式为:
CH3CH2OH+O2=CH3COOH+H2O。下列有关说法不正确的是
| A.检测时,电解质溶液中的H+向正极移动 |
| B.若有0.4mol电子转移,则消耗2.24L氧气 |
| C.正极上发生还原反应,负极上发生氧化反应 |
| D.负极上的反应为:CH3CH2OH-4e-+H2O=CH3COOH+4H+ |
铝是一种高能量载体,是开发电池的理想电极材料。如图所示的室温铝二次电池,采用有机阳离子(EMIm)和AlCl4-组成的离子液体为电解液,有关反应为Al+Mn2O4 AlMn2O4下列说法正确的是
AlMn2O4下列说法正确的是
| A.电池放电时,AlCl4-向Y极扩散 |
| B.电池放电时,X是正极 |
| C.电池充电时X极的反应为:4Al2Cl7-+3e-=Al+7AlCl4- |
| D.铝作为负极材料的比能量高于锂 |
下图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是
| A.电流由O2所在的铂电极流出 |
| B.O2所在的铂电极处发生还原反应 |
| C.该电池的负极反应式为:CH3CH2OH+3H2O -12e-=2CO2↑+12H+ |
| D.微处理器通过检测电流大小而计算出被测气体中酒精的含量 |