镁—次氯酸盐燃料电池的工作原理如图,该电池反应为:Mg +ClO - +H2O ="=" Mg(OH)2+ Cl-下列有关说法正确的是
| A.电池工作时,C溶液中的溶质是MgCl2 |
| B.电池工作时,正极a附近的pH将不断增大 |
| C.负极反应式:ClO -—2e - +H2O ="=" Cl- + 2OH- |
| D.a电极发生还原反应,每转移0.2mol电子,理论上生成0.1mol Cl- |
高铁电池是一种新型可充电电池,电解液为KOH溶液,放电时的总反应式为:
3Zn+2K2 FeO4 +8H2O=3Zn(OH)2+2Fe(OH)3 +4KOH
下列叙述正确的是
| A.放电时,正极区溶液的pH减小 |
| B.该电池也可用稀H2SO4代替KOH溶液 |
| C.充电时,电解质溶液中的K+等阳离子向Zn电极移动 |
| D.充电时,每转移3 mol电子,阳极有1 mol Fe(OH)3被还原 |
微型纽扣电池在现代生活中是广泛应用的一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应式分别为:Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-,电池总反应式为Ag2O+Zn===2Ag+ZnO。根据上述反应式,判断下列叙述中正确的是
| A.在使用过程中,电池负极区溶液pH增大 |
| B.在使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应 |
| D.外电路中每通过0.2 mol电子,正极的质量理论上减小1.6 g |
2010年4月中旬全球核安全峰会在华盛顿举行,发展核电、制裁核武器发展是会议主题,各式各样电池的发展是化学对人类的一项重大贡献,下列有关电池的叙述正确的是
| A.手机上用的锂离子电池属于一次电池 |
| B.锌锰干电池中,锌电极是负极 |
| C.氢氧燃料电池工作时氢气在负极被还原 |
| D.太阳能电池的主要材料为二氧化硅 |
人造地球卫星用到的一种高能电池——银锌蓄电池,其电池的电极反应式为Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是
| A.负极,并被氧化 |
| B.正极,并被还原 |
| C.负极,并被还原 |
| D.正极,并被氧化 |
电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重大贡献。下列有关电池的叙述正确的是
| A.锌锰干电池工作一段时间后碳棒变细 |
| B.氢氧燃料电池可将热能直接转变为电能 |
| C.氢氧燃料电池工作时氢气在负极被氧化 |
| D.太阳能电池的主要材料是高纯度的二氧化硅 |
镍镉(NiCd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
Cd(OH)2+2Ni(OH)2  Cd+2NiO(OH)+2H2O由此可知,该电池放电时的负极材料是
Cd+2NiO(OH)+2H2O由此可知,该电池放电时的负极材料是
| A.Cd(OH)2 | B.Ni(OH)2 | C.Cd | D.NiO(OH) |
如图所示是一个燃料电池的示意图,当此燃料电池工作时,下列分析中正确的是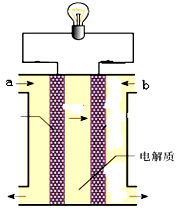
| A.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上发生的反应为:H2-2e-=2H+ |
| B.如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通 O2的电极上发生的反应为:O2+4e-+2H2O=4OH- |
| C.如果a极通入CH4,b极通入O2,NaOH作电解质溶液,则通CH4的电极上发生的 反应为:CH4-8e-+10 OH-=CO32-+7H2O |
| D.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则溶液中的OH-离子向b极附近移动 |
电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重大贡献,下列有关电池的叙述正确的是
| A.锌锰干电池工作一段时间后碳棒变细 |
| B.氢氧燃料电池可将热能直接转变为电能 |
| C.氢氧燃料电池工作时氢气在负极被氧化 |
| D.太阳能电池的主要材料是高纯度的二氧化硅 |
下列叙述中正确的是
| A.Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质 |
| B.燃料电池的能量转化率可达100% |
| C.电解质为NH4Cl的锌锰干电池比电解质KOH锌锰干电池使用寿命长 |
| D.钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高 |
下列有关电化学原理的说法中,错误的是
| A.在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 |
| B.在铜的精炼装置中,通常用粗铜作作阳极,精铜作阴极 |
| C.氯碱工业,主要依托电解熔融的氯化钠来制取工业上重要的化工原料烧碱和氯气 |
| D.可充电的电池称“二次电池”,在充电时,是将电能转变成化学能,在放电时,又将化学能转化成电能 |
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图。下列有关氢氧燃料电池的说法不正确的是
A.由于A、B两电极没有活动性差别,不能构成原电池
B.A电极是负极,电极上发生氧化反应
C.产物为无污染的水,属于环境友好的绿色电池
D.外电路中电流由B电极通过导线流向A电极
利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,下图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图.该电池工作时,有关说法正确的是
| A.铝罐将逐渐被腐蚀 |
| B.炭粒和炭棒上发生的反应为:O2+4e-===2O2- |
| C.炭棒应与玩具电机的负极相连 |
| D.该电池工作一段时间后炭棒和炭粒的质量会减轻 |
二甲醚是一种绿色、可再生的新能源。下图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极)。该电池工作时,下列说法不正确的是
| A.a电极为该电池负极 |
| B.电池工作时,燃料电池内部H+从a电极移向b电极 |
| C.电池工作时,a电极反应式:CH3OCH3—12e-+3H2O═ 2CO2↑+12H+ |
| D.O2在b电极上得电子,电极反应式:O2+4e-+2H2O═ 4OH- |
磷酸铁锂电池结构如右图所示。左边由LiFePO4晶体组成,铝箔与电池一极连接;中间是聚合物隔膜,锂离子可以通过而电子不能通过;右边由石墨组成,铜箔与电池另一极连接,电池内充满电解质。在充电过程中 LiFePO4中的锂离子脱出并伴随着铁元素的氧化。下列说法不正确的是
| A.放电时,铝箔所在电极为负极,铜箔所在电极为正极 |
| B.放电时,电池反应式为:FePO4+Li = LiFePO4 |
| C.充电时,Li+ 向阴极移动 |
| D.充电时,阳极的电极反应式为:LiFePO4 – e— = FePO4+Li+ |