浙江省嘉兴市高三下学期教学测试(二)理综化学试卷
下列说法不正确的是
| A.2014年诺贝尔化学奖授予发明超分辨率荧光显微镜的科学家,他们使光学显微镜分辨率提高到纳米尺度。利用超分辨率荧光显微镜可以观测到胶体中的胶粒。 |
| B.人体从食物中摄取蛋白质,在体内先水解成各种氨基酸,经过不断的分解,最终生成水和二氧化碳排出体外。 |
| C.臭氧是一种有鱼腥味、氧化性极强的淡蓝色气体,可用作自来水的消毒剂。 |
| D.我国油品从国 IV 汽油升级到国 V 汽油,有助于减少酸雨、雾霾,提高空气质量。 |
下列有关实验说法正确的是
| A.在进行中和滴定时,用标准酸溶液润洗酸式滴定管 2~3 次,如果再用蒸馏水洗 2~3 次,效果更佳 |
| B.基于硫代硫酸钠与稀硫酸反应生成S和SO2,在定量分析测定反应速率时,既可用S对标记遮盖法,也可用排水法测 SO2体积,计算出相关的反应速率。 |
| C.燃料电池的制作:用包有薄海绵的两根碳棒做电极电解Na2SO4溶液,一段时间后切断电源,在两极之间接上发光二极管,发现发光。 |
| D.过滤、结晶、灼烧 、萃取、分液和蒸馏等都是常用的分离有机混合物的方法。 |
短周期元素 W、X、 Y 和 Z 的原子序数依次增大。 其中 W 的阴离子的核外电子数与 X、 Y 原子的核外内层电子数相同。X 的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气方法来生产Y的单质,Z 与 X 同族。下列说法中正确的是
| A.以上四种元素的原子半径大小为 W<X<Y<Z |
| B.X 的氢化物与水分子之间可形成氢键 |
| C.已知 Z-Cl 键能比 X-Cl 键能小, 所以 Z 的最简单氯化物比 X 的简单氯化物沸点低。 |
| D.W 与 Y 可形成既含共价键又含离子键的化合物 |
下列说法正确的是
| A.某烷烃的名称为 2-甲基-4-乙基戊烷 |
B.甲醇、乙二醇、丙三醇(结构如右图)互为同系物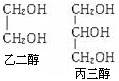 |
| C.淀粉、纤维素、蔗糖都属于天然高分子化合物,而且水解产物中都有葡萄糖 |
| D.等物质的量的乙烯与碳酸二甲酯(CH3OCOOCH3)完全燃烧耗氧量相同 |
磷酸铁锂电池结构如右图所示。左边由LiFePO4晶体组成,铝箔与电池一极连接;中间是聚合物隔膜,锂离子可以通过而电子不能通过;右边由石墨组成,铜箔与电池另一极连接,电池内充满电解质。在充电过程中 LiFePO4中的锂离子脱出并伴随着铁元素的氧化。下列说法不正确的是
| A.放电时,铝箔所在电极为负极,铜箔所在电极为正极 |
| B.放电时,电池反应式为:FePO4+Li = LiFePO4 |
| C.充电时,Li+ 向阴极移动 |
| D.充电时,阳极的电极反应式为:LiFePO4 – e— = FePO4+Li+ |
常温下 0.1mol·L-1亚硫酸溶液中H2SO3、HSO3—、SO32—三者中所占物质的量分数(α)随pH 变化的关系如图所示。下列表述 正确的是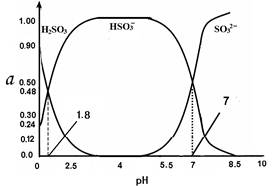
A.H2SO3 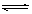 2H+ + SO32—K=10—5.2 2H+ + SO32—K=10—5.2 |
| B.在0.1mol·L H2SO3 溶液中,存在:c2(H+)= c(H+)·c(HSO3—) + 2c(H+)·c(SO32—) + Kw |
| C.在pH="2.5" 溶液中: c(H2SO3)>c(HSO3—)>c(H+) >c(OH—) |
| D.向pH 为 8.5 的上述体系中通入极少量 Cl2的过程中,溶液中c(HSO3—)和c(SO32—)均减小 |
检验某溶液中是否含有 K+、Fe3+、Cl- 、Mg2+、I- 、CO32- 、SO42-,限用的试剂有:盐酸、硫酸、硝酸银溶液、硝酸钡溶液。设计如下实验步骤,并记录相关现象。下列叙述不正确的是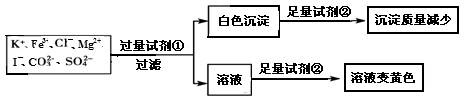
| A.该溶液中一定有 I- 、CO32- 、SO42- 、K+ |
| B.试剂①为硝酸钡 |
| C.通过在黄色溶液中加入硝酸银可以检验原溶液中是否存在Cl- |
| D.试剂②一定为盐酸 |
(10 分)有机物 G 是一种医药中间体,常用于制备抗凝血药。可以通过下图所示的路线合成有机物 G。
已知:1. 
2. 
请回答下列问题:
(1)葡萄糖的分子式是 ,写出 G 中所含含氧官能团的名称 。
(2)由 A 转化为 B 的化学方程式为 。
(3)已知 D 的分子式为 C7H6O3,则 D 的结构简式为 。
(4)在上述转化过程中,属于取代反应的有 (填选项序号)。
①葡萄糖→A ②D→E ③B→C ④E + CH3COCl→ F
(5)写出 F 与足量的氢氧化钠反应生成的有机物的结构简式 。
(18 分)(Ⅰ) 将某红棕色气体 A 通入到稀钠盐溶液甲中,有白色沉淀产生;当红棕色气体通入过量时,白色沉淀逐渐完全消失。上述过程中还产生一种无色气体B,B 遇空气后又可产生 A。则:
(1)写出钠离子的结构示意图 ; B 与空气反应的化学方程式 。
(2)甲中肯定不含有下列物质中的 ;(填选项字母)。
A.Na2S B.NaAlO2 C.Na2SiO3 D.NaCl
(3)通入气体 A 使白色沉淀逐渐消失且产生气体 B,该反应的离子方程式是 。
(Ⅱ)某研究小组为了探究一种无机化合物X(化合物 X 中带有 6 个结晶水,仅含五种元素,且每种元素在该化合物中均只有单一价态,X 的式量为400)的组成和性质,设计了如下实验:
(注明:以上气体体积均在标准状况下测定,产物中只有水未标出)
(1)写出气体B 的电子式 ,气体 D 的结构式 。
(2)混合气体 C 通入品红溶液褪色,加热后恢复原色的原因是 。
(3)8.00 固体 X 所含阴离子的物质的量是 mol。
(4)固体X 受热分解的化学方程式是 。
(15 分)二甲醚是一种重要的化工原料,利用水煤气(CO、H2)合成二甲醚是工业上的常用方法,该方法由以下几步组成:
2H2(g) +CO(g)  CH3OH(g) ΔH=" —90.0" kJ· mol-1 ①
CH3OH(g) ΔH=" —90.0" kJ· mol-1 ①
2CH3OH(g)  CH3OCH3(g) + H2O(g) ΔH="—24.5" kJ· mol-1 ②
CH3OCH3(g) + H2O(g) ΔH="—24.5" kJ· mol-1 ②
CO(g) + H2O(g) CO2(g) + H2(g) ΔH="—41.1" kJ· mol -1 ③
CO2(g) + H2(g) ΔH="—41.1" kJ· mol -1 ③
(1)反应①的 ΔS 0(填“>”、“<”或“=”)。在 (填“较高”或“较低”)温度下该反应自发进行。
(2)在 250℃的恒容密闭容器中,下列事实可以作为反应③已达平衡的是_______(填选项字母)
| A.容器内气体密度保持不变 |
| B.CO 与 CO2的物质的量之比保持不变 |
| C.H2O 与 CO2的生成速率之比为 1∶1 |
| D.该反应的平衡常数保持不变 |
(3)已知一些共价键的键能如下:
运用反应①计算一氧化碳中碳氧共价键的键能 kJ· mol-1。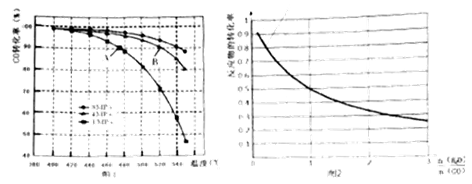
(4)当合成气中 CO 与 H2的物质的量之比恒定时,温度、压强对 CO 转化率的影响如图 1 所示。图 1 中 A 点的 v(逆) B 点的 v(正)(填“>”、“<”或“=”),说明理由 。实际工业生产中该合成反应的条件为 500℃、4MPa 请回答采用 500℃的可能原因 。
(5)一定温度下,密闭容器中发生反应③,水蒸气的转化率与 n(H2O)∕n(CO)的关系如图2所示。计算该温度下反应③的平衡常数 K= 。
在图 2 中作出一氧化碳的转化率与 n(H2O)∕n(CO)的曲线。
(15 分)K3[Fe(C2O4)3]· 3H2O(三草酸合铁酸钾晶体)为翠绿色晶体, 溶于水, 难溶于乙醇, 110℃下失去结晶水,230℃分解;是制备负载型活性铁催化剂的主要原料。 实验室利用(NH4)2Fe(SO4)2· 6H2O (硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、30%双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下: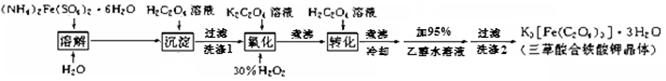
已知:沉淀:FeC2O4 · 2H2O 既难溶于水又难溶于强酸
6FeC2O4 + 3H2O2 + 6K2C2O4 = 4K3[Fe(C2O4)3] + 2Fe(OH)3↓
2Fe(OH)3 + 3H2C2O4 + 3K2C2O4 = 2K3[Fe(C2O4)3] + 6H2O
(1)检验硫酸亚铁铵是否变质的试剂是 ;溶解时加几滴稀硫酸的目的是 。
(2)硫酸亚铁铵溶液与 H2C2O4溶液反应生成 FeC2O4 · 2H2O 沉淀,写出该反应方程式 ;沉淀过滤后,洗涤 1 的操作方法是 。
(3)在沉淀中加入饱和 K2C2O4 溶液,并用 40 ℃ 左右水浴加热,再向其中慢慢滴加足量的 30% H2O2 溶液,不断搅拌。此过程需保持温度在 40 ℃ 左右,可能的原因是 。加入30%过氧化氢溶液完全反应后,煮沸的目的是 。
(4)洗涤 2 中所用洗涤试剂最合适的是 (填选项字母)。
| A.草酸钠溶液 | B.蒸馏水 | C.乙醇 | D.KCl 溶液 |
(5)为了不浪费药品,95%乙醇水溶液进行回收的方法是 ,所用的主要玻璃仪器有 (任写两种)等。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号