以下是氯化钠溶液的配制和粗盐中难溶性杂质的去除(需要计算粗盐的产率)实验活动中的部分操作。
(1)仪器a的名称是 。
(2)完成粗盐提纯的实验上图中正确的操作顺序为 (填字母序号)。
(3)配制6%的氯化钠溶液和粗盐中难溶性杂质的去除都要用到的实验操作是 (填序号)。
(4)A中玻璃棒搅拌的作用是使氯化钠 。如果B中的滤液仍然浑浊,就应该 。D操作中,当观察到蒸发皿中出现 时,停止加热。
(5)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 。
| A.增加适量氯化钠固体 | B.减少适量氯化钠固体 |
| C.调节游码 | D.添加砝码 |
(6)用提纯得到的精盐配制了50 g 6%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有 (填序号)。
①氯化钠固体仍然不纯 ②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,有少量溶液洒出
某同学欲用98%的浓H2SO4(ρ=1.84g/cm3)配制成100g 10%的稀H2SO4:
(1)填写下列操作步骤:
①所需浓H2SO4的体积为 。
②如果实验室有a、10mLb、20mLc、50mLd、100mL量筒,应选用 (填字母序号)量筒量取。读数时,使液体的 正好跟刻度相平。;
③将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的烧杯里。
④用 不断搅拌。
(2)请指出上述操作中一处明显错误: 。(填写操作步骤中的序号)
(3)误差分析:(填偏高、偏低、无影响)操作②中量取时发现量筒不干净,用水洗净后直接量取,所配溶液的溶质质量分数将 。
(4)小王想粗略测定所配溶液的酸碱度可选用 ,请你告诉他如何操作 。
小华实验操作考试的题目是:配制一定溶质质量分数的碳酸钠溶液并测定其酸碱度.考试时,小华进行了如下图所示的操作:
(1)请填写标号仪器的名称:a ;b .
(2)以上实验的正确操作顺序为 (用序号字母表示).
(3)上图所示的操作中,若C中砝码的质量为10g,游码的读数为3.5g,则碳酸钠的实际质量为 g.
(4)小华在测定所配制溶液的酸碱度时,先将pH试纸用蒸馏水湿润,再进行测定,则测的溶液的pH值 (选填“偏大”、“偏小”或“不受影响”).
(5)用pH试纸测定所配制溶液的pH,正确操作方法为 .
海洋为我们提供了丰富的资源,二十一世纪是海洋开发与利用的世纪,请围绕“海洋”这个话题回答以下问题:
(1)下图1是我们从海水中提取镁的流程图:
①上述一系列转化过程中,属于中和反应的是 (用化学方程式表示)
②海水制镁过程中对于如何富集镁离子,甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳.
乙:高温加热蒸发海水后,加入石灰乳.
丙:向晒盐后的卤水中,加入石灰乳.
通过分析比较,你认为 的设想最为经济合理(选填“甲”、“乙”或“丙”).
(2)关于海水“制碱”中得到的“碱”的成分,甲同学认为是氢氧化钠,乙同学认为是碳酸钠,为确定其成分,甲、乙同学各做了以下两个实验:
①甲向“碱”溶液中加入酚酞,观察到酚酞变红,于是认为“碱”是氢氧化钠.
②乙向“碱”溶液中加入氢氧化钙溶液,产生白色沉淀,于是认为“碱”是碳酸钠.
你同意 (填甲或乙)同学的观点,请指出另一个同学实验设计的不合理之处
(3)从海水晒盐留下的“苦卤”中加工得到不纯的硫酸镁晶体,其中含有少量氯化钠,根据溶解度曲线图2回答下列问题:
①t1℃时,等质量的水中最多溶解的硫酸镁质量 (填大于、小于或等于)最多溶解的氯化钠的质量.
②t2℃时,向50克水中加入50克硫酸镁,所得溶液的溶质质量分数是 .
③要除去少量的氯化钠,得到较纯净的硫酸镁,可采用的方法是 .
A.过滤
B.蒸干水分
C.将t2℃硫酸镁的饱和溶液升温,析出晶体后过滤.
请根据下列所示的实验过程和提供的数据,试回答下列问题:
(1)在滴入稀盐酸的过程中,观察到的明显现象是 .
(2)该反应过程中生成的CO2气体的质量 .
(3)求最终所得溶液中溶质的质量是多少?(请写出规范的计算过程,并且最后结果保留一位小数)
实验室欲用已配好的质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),配制100g质量分数为5%的氢氧化钠溶液,并用此溶液测定某硫酸溶液的溶质质量分数。
(1)配制100g质量分数为5%的氢氧化钠溶液,需要10%的氢氧化钠溶液 g。
(2)配制氢氧化钠溶液时,需要的玻璃仪器有 、滴管、烧杯、玻璃棒。
(3)用配得的氢氧化钠溶液与待测溶质质量分数的硫酸溶液反应,实验过程中溶液的pH变化曲线如图所示:
①根据如图变化曲线,判断进行的操作是 (填字母)。
A.将硫酸溶液逐滴滴加到氢氧化钠溶液中
B.将氢氧化钠溶液逐滴滴加到硫酸溶液中
②b点对应的溶液中的溶质为 (写化学式)。
(4)若完全中和50g稀硫酸溶液,恰好消耗配得的氢氧化钠溶液80g,试计算该稀硫酸的溶质质量分数(请写出计算过程)
无土栽培是利用营养液栽培作物的一种方法(如图1)。
(1)下列化学肥料中属于复合肥的是 (填序号)。
①硝酸铵 ②碳酸氢铵 ③硝酸钾 ④硫酸钾
(2)小军要配制50g溶质质量分数为24%的硝酸钾溶液,需硝酸钾质量为 g。
(3)如图2A所示,称量时A出现了右盘低的现象,接下来的操作应该是 。
①左边的平衡螺母向左调至天平平衡 ②移动游码至天平平衡
③右盘中减少砝码至天平平衡 ④左盘中添加食盐至天平平衡
(4)量取水时,如果按照图2B的方法读数,会使配制的溶液溶质质量分数 (填“偏大”或“偏小”);图2C中用玻璃棒搅拌的作用是 。
(5)现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图3所示的实验。
根据以上实验,请你进行有关推断。
①由实验1可确定原营养液中一定没有的物质是 ;
②根据实验1、实验2推测原营养液的组成可能有 种情况;
③若测得原营养液中K+和Cl一的数目之比为3:1,则原营养液的组成中的溶质是 。
下图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图: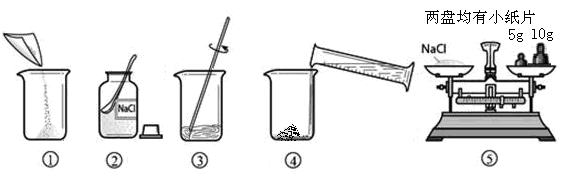
(1)用上图表示的序号表示配制溶液的正确操作顺序_______________________。
(2)图②中,有一种塑料仪器,其名称是___________。
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数见图,则称取的NaCl质量为 。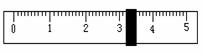
(4)根据计算需要量取水的体积是 (水的密度为1g/mL)。量取读数时,视线应与 齐平。
无土栽培是利用营养液栽培作物的一种方法。
(1)小军要配制50g溶质质量分数为24%的硝酸钾溶液,需硝酸钾质量为 g。
(2)量取水时,如果按照图A的方法读数,会使配制的溶液溶质质量分数 (填“偏大”或“偏小”);B中用玻璃棒搅拌的作用是 。
请你参与配制一定溶质质量分数的氢氧化钠溶液,并进行有关计算。
(1)小红同学在实验室欲配制10%的氢氧化钠溶液143g,请回答:
①配制 10%的氢氧化钠溶液143g,需要40%的氢氧化钠溶液(密度为1.43g/cm3) mL,加水 mL
(结果保留一位小数)。
②实验中,必需用到的仪器有 。
(2)将一定质量的二氧化碳通入 200g10%的氢氧化钠溶液中,恰好完全反应,反应的化学方程式为 ,生成的碳酸钠的质量是 g。
实验室需要配制50 溶质质量分数为4%的氢氧化钠溶液,所需固体氢氧化钠的质量为 ,主要操作步骤是:计算、、溶解.在溶解过程中用玻璃棒搅拌,其作用是.在量取水的过程中,某同学仰视读数,会使所配置的溶液中溶质质量分数(填"偏大""偏小"或"不变").
同学们在实验室对含有泥沙的粗盐进行提纯,实验的基本流程如下:
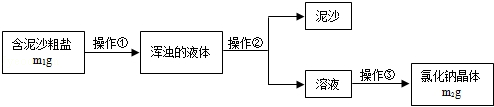
(1)操作②的名称是;
(2)操作①②③都要用到的一种玻璃仪器是,在操作③中,使用这种玻璃仪器的目的是.
(3)计算所获得的氯化钠产率,发现产率偏低,由实验不当导致的可能原因是(只写一种原因).
(4)用提纯所得的氯化钠溶液配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能的原因是(填字母编号).
a、称量氯化钠所用天平砝码沾有杂质;b、用量筒取水时俯视读数;c、用量筒取水时仰视读数;d、配制溶液的烧杯用蒸馏水润洗过
(5)若用6%的氯化钠溶液(密度为1.04g/cm3),配制16g质量分数为3%的氯化钠溶液,需要6%的氯化钠溶液ml(结果保留小数点后一位).
实验室配制一定量10%的氢氧化钠溶液.
(1)用8.0
氢氧化钠固体配制10%的氢氧化钠溶液,需要水
.
(2)氢氧化钠固体溶解时要用玻璃棒搅拌,其目的是.
(3)将配好的溶液倒入洗净后未晾干的细口瓶中,溶液的溶质质量分数(填"不变"、"变大"或"变小").
无土栽培是一种在营养液中培育植物的农业高新技术。因为硝酸钾属于 肥料,所以常用于配制营养液。小强要用5%的KNO3 溶液配制150 g 溶质质量分数为2%的硝酸钾溶液,配制此硝酸钾溶液的步骤为计算、 、 ;