实验室用固体氯化钠配制50g5%的氯化钠溶液的主要实验步骤有:
①称量 ②溶解 ③计算 ④装瓶。
(1)配制过程的先后顺序是(用序号表示) ;
(2)配制过程中用到的仪器有天平、药匙、量筒、烧杯和 ;
(3)其他操作都正确,装瓶时不慎将少量氯化钠溶液倒在了瓶子外边,则最后得到的氯化钠溶液的溶质质量分数 5%(填“大于”、“小于”或“等于”).
如图AB两种固体物质的溶解度随温度变化的曲线。请回答
(1) ℃时,A、B两物质的溶解度相等
(2)20℃时,A物质的溶解度 B物质的溶解度(填“>”、“<”或“=”)。
(3)现有50℃时A物质的不饱和溶液在不减少溶剂的情况下,欲使其变成饱和溶液,下列措施肯定不能实现的是 (填序号)。①降低温度 ②升高温度 ③加入A物质
下面表格中列出了NH4Cl在不同温度下的溶解度:
| 温度/℃ |
0 |
20 |
40 |
60 |
| 溶解度/g |
29.4 |
37.2 |
45.8 |
55.2 |
(1)由上表可推出NH4Cl的溶解度随温度的变化规律是 ;
(2)在20 ℃时,向100 g水中加入50 g NH4Cl,形成 (填“饱和”或“不饱和”)溶液,将其温度升高到60 ℃时,形成的溶液中溶质与溶剂的质量比为 。
如图是a、b两种固体物质的溶解度曲线。试回答:
(1)t ℃时,两物质溶解度大小关系为a b(填“>”“<”或“=”);
(2)当a中含有少量b时,可以用 法提纯a;
(3)在 ℃时,a、b的溶解度相等,此温度下所得溶液中溶质的质量分数最大为 。
下图是配制50 g质量分数为9%的氯化钠溶液的操作过程部分示意图,请你完成:
(1)A操作中的错误是____________________。
(2)B操作中所用仪器的名称是________________。
(3)D操作中应选用____________(填“10 mL”“50 mL”或“100 mL”)的量筒量取 ________mL水。
(4)E操作的作用是__________________。
(5)在配制时,下列操作可能导致溶质质量分数小于9%的是________(填序号)。
①称量时砝码和食盐放颠倒
②C操作中有固体撒落
③D操作中有少量水溅出
④将配好的氯化钠溶液转移到细口瓶中时,不慎洒出部分溶液
(6)将按正确方案配制好的溶液倒入试剂瓶中,盖上瓶盖,并贴上标签。请你把如图标签填写完整:
化学实验室取用16 g硫酸铜粉末,可配制8%的硫酸铜溶液___________g;若用20%的硫酸铜溶液100 g加水稀释,可得8%的硫酸铜溶液________________g。
实验室欲配制1 000 g溶质质量分数为4%的氢氧化钠溶液。请回答下列问题;
(1)配制步骤
①计算:需氢氧化钠固体 g,水960mL(水的密度是1 g/cm3)。
②称量:用质量为23.1 g的烧杯作称量容器,托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在左盘。
③溶解:将氢氧化钠固体溶于水,用玻璃棒搅拌,使氢氧化钠全部溶解,冷却至室温。
④装瓶:把配好的溶液装入试剂瓶,盖好瓶盖并贴上标签,放入试剂柜中。
请在装有所配制溶液的试剂瓶(见右图)标签上标明相应的信息。
(2)在配制过程中,导致溶液中氢氧化钠质量分数小于4%的可能原因是
①用量筒量取水时俯视读数;②配制溶液的烧杯用少量蒸馏水润洗;③用托盘天平称取氢氧化钠,将氢氧化钠放置在右盘;④盛装溶液的试剂瓶用蒸馏水润洗;⑤氢氧化钠固体不纯。
(3)若老师提供的药品有500 g 8%的氢氧化钠溶液,500 g 1%的氢氧化钠溶液,足量的氢氧化钠固体和水,除了上述配制方案外,你还可以设计出哪些配制方案,请你写出其中的一种: .(只要说明配制时所需的各种药品及用量即可)。
下图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
(1)用上图表示的序号表示配制溶液的正确操作顺序_______________________。
(2)图②中,有一种塑料仪器,其名称是___________。
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数见图,则称取的NaCl质量为 。
(4)根据计算需要量取水的体积是 (水的密度为1g/mL)。量取读数时,下图视线角度正确的是_____。(选填字母标号)
(5)称量NaCl质量完毕放回砝码时,发现有一个砝码缺损了一个小角,若其他操作步骤正确,则所配溶液的溶质质量分数 (填“大于”、“小于”或“等于”)10%。
如图是甲、乙两种固体物质的溶解度曲线。
(1)t2℃时,甲物质的溶解度为____________;
(2)从图中你还能获得哪些信息?(任填一条)______________________________________;
(3)分析t1℃时,将10g乙物质放入100g水中,充分溶
解后所得的溶液是________(填“饱和”或“不饱和”)溶液。欲使t2℃时乙物质的饱和溶液变为不饱和溶液,可采取的方法是______________(任填一种方法)。
配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行.
请回答下列问题:
(1)计算配制100g溶质质量分数为5%的氯化钠溶液所需:氯化钠___g,水____ml(水的密度为1g/ml),应选________量筒(10ml 、 50ml、100ml 、200ml)
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应( )
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节平衡螺母 D.向右盘加砝码
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是
(4)下列操作会导致所配制溶液溶质质量分数偏低的是
A.称量时药品和砝码放反了 B.只在称量食盐的托盘垫上了干净的纸
C.量取溶剂时,俯视量筒读数 D.把配制好的溶液倒入试剂瓶时有部分溅出
某校进行中考化学实验考查,给出以下三个考题:①粗盐提纯;②二氧化碳的制取和收集;③氧气的制取和收集。考查规定由学生抽签确定考题。
I.甲同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:
(1)上图中仪器A的名称是 ;甲同学抽到的考题是 (填序号);实验前甲同学发现其中缺少了一种药品,该药品是 ;写出该实验反应的化学方程式 ;
(2)若另选药品,也能完成另一个考题的气体制备,其中的化学方程式为 。
II.乙同学抽签并完成实验后,监考老师要他回答如下问题,请你帮他回答。
(3)粗盐中除混有泥沙等难溶性杂质外,通常还含有MgCl2等可溶性杂质,为了除去MgCl2.可以加入适量的试剂是 。
(4)如图是用托盘天平称量烧杯的质量时,天平平衡后的状态,错误操作是 ,烧杯的实际质量是 g。
无土栽培是利用营养液栽培作物的一种方法.
(1)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量
为 g.
(2)现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验.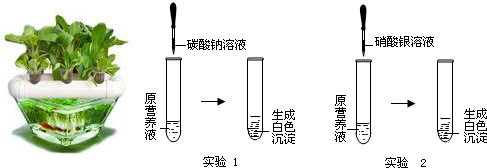
根据以上实验,请你进行有关推断.
①由实验1可确定原营养液中一定没有的物质是 。
②根据实验1、实验2推测原营养液的组成可能有 种情况;
③若测得原营养液中K+和Cl一的数目之比为1:1,则原营养液的组成中的溶质是
实验室用浓盐酸(溶质质量分数为37%,密度为1.18g·mL-1)配制100g溶质质量分数为10%的稀盐酸。
(1)计算:需要浓盐酸 mL,水 mL。(结果保留小数点后一位)
(2)量取:用规格为 mL的量筒(从50mL、100 mL中选择)量取浓盐酸,倒入烧杯中,再用规格为 mL的量筒(从50mL、100 mL中选择)量取水。
(3)稀释:_ 。
实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数。现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶段加入,溶液液的pH的变化如图所示。试回答:
(1)a点溶液中含有的离子有____________________________。
(2)当pH=7时,消耗NaOH溶液中NaOH的质量为____________。
(3)计算稀H2SO4的溶质质量分数。
(届上海市浦东区第一学期期末试题)下图是甲、乙两种固体(不含结晶水)在不同温度下的溶
解度(单位:g/100g水)
| 温度(℃) |
0 |
20 |
40 |
60 |
80 |
90 |
100 |
| 甲 |
13.3 |
32 |
64 |
110 |
169 |
202 |
246 |
| 乙 |
35.7 |
36 |
36.6 |
37.3 |
38.4 |
39 |
39.8 |
①60℃时甲的溶解度为 ⑺ g/100g水,将60g甲放入50g水中充分溶解得到溶液 ⑻ g。
②从乙的溶液中提取乙的方法是 ⑼ (填“降温结晶”或“蒸发结晶”)。
③分别将100g甲、乙的饱和溶液从60℃降温至20℃,对所得溶液的叙述正确的是 ⑽ 。
A.甲、乙均为饱和溶液 B.溶液质量:甲>乙
C.所含溶剂质量:甲<乙 D.溶质质量分数:甲>乙