恒温下,将a mol N2与b mol H2的混合气体通入一定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,
计算a= 。
(2)反应达到平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的百分含量(体积分数)为25%。计算:平衡时NH3的物质的量为 。
(3)原混合气体与平衡混合气体的总物质的量之比
n(始): n(平)= 。
(4)原混合气体中a : b= 。
(5)达到平衡时,N2和H2的转化率 (N2):
(N2):  (H2)= 。
(H2)= 。
(6)平衡混合气体中n(N2): n(H2): n(NH3)= 。
373K时,某 1L密闭容器中加入1molPCl5发生如下可逆反应: 其中物质PCl3的物质的量变化如右图所示。
其中物质PCl3的物质的量变化如右图所示。
(1 )前 20
)前 20 s内 PCl5(g)的平均反应速率为
s内 PCl5(g)的平均反应速率为
(2)373K时该反应的平衡常数的值为
(3)若在此平衡体系中再加入 1mol的 PCl5,与原平衡比较,新平衡时 PCl5的转化率 (填“增大”或“减小”,下同)。PCl5的平衡浓度 。
(4)将原平衡升温至 473K,重新达平衡时(其他条件不变),PCl3的平衡浓度为 PCl5的3倍,该反应的正反应为(填“放热反应”或 “吸热反应”) ,为增大平衡体系中 Cl2的物质的量,下列措施正确的是(其它条件相同)
a.升高温度 b.扩大容器的体积
c.加入合适的催化剂 d.再充入 PCl3
在一定温度和压强下,有如下反应:2SO2(g)+O2(g) 2SO3(g),将1.6 mol SO2和0.8 mol O2放人一体积可变的密闭容器中,测得容器的起始容积为100L。经一段时间后,反应达到平衡,测得混合气体的密度为1.6g·L-1。请回答下列问题:
2SO3(g),将1.6 mol SO2和0.8 mol O2放人一体积可变的密闭容器中,测得容器的起始容积为100L。经一段时间后,反应达到平衡,测得混合气体的密度为1.6g·L-1。请回答下列问题:
(1)达平衡时混合气体的体积为______________L,SO2的转化率为______________。
(2)若起始时加入a mol SO2、b mol O2,且a:b=2:1,在同样温度和压强下,反应达到平衡 时,测得混合气体的容积为120L。则a、b的值分别为:a=______________,b=______________。
时,测得混合气体的容积为120L。则a、b的值分别为:a=______________,b=______________。
(3)若容器为体积不变的密闭容器,其容积为100L。起始时加入χmol SO2、y mol O2和z mol SO3,反应达平衡时,温度和压强与(2)完全相同,容器内各气体的体积分数也与(2)达平衡时的情况完全相同,则χ、y应该满足的关系式为______________,χ、z应该满足的关系式为______________。
下图表示的是N2 + 3H2 2NH3;△H<0达到平衡后,改变条件建立的新平衡(图中横坐标表示反应时间, 纵坐标表示反应速率)
2NH3;△H<0达到平衡后,改变条件建立的新平衡(图中横坐标表示反应时间, 纵坐标表示反应速率) 

(1)表示减少H2的量而建立新平衡的是 。
(2)表示压缩气体, 体积减小而建立新平衡的是 。
(3)表示降低温度而建立新平衡的是 。
(4)表示升高温度而建立新平衡的是 。
(5)表示加入催化剂后而建立新平衡的是 。
汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,反应原理:2NO(g)+2CO(g)===N2(g)+2CO2(g),在298 K、100 kPa下,ΔH=-113 kJ/mol,ΔS=-145 J/(mol·K).
(1)为了提高该反应的速率和NO的转化率,采取的正确措施为________.
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
(2)该反应达到平衡时若缩小体积,则混合气体的平均相对分子质量________,若升高温度,则该反应的平衡常数________(均填“增大”、“减小”或“不变”).
(3)该条件下反应__________________(填“能”或“不能”)自发进行.
(4)在如图中画出在某时刻条件改变后的图象(其他条件不变).
t1:增大NO的浓度
t2:降低温度
一定温度下,将2mol A和2mol B两种气体混合于体积为2 L的某恒容的密闭容器中,发生如下反应:3A(g)+B(g) x C(g)+2D(g),
x C(g)+2D(g), H <0,2min 末反应达到平衡状态(温度不变),生成了0.8 mol D,并测得C的浓度为0.4 mol/L,请填写下列空白:
H <0,2min 末反应达到平衡状态(温度不变),生成了0.8 mol D,并测得C的浓度为0.4 mol/L,请填写下列空白:
(1)X的值等于 ,
(2)该反应的化学平衡常数K= ,升高温度时K值将
(填“增大”、“减小”、“不变”)
(3)A物质的转化率为 。
(4)若维持温度不变,在原平衡混合物的容器中再充入3mol C和3mol D,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入B的物质的量为 mol;达新平衡时,A的物质的量为n(A)= mol。
在一个固定容积的密闭容器中,在一定温度下发生下列反应:
A(g)+B(g)→2C(g),起始加入1molA和2molB,反应达到平衡后测得C的浓度为
p mol/L,且C的体积分数为ω。在相同条件下:
(1)若在相同容器中加入2molA和4molB,达平衡后,C的物质的量浓度为_______mol/L;
(2)若在相同容器中加入0.5molC,要求平衡后C的浓度为0.5p mol/L,且C的体积分数为ω,则还应在容器中加入A______mol,B______mol;
(3)若在相同容 器中加入a mol A、b mol B、c mol C,并要求平衡后C的浓度为p mol/L,C的体积分数仍为ω,则a、b、c应符合的关系是__________________________(其中一个只含a和b,另一个只含a和c)。
器中加入a mol A、b mol B、c mol C,并要求平衡后C的浓度为p mol/L,C的体积分数仍为ω,则a、b、c应符合的关系是__________________________(其中一个只含a和b,另一个只含a和c)。
常温下,将0.01 mol NH4Cl和 0.002 mol NaOH 溶于水配成1 L混合溶液,
!)该溶液中存在的三个平衡体系是:______________________________、
_______________________________、_______________________________。
溶液中共有_______种不同的粒子。
这些粒子中浓度为0.01 mol/L 的是_________,浓度为0.002 mol/L 的是_________。
(4)物质的量之和为0.01 mol的两种粒子是:___________和______________。
(5)_______和_______ 两种离子数量之和比OH-多0.008mol。
⑴高温下,某反应达到平衡,平衡常数K=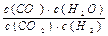 。
。
①该反应化学方程式为 。
②若恒容时,温度升高,H2浓度减小,则该反应焓变为 (填正值或负值)。
③恒温恒压下,若继续向原平衡混合物的容器中通入少量氦气(假设氦气和各物质不反应)后,化学平衡 移动;反应物的转化率 (填增大、减小、或不变);H2的浓度
(填增大、减小、或不变);
⑵可逆反应: X+ 3Y(g)  2Z(g) +2W(g)达到平衡,混
2Z(g) +2W(g)达到平衡,混
合物中Y的体积分数随压强(P)与温度T(T2>T1)的变化关系如图示。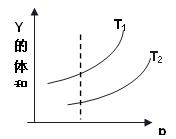
①当压强不变时,升高温度,Y的体积分数变 ,
平衡向 方向移动,则正反应是 热反应。
②当温度不变时,增大压强,Y的体积分数变 ,
平衡向 方向移动,则X的状态是
反应N2+3H2 2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2 )= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2 )= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
(1)求达到平衡时, H2和NH3的浓度分别为c (H2 )= mol/L,c (NH3)=" " mol/L
(2)求平衡时H2的转化率为 ;求平衡时NH3的物质的量与平衡后总物质的量的比值为
(3)求该温度下的平衡常数为 ;达到平衡后,提高温度,则平衡 (填正移,逆移或不移动);K值 ;H2的转化率 (后两个空填增大,减小或不变)
在稀氨水中存在平衡:NH3+H2O NH
NH +OH-,如进行下列操作,则NH3、NH
+OH-,如进行下列操作,则NH3、NH 、H+、OH-浓度及PH值如何变化?(试用“增大”“减小”“不变”填写。)(1)通适量HCl气体时,c(NH3) ,c(H+) ,PH值 。
、H+、OH-浓度及PH值如何变化?(试用“增大”“减小”“不变”填写。)(1)通适量HCl气体时,c(NH3) ,c(H+) ,PH值 。
(2加入少量NaOH固体时,c(NH ) ,c(OH-) ,PH值 。
) ,c(OH-) ,PH值 。
(3)加入NH4Cl晶体时,c(NH ) ,c(OH-) 。
) ,c(OH-) 。
在水的电离平衡中, 和
和 的关系如下图所示:
的关系如下图所示:
(1)A点水的离子积为1×10-14,B点水的离子积为 。造成水的离子积变化的原因是 。
(2)25℃时, 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: ,
,

 。
。
① 0.1 mol/L 溶液的pH 1(填“>”、“<”或“=”)。
溶液的pH 1(填“>”、“<”或“=”)。
②在0.1 mol/L 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是:
。
(3)100℃时,0.01 mol/L 溶液的pH = 。
溶液的pH = 。
(4)100℃时,将pH =8的 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则 溶液与盐酸的体积比为 。
溶液与盐酸的体积比为 。
在一定体积的密闭容器中,进行如下化学反应:

 ,其化学平衡常数K和温度T的关系如下表:
,其化学平衡常数K和温度T的关系如下表:
| T/℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 (填“吸热”或“放热”)反应。
(3)能判断该反应已达到化学平衡状态的依据是( )
| A.容器中压强不变 | B.混合气体中 不变 不变 |
C. |
D.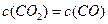 |
(4)某温度下,平衡浓度符合下式: ,试判断此时的温度为 ℃。
,试判断此时的温度为 ℃。
中学常用淡黄色的pH试纸测定溶液的酸碱性。在25℃时,若溶液的pH=7,试纸不变色;若pH< 7 ,试纸变红色;若pH > 7,试纸变蓝色。
⑴已知水中存在如下平衡: H2O + H2O  H3O+ + OH-。现要使平衡向右移动,且所得的溶液呈酸性,选择的方法是
H3O+ + OH-。现要使平衡向右移动,且所得的溶液呈酸性,选择的方法是
| A.向水中加入NaHSO4 | B.向水中加入Cu(NO3)2 | C.加热至100℃ | D.向水中加入(NH4)2SO4 |
⑵现要用pH试纸测定100℃沸水的pH。若则试纸显 色,溶液呈 性(填酸、碱或中)。
⑶纯碱因水溶液显碱性而得名。请用离子方程式表示显碱性的原因:
。