将0.06molFeCl2加入100mLK2Cr2O7溶液中,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72﹣还原为Cr3+.则K2Cr2O7溶液的物质的量浓度为
| A.0.05mol/L | B.0.1mol/L | C.0.2mol/L | D.0.3mol/L |
下列有关的计算分析不正确的是
| A.在反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O中,当有1 mol铜被氧化时,被还原的硝酸为2/3mol |
| B.将a mol硫化亚铁放入含3a mol H2SO4的浓硫酸中,充分反应后,氧化、还原产物分别是Fe3+、S和SO2,则放出的气体少于1.5a mol |
| C.室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧。则a、b的关系为a=4b+3c |
| D.某溶液100 mL,其中含硫酸0.03 mol,硝酸0.04 mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015 mol |
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
| A.反应中转移电子的物质的量是0.21 mol |
| B.ClO3-的生成是由于温度升高引起的 |
| C.苛性钾溶液中KOH的质量是16.8 g |
| D.氯气被还原成0.06 mol ClO-和0.03 mol ClO3- |
在标准状况下,0.0672L H2S气体通入含有1.0×10-3mol X2O72-离子的酸性溶液中,两者恰好完全反应,而且H2S全部被氧化成硫单质,则X元素在还原产物中的化合价为

| A.+3 | B.+4 | C.+2 | D.+1 |
将4.48g Fe溶于1L 0.2mol·L-1的稀硫酸,再加入50mL 0.4mo1·L-1KNO3溶液后,其中的Fe2+全部转化成Fe3+,NO3-无剩余,生成一种氮氧化物NYOX。则该氮氧化物的化学式是
| A.N2O | B.NO | C.N2O3 | D.NO2 |
硫代硫酸钠(Na2S2O3)可作为还原剂,已知25.0mL0.0100mol/LNa2S2O3溶液恰好把22.4mL(标准状况下)Cl2完全转化为Cl 离子, 则S2O32- 将转化成( )
离子, 则S2O32- 将转化成( )
| A.S2- | B.S | C.SO32- | D.SO42- |
1.92gCu投入一定量的浓HNO3溶液中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下的气体672 mL,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的氧气,恰好使气体完全溶于水,则通入的氧气的体积(标况)为
| A.168 mL | B.504 mL | C.336 mL | D.448 mL |
将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断正确的是
| A.与NaOH反应的氯气一定为0.3 mol |
| B.若反应中转移的电子为n mol,则0.15<n<0.25 |
| C.n(Na+):n(Cl-)可能为7:3 |
| D.n(NaCl):n(NaClO):n(NaClO3)可能为8:2:1 |
锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成a mol硝酸锌时,被还原的硝酸的物质的量为( )
| A.a /4 mol | B.a / 2 mol | C.a mol | D.2a mol |
取x g铜镁合金完全溶于浓硝酸中,若反应过程中HNO3被还原只生成NO、NO2,收集产生的气体,再通入0.56L氧气(标况),气体恰好可以被水吸收,在合金与HNO3反应后的溶液中加入足量的NaOH溶液可以生成3.9g沉淀,则x等于( )
| A.1.2g | B.2.2g | C.3.2g | D.无法计算 |
0.3molSO32-恰好将0.2molXO4-离子还原,则X元素在还原产物中的化合价是( )
| A.+1 | B.+2 | C.+3 | D.+4 |
现有一定量的铁粉和铜粉的混合物,将其平均分成四份,分别加入同浓度不同体积的稀硝酸,充分反应后,在标准状况下生成NO的体积和剩余金属的质量如表所示(假设硝酸的还原产物只有NO一种)。根据上表中的数据计算分析,下列推断正确的是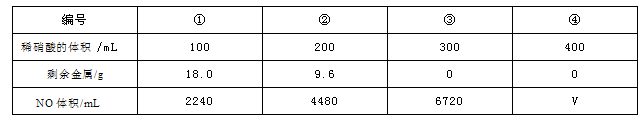
| A.①中溶解了5.6gFe | B.②中溶解了9.6gCu |
| C.硝酸的物质的量浓度为4 mol•L-1 | D.④中V=6720 |
某污水中含CN-a mg·L-1,现用ClO2将CN-氧化,只生成两种无毒气体。处理100 m3这种污水,至少需要ClO2的物质的量为
| A.50a/13 mol | B.50a/26 mol | C.25a/13 mol | D.100a/13 mol |
24mL浓度为0.05mol/L 的Na2SO3溶液恰好与20mL浓度为0.02 mol/L的K2Cr2O7溶液完全反应;已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
| A.+2 | B.+3 | C.+4 | D.+5 |