工业废气NO、NO2是造成大气污染的气体之一,工业上常用原理:NOx + NH3→N2 + H2O,使其转化为无毒的N2,现有NO、NO2的混合3.0 L,可与3.5 L相同状况的NH3恰好完全反应,全部转化为N2,则在原混合气体中NO和NO2的物质的量之比是
| A.1:1 | B.2:1 | C.3:1 | D.1:3 |
在100mL HNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.6mol ,向该溶液中加入足量铜粉,加热、充分反应后,所得溶液中c(Cu2+)的最大值为(反应前后溶液体积变化忽略不计)
,向该溶液中加入足量铜粉,加热、充分反应后,所得溶液中c(Cu2+)的最大值为(反应前后溶液体积变化忽略不计)
A.0.36 mol |
B.0.30 mol |
C.0.225 mol |
D.0.45 mol |
已知在一定条件下,Cl2、ClO2(其还原产物为 Cl―)、O3(l mol O3转化为 l molO2和1molH2O)、H2O2等物质都具有氧化性,因而常被用作消毒剂。等物质的量的上述物质消毒效率最高的是
| A.C12 | B.ClO2 | C.O3 | D.H2O2 |
将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、NO2、N2O4)的混合物共0.8mol,这些气体恰好能被500mL 2.0mol/L NaOH溶液完全吸收,溶液中生成NaNO3和NaNO2,则原混合气体中NO的物质的量为
| A.0.3mol | B.0.4mol | C.0.5mol | D.0.6mol |
在1 L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2 mol•L-1和1.5mol•L-1,现向该溶液中加入39.2 g铁粉使其充分反应。下列有关说法正确的是
| A.反应后溶液中Fe3+物质的量为0.8 mol |
| B.反应后产生13. 44 L H2(标准状况) |
| C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9 mol |
| D.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体 |
在隔绝空气的情况下,9.2 g铁、镁、铝混合物溶解在一定量某浓度的稀硝酸中,当金属完全溶解后收集到4.48 L(标准状况下)NO气体。在反应后的溶液中加入足量的烧碱溶液,可生成氢氧化物沉淀的质量为
| A.18.6 g | B.20 g | C.19.4 g | D.24 g |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA |
| B.22.4L CO2与过量的Na2O2反应,转移的电子数为NA |
| C.物质的量浓度为0.3mol/L的BaCl2溶液中,含有Cl-个数为0.6 NA |
| D.3mol NF3(F元素为-1价)与水完全反应生成HF、HNO3和NO,转移电子数2NA |
氮氧化铝(AlON)是一种高硬度防弹材料,可以在高温下由反应Al2O3+C+N2=2AlON+CO合成,下列有关说法正确的是
| A.氮氧化铝中氮的化合价是-3 |
| B.反应中每生成5.7g AlON 同时生成1.12 L CO |
| C.反应中氧化产物和还原产物的物质的量之比是2:1 |
| D.反应中氮气作氧化剂 |
As2S3和HNO3有如下反应:As2S3 + 10H+ + 10NO3- 2H3AsO4 + 3S + 10NO2↑+ 2H2O,下列说法正确的是
2H3AsO4 + 3S + 10NO2↑+ 2H2O,下列说法正确的是
| A.生成1mol H3AsO4时,转移电子个数为10NA |
| B.将该反应设计成一原电池,则NO2应该在正极附近逸出 |
| C.该反应的氧化产物之一为S |
| D.反应产物NO2与11.2LO2(标准状况)混合后用水吸收全部转化为浓HNO3,然后与过量的碳反应,所产生的CO2的量为0.5mol |
LiAlH4( )、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是
| A.LiH与D2O反应,所得氢气的摩尔质量为4 g/mol |
| B.1 mol LiAlH4在125℃完全分解,转移3 mol电子 |
C.LiAlH4溶于适量水得到无色溶液,则化学方程式可表示为:LiAlH4 + 2H2O LiAlO2 + 4H2↑ LiAlO2 + 4H2↑ |
| D.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂 |
北京市规定食盐中碘含量标准为(18~33)mg/kg。为测定加碘食盐样品的碘含量,某实验小组设计了如下步骤:
Ⅰ.用天平准确称取5.0 g食盐样品,加适量蒸馏水使其完全溶解。
Ⅱ.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全。
Ⅲ.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液3.0 mL,恰好反应完全。
(1)步骤Ⅱ中反应后碘元素以 形式(填物质的化学式)存在。
(2)已知步骤Ⅲ中S2O32-反应后转化为S4O62-,写出步骤Ⅲ的离子方程式 。
(3)上述实验样品中碘含量是 mg/kg。
某离子反应涉及H2O、ClO—、IO3—、OH—、I2、Cl—六种微粒。其中c(ClO—)随反应进行逐渐减小。下列判断错误的是
| A.该反应的还原剂是I2 |
| B.氧化剂与还原剂的物质的量之比为5:2 |
| C.消耗1 mol氧化剂,转移2 mol电子 |
| D.反应后溶液的碱性明显减弱 |
水热法制备Fe3O4纳米颗粒的总反应: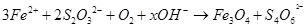
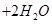 ,有关说法正确的是
,有关说法正确的是
| A.每转移1.5mol电子,有1.125mol Fe2+被氧化 |
| B.x=2 |
| C.Fe2+、S2O32-都是还原剂 |
| D.每生成1mol Fe3O4,转移电子2mol |
在100ml硝酸和硫酸的混合液中,两种酸的物质的量浓度之和是0.6mol/l.向混合液中加入足量的铜粉,加热充分反应,所得溶液中铜离子的物质的量浓度最大值为(忽略反应前后溶液体积变化)
| A.0.30mol/l | B.0.225mol/l | C.0.45mol/l | D.0.36mol/l |