山东省青岛市高三上学期期末考试化学试卷
化学与生活密切相关,下列说法正确的是
| A.含有是食品添加剂的食物对人体健康均有害 |
| B.普通玻璃和氮化硅陶瓷都属于新型无机非金属材料 |
| C.大力推广应用燃料“脱硫、脱硝”技术,可减少硫氧化物和氮氧化物对空气的污染 |
| D.为消除碘缺乏病,政府规定在食盐中必须添加一定量的KI |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B.25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA |
| C.12 g石墨和C60的混合物中质子总数一定为6NA个 |
| D.常温常压下,22.4L乙烯中C—H键数为4NA |
有关“油”的说法正确的是
| A.油脂包括矿物油、植物油与动物油 |
| B.油脂的氢化与油脂的皂化都属于加成反应 |
| C.植物油能使碘酒褪色 |
| D.油脂属于高分子化合物,可以发生水解反应 |
下列叙述中因果关系成立的是
| A.因为NH3的水溶液可以导电,所以NH3是电解质 |
| B.因为SO2可以使溴水褪色,所以SO2具有漂白性 |
| C.因为加热后纯水的pH<7,所以升温可使水呈酸性 |
| D.因为电解质溶于水后发生电离,所以电解质在溶液中的反应实质是离子间的反应 |
物质间常常相互联系、互相影响着,微粒也不例外。下列各组离子可能大量共存的是
| A.不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、C1O-、I- |
| B.能与金属铝反应放出氢气的溶液中:K+、NO3-、C1-、NH4+ |
C.常温下水电离出的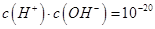 的溶液中:Na+、Cl-、S2-、SO32- 的溶液中:Na+、Cl-、S2-、SO32- |
| D.无色透明溶液:K+、HCO3-、NO3-、SO42-、Fe3+ |
下列有关物质分类或归类正确的一组是
①化合物:CaCl2、NaOH、HCl、HD ②混合物:盐酸、漂白粉、水玻璃、水银
③同素异形体:C60、金刚石、石墨 ④电解质:氯化铵、硫酸钡、冰醋酸
| A.①② | B.①③ | C.②③ | D.③④ |
利用下列实验装置进行的相应实验,不能达到实验目的的是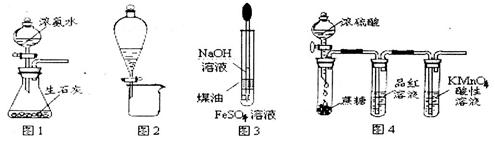
| A.图1所示装置可制取氨气 |
| B.图2所示装置可分离CH3CH2OH和CH3COOC2H5混合液 |
| C.图3所示装置可制备Fe(OH)2并容易观察到白色沉淀 |
| D.图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂自性、还原性 |
水热法制备Fe3O4纳米颗粒的总反应: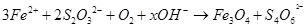
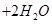 ,有关说法正确的是
,有关说法正确的是
| A.每转移1.5mol电子,有1.125mol Fe2+被氧化 |
| B.x=2 |
| C.Fe2+、S2O32-都是还原剂 |
| D.每生成1mol Fe3O4,转移电子2mol |
下述四个反应中,酸所体现的性质与其他三者明显不同的是
| A.浓盐酸与二氧化锰共热制氯气 |
| B.浓硫酸与铜片加热 |
| C.浓硝酸与铜反应 |
| D.稀硝酸与铜反应 |
下表是元素周期表一部分。X、Y、Z均为短周期元素,X、Z的质子数之和为23,下列说法正确的是
| A.W的原子序数比Z的大9 |
| B.Y的最高价氧化物溶于水,与水反应得到酸 |
| C.W的单质能与Z的一种氧化物的水溶液反应生成两种强酸 |
| D.Z的单质在一定条件下可与铁粉反应,将铁粉氧化为+3价 |
以下关于下图说法正确的是
| A.图表明催化剂可以改变反应的热效应 |
| B.图表示某反应能量的变化与生成物状态无关 |
| C.图表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| D.图表明化学反应不仅遵循质量守恒定律,也遵循能量守恒 |
下列对应化学反应的离子方程式正确的是
A.KIO3与KI在酸性溶液中反应: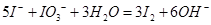 |
B.向碳酸氢铵溶液中加过量氢氧化钠溶液并加热: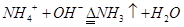 |
C.将过量二氧化硫通入稀氨水中: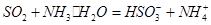 |
D.用稀硝酸洗涤试管内壁的银镜: |
25℃时,纯水中存在电离平衡:H2O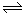 H++OH-△H>0下列叙述正确的是
H++OH-△H>0下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
NO2、NH3和O2组成的混合气体,在一定条件下恰好完全反应,生成N2和H2O,则原混合气体中 NO2、NH3和O2的体积比可能是(不考虑NO2与N2O4之间的转化)
| A.2:4:l | B.2:1:2 | C.1:l:1 | D.1:4:3 |
温度为T 时,向2.0 L恒容密闭容器中充入1.0 mol PC15,
反应: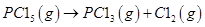 经一段时间后达到平衡。反应过程中测定的部分数据见下表:
经一段时间后达到平衡。反应过程中测定的部分数据见下表:
下列说法正确的是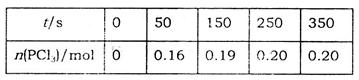
A.反应在前50 S内的平均速率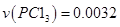 mol/( mol/( ) ) |
B.保持其他条件不变,升高温度,平衡时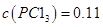 mol·L mol·L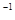 ,该反应为放热反应 ,该反应为放热反应 |
| C.相同温度下,起始时向容器中充入1.0 mol PC15、0.20 mol PC13和0.20 mo1 C12,达到平衡前的v(正)>v(逆) |
| D.相同温度下,起始时向容器中充入2.0 mol PC13、2.0 mol C12,达到平衡时,PCl3的转化率小于80% |
常温下,下列溶液中的微粒浓度关系正确的是
A.氯气通入氢氧化钠溶液中: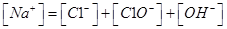 |
B.pH=8.3的NaHCO3溶液: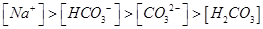 |
C.pH=11的氨水与pH=3的盐酸等体积混合: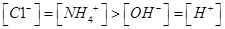 |
D.某溶液中只存在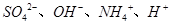 四种离子,则可能存在: 四种离子,则可能存在: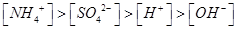 |
(5分)化学实验是化学学科学习、探究的基础。
(1)下列描述错误的是_______.
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、 泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解。
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液肯定存在的离子是:_______________
在②中产生的自色沉淀是:_________________
(14分)已知有A、B、C、D、E五种短周期元素元素,其原子序数依次增大。F是常见的金属,在潮湿的空气中被腐蚀形成红棕色固体。A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正价与最低负价的代数和为6,D是同周期中离子半径最小的元素。
(1)五种元素中,金属性最强的元素在周期表的位置是________写出D元素的原子结构示意图________
(2)B元素的气态氢化物与其最高价氧化物对应的水化物化合,生成物的水溶液呈___性,原因________(离子方程式表示)上述化合物浓溶液滴加到Mg(OH)2悬浊液中,沉淀逐渐消失最后澄清,请解释澄清的原因______________________________________________
(3)含F的二价离子的酸性溶液,在空气中易被氧化变质,该过程的离子反应为:____________________
检验该二价离子没有被完全氧化的方法为:_______________________________
(4).E元素的最高价氧化物对应的水化物与D元素的最高价氧化物对应的水化物反应的化学方程式为____________________________________________________
(17分)二甲醚是一种重要的清洁燃料。合成二甲醚是解决能源危机的研究方向之一。
(1)用CO2和H2可以合成二甲醚(CH3OCH3)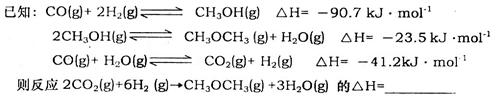
(2)已知在一定温度下,以下三个反应的平衡常数为k1、k2、k3: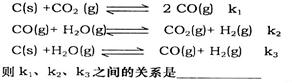
(3)二甲醚(CH3OCH3)燃料电池可以提升能量利用率。利用二甲醚酸性介质燃料电池电解100mL 1mo1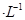 的食盐水(惰性电极),电解一段时间后,收集到标况下的氢气2.24L(设电解后溶液体积不变)
的食盐水(惰性电极),电解一段时间后,收集到标况下的氢气2.24L(设电解后溶液体积不变)
①二甲醚燃料电池的负极反应式为_____________。
②电解后溶液的PH=_________________________
(4)工业合成氨的反应为: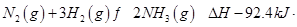 mol-1
mol-1
已知合成氨反应在某温度下2L的密闭绝热容器中进行,测得数据如下表: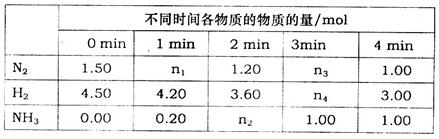
根据表中数据计算:
①0 min~1 min内N2的平均反应速率为_________
②该条件下反应的平衡常数k=________(保留两位小数)
③反应达到平衡后,若往平衡体系中再加入N2、H2、NH3各1mol,化学平衡向_______(填“正向”、“逆向”或“不移动”),该反应的平衡常数k___________(填“变大”“减小”或“不变”)
(5)常温下,将0.2mol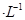 HCOOH和0.1mol
HCOOH和0.1mol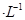 NaOH溶液等体积混合,所得溶液的PH<7,说明HCOOH的电离程度____________HCOONa的水解程度(填“大于”或“小于”)。该溶液中[HCOOH]-[OH-]+[H+]=______mol
NaOH溶液等体积混合,所得溶液的PH<7,说明HCOOH的电离程度____________HCOONa的水解程度(填“大于”或“小于”)。该溶液中[HCOOH]-[OH-]+[H+]=______mol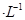
(8分)下面是在实验室中模拟“侯氏制碱法”制取NaHCO3的实验步骤。
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在C中溶解,再通入另一装置中产生的气体,片刻后,C中出现固体。继续向C中通入两种气体,直到不再有固体产生。
第三步:过滤C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl粉末,有NH4C1晶体析出。
(1)下图所示装置的连接顺序是:a接____;____接___;b接_____。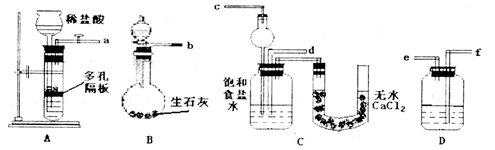
(2)A中常选用的固体反应物为_____;D中应选用的液体为______
(3)第二步中必须先让_______装置先发生反应
(4)C中用球形干燥管而不用直导管,其作用是________
(5)第四步中分离出NH4Cl晶体的操作是_______;其所得的NH4C1晶体中常含有少量的NaCl和NaHCO3(约占5%~8%),请设计一个简单的实验,证明所得固体的成分大部分是NH4C1。简要写出操作和现象:_______。
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)e的基态原子电子排布式为_______。
(2)b、c、d的第一电离能由大到小的顺序是_________(填元素符号)
(3)a和其他元素形成的二元共价化合物中,分子中既含有极性共价键、又含有非极性共价键的化合物是________(填化学式)。
(4)d与c可以形成两种分子,低价态分子中心原子的杂化方式为_______该分子的空间构型为______________
(5)e和c形成的一种离子化合物的晶体结构如图,则该离子化合物的化学式为__________。(填元素符号)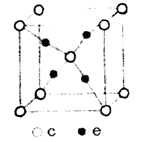
 粤公网安备 44130202000953号
粤公网安备 44130202000953号