下列叙述或表示正确的是( )
| A.0.1mol·L﹣1的醋酸的pH=a,0.01mol·L﹣1的醋酸的pH=b,则a+1=b |
| B.常温下0.1mol·L﹣1的醋酸溶液与等浓度等体积NaOH溶液反应后的溶液中:c(CH3COOH)+c(CH3COO﹣)=0.1mol·L﹣1 |
| C.难溶电解质AB2的饱和溶液中,已知:c(A2+)="x" mol·L﹣1,c(B﹣)="y" mol·L﹣1,则Ksp值为4xy2 |
| D.用200mL4mol·L﹣1的NaOH溶液将0.6mol CO2完全吸收,反应的离子方程式为: 3CO2+4OH﹣=CO32﹣+2HCO3﹣+H2O |
某氨水的pH=X,某盐酸的pH=Y,已知X+Y=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是
| A.c(NH4+)>c(Cl-)>c(OH-)>c(H+) | B.c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D.c(NH4+)>c(H+)>c(Cl-) >c(OH-) |
下列说法正确的是( )
| A.中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠多于醋酸 |
| B.将氢氧化钠和氨水溶液各稀释一倍,两者的OH—浓度均减少为原来的一半 |
| C.如果盐酸的浓度是醋酸浓度的二倍,则盐酸中氢离子浓度也是醋酸氢离子浓度的二倍 |
| D.物质的量相同的磷酸钠溶液和磷酸溶液中所含的磷酸根离子的量不相同 |
常温下,向20 mL某浓度的盐酸中逐滴加入0.1 mol/L的氨水,溶液pH的变化与加入氨水的体积关系如图所示。
下列叙述正确的是
| A.盐酸的物质的量浓度为l mol/L |
| B.在①、②之间的任意一点:c(Cl-)>c(NH4+),c(H+)>c(OH-) |
| C.在点②所示溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+),且V<20 |
| D.在点③所示溶液中:由水电离出的c(OH-)>l0-7mol/L |
关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的( )
| A.c(NH4+):③>① |
| B.水电离出的c(H+):②>① |
| C.①和②等体积混合后的溶液:c(H+)=c(OH )+c(NH3•H2O) |
| D.①和③等体积混合后的溶液:c(NH4+)>c(Cl )>c(OH )>c(H+) |
25℃时,在10mL浓度均为0.1mol/LNaOH和NH3·H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是:
| A.未加盐酸时:c(OH-)>c(Na+)= c(NH3·H2O) |
| B.入10mL盐酸时:c(NH4+) +c(H+) = c(OH-) |
| C.加入盐酸至溶液pH=7时:c(Cl-) = c(Na+) |
| D.加入20mL盐酸时:c(Cl-) =c(NH4+) +c(Na+) |
常温下,下列溶液中的微粒浓度关系正确的是
A.氯气通入氢氧化钠溶液中: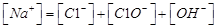 |
B.pH=8.3的NaHCO3溶液: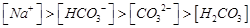 |
C.pH=11的氨水与pH=3的盐酸等体积混合: |
D.某溶液中只存在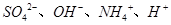 四种离子,则可能存在: 四种离子,则可能存在: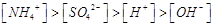 |
设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.在标准状况下,2.24 L苯含有的分子数为0.1NA |
| B.100ml 1mol/L的NH4Cl溶液中,NH4+的数目为0.1NA |
| C.7.8 g Na2S和Na2O2的混合物中所含离子数为0.3NA |
| D.电解精炼铜时,阳极质量每减少32 g,电路中就转移NA个电子 |
今有120 mL, 0.20 mol/L Na2CO3的溶液和某浓度的200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
| A.1.5 mol/L | B.2.0mol/L | C.0.18 mol/L | D.0.24mol/L |
下列溶液中各离子的浓度关系正确的是
| A.0.1 mol·L-1 CH3COONa溶液中:c(CH3COO-)+c(CH3COOH)="0.1" mol·L-1 |
| B.25℃时,等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(C6H5ONa)>pH(NaHCO3)>pH(CH3COONa) |
| C.25℃时,pH=9.4、浓度均为0.1 mol·L-1的HCN与NaCN的混合溶液中:c(Na+)>c(HCN)>c(CN-)>c(OH-) |
| D.将足量AgCl分别放入:①5m水,②10mL0.2mol/LMgC12,③20mL0.3mol/L盐酸中溶解至饱和,c(Ag+):①>②>③ |
由硫酸钾、硫酸铝和硫酸组成的混合溶液,pH=1,c(Al3+)=0.4mol·L﹣1,c(SO42﹣)=0.8mol·L﹣1,则c(K+)=( )
| A.0.15 mol·L﹣1 | B.0.2 mol·L﹣1 |
| C.0.3 mol·L﹣1 | D.0.4 mol·L﹣1 |
常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH随溶液体积变化的曲线如下图所示,则下列叙述正确的是
| A.b、c两点溶液的导电能力相同 |
| B.a、b、c三点溶液中水的电离程度a>c>b |
| C.c点溶液中c (H+) = c (OH-) + c (CH3COOH) |
| D.用等浓度的盐酸分别与等体积的b、c处溶液恰好完全反应,消耗盐酸体积 Vb = Vc |
下列说法中不正确的是
| A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H<O,则该反应能自发进行 |
| B.pH相等的四种溶液:a.CH3COONa b.Na2CO3 c.NaHCO3d.NaOH,则四种溶液中溶质的物质的量浓度由小到大顺序为:d<b<c<a |
| C.pH=2的一元酸和pH=12的二元强碱等体积混合:c(OH-)≤c(H+) |
| D.pH=9的CH3COONa溶液和pH=9的NH3·H2O溶液中水的电离程度相同 |
常温下a mol·L-1稀氨水和b mol·L-1稀盐酸等体积混合,对混合后溶液判断一定正确的是
| A.若a=b,则c(NH4+)=c(Cl-) | B.若a>b,则c(NH4+)>c(Cl-) |
| C.若a>b,则c(OH-)>c(H+) | D.若a<b,则c(OH-)<c(H+) |