下列有关说法正确的是( )
| A.AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 |
| B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| C.将纯水加热至较高温度,KW变大、pH变小、呈酸性 |
| D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 |
25℃时,在10 mL浓度均为0.1mol/L NaOH和NH3·H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是
| A.未加盐酸时:c(OH-)>c(Na+)= c(NH3·H2O) |
| B.加入10 mL盐酸时:c(NH4+) +c(H+) =c(OH-) |
| C.加入盐酸至溶液pH=7时:c(Cl-) = c(Na+) |
| D.加入20 mL盐酸时:c(Cl-) =c(NH4+) +c(Na+) |
人体血液呈弱碱性,pH在7.35~7.45之间,超出范围会引起酸或碱中毒。
下列有关血液说法不合理的是
A.血液中溶解的CO2有平衡存在:CO2 + H2O  H2CO3 H2CO3 H++HCO3- H++HCO3- |
| B.当pH<7.35时造成酸中毒,可静脉滴注NaHCO3溶液解毒 |
| C.病人心肺复苏时大量使用NaHCO3,会造成血液的pH升高,引起碱中毒 |
| D.取一定量pH=8.1的血液稀释到原体积的10倍,pH=7.1 |
将下列物质的溶液在蒸发皿中加热蒸干并灼烧(400 ℃),可以得到该物质的固体的是
| A.AlCl3 | B.NaHCO3 | C.KMnO4 | D.MgSO4 |
室温下,下列溶液中粒子浓度关系正确的是
| A.Na2S溶液:c(Na+) > c(HS-) > c(OH-) > c (H2S) |
| B.Na2C2O4溶液:c (OH-) = c(H+) + c(HC2O4-) + 2c (H2C2O4) |
| C.Na2CO3溶液:c (Na+) + c (H+) = 2c (CO32-)+ c (OH-) |
| D.CH3COONa和CaCl2混合溶液: c (Na+) + c (Ca2+)=c (CH3COO-) +c (CH3COOH) +2c (Cl-) |
已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1 mol·L-1的NaA和NaB混合溶液中,下列排序正确的是
A.c(OH-)>c(HA)>c(HB)>c(H+) B.c(OH-)>c(A-)>c(B-)>c(H+)
C.c(OH-)>c(B-)>c(A-)>c(H+) D.c(OH-)>c(HB)>c(HA)>c(H+)
在蒸发皿中加热蒸干下列物质的水溶液并灼烧(低于400℃),可以得到该物质的固体的是
| A.氯化铝 | B.碳酸氢钠 | C.硫酸镁 | D.高锰酸钾 |
下列溶液中离子浓度关系的表示正确的是
| A.NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) |
| B.pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后的溶液中:c(OH-)>c(H+)+c(CH3COO-) |
| C.0.1 mol·L-1的NH4Cl溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后的溶液中:2c(Na+)=c(CH3COOH)+c(CH3COO-) |
常温下的下列溶液,有关说法正确的是
A.某酸H2A的钠盐NaHA溶液中:c(A2-) < c(H2A),则该溶液的pH>7
B.1.0×10-3 mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0
C.在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7
D.Na2CO3、NaHCO3两种盐溶液中,离子种类不相同
下列依据相关实验得出的结论正确的是
| A.将Al2(SO4)3溶液蒸干、灼烧至恒重,最终剩余固体是Al2O3 |
| B.将某气体通入品红溶液中,品红溶液褪色,则此气体一定是SO2 |
| C.取少许某溶液,滴加数滴KSCN溶液,无明显现象;再另取少许原溶液,先滴少量新制氯水,再滴加数滴KSCN溶液,溶液变血红色,则原溶液中一定含Fe2+ |
| D.在淀粉溶液中加入稀硫酸并加热片刻后,再加入适量银氨溶液,水浴加热后没有银镜生成,说明淀粉没有水解 |
关于氯化铁水解的错误说法是
| A.水解达到平衡(不饱和)时,无论加氯化铁饱和溶液还是加水稀释,平衡均向正方向移动 |
| B.浓度为5mol/L和0.5mol/L的两种FeCl3溶液,其它条件相同时,Fe3+的水解程度前者比后者低 |
| C.有50℃和20℃的相同浓度氯化铁溶液,其他条件相同时,Fe3+的水解程度前者比后者小 |
| D.为抑制Fe3+水解,较好地保存FeCl3溶液,应加少量盐酸 |
常温下,0.2 mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是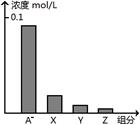
| A.HA为强酸 |
| B.该混合液pH=7 |
| C.图中X表示HA,Y表示OH-,Z表示H+ |
| D.该混合溶液中:c(A-)+c(Y)=c(Na+) |
下列离子反应方程式中,属于水解反应的是
A.NH4++H2O NH3·H2O+H+ NH3·H2O+H+ |
B.NH3·H2O NH4++OH- NH4++OH- |
C.HCO3-+H2O H3O++CO32- H3O++CO32- |
| D.2Na2O2+2H2O===4NaOH+O2↑ |
25℃时,将V1 ml 0.1 mol /L NaOH溶液和V2 ml 0.1 mol /L的CH3COOH溶液充分混合,若混合后溶液呈中性,则该混合溶液中有关粒子的浓度应满足的关系是
A. |
B. |
C. |
D. |