(每空1分,共6分)
写出除去下列物质中的杂质(括号内物质)所用的试剂,并写出发生的离子方程式。
(1)NaOH溶液(Na2CO3) , 。
(2)NaCl溶液(MgCl2) , 。
(3)KCl溶液(CuSO4) , 。
Ⅰ、147 g H2SO4的物质的量是_______,其中含有______mol H,含氧原子数为____个。
Ⅱ、写出下列反应的离子方程式:
⑴硫酸与氢氧化钡溶液反应:
⑵碳酸钙与盐酸反应:
⑶氯化铁溶液加入氢氧化钠溶液中:__________________________________
无机化合物可根据其组成和性质进行分类:

(1)上述所示的物质分类方法名称是 。
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②、③和⑥后面。(每空填写一个化学式即可)
| 物质类别 |
酸 |
碱 |
盐 |
氧化物 |
| 化学式 |
①HCl ② |
③ ④Ba(OH)2 |
⑤Na2CO3 ⑥ |
⑦CO2 ⑧Na2O2 |
(3)二氧化碳与氢氧化钠溶液反应的离子方程式为____________。
(4)过氧化钠可作供氧剂,原因是_______(用化学方程式表示)。
化学用语是化学学科的特色语言,化学用语可以准确表述化学现象、变化以及本质,请按要求完成以下两个问题。
(1)配平酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式:
H2O2+ MnO4-+ = Mn2++ O2↑+
(2)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:____________________、_______________________。
Ⅰ、写出下列物质在水溶液中的电离方程式:
(1)Al2(SO4)3
(2)NaHCO3
Ⅱ、写出下列反应的离子方程式或化学方程式
(1)碳酸钠溶液与盐酸反应
(2)铁片插入到硝酸铜溶液中
(3)向氢氧化钙溶液加入足量碳酸氢钠溶液
(4)Ba2+ + SO42- =BaSO4 ↓
(5)Cu(OH)2 + 2H+=" Cu" 2+ + 2H2O
现有四瓶贴有A、B、C、D标签的溶液,它们可能是K2CO3、Ba(NO3)2、NaHSO4和K2SO4溶液。现进行如下实验,并记录部分现象(如下图)。
判断A是 (写化学式,下同),B是 ,C是 ,D是 。
B和D反应的离子方程式是
A和B反应的离子方程式 。
某无色溶液的溶质只由以下离子中的若干离子构成:Na+、Ag+、Ba2+、Al3+、AlO2﹣、CO32﹣、SO42﹣.将该溶液进行如下实验,根据所给实验现象判断原溶液中离子的存在情况,填写空格.
(1)取适量该溶液,加入过量盐酸,有气体生成,最终得到无色透明溶液.肯定存在的离子 ;肯定不存在的离子 .
(2)在(1)所得到的溶液中再加入过量NH4HCO3溶液,有无色无味的气体生成,同时析出白色沉淀.原溶液中肯定存在的离子 ,写出生成沉淀的离子方程式 .
(3)在(2)所得溶液中加入过量Ba(OH)2溶液,加热,有刺激性气味的气体生成,同时析出白色沉淀.沉淀中一定含有
(4)原溶液中溶质的成分为 (填写化学式)
写出碳酸钙与盐酸反应的离子方程式_____________________。
现有下列物质:①碳酸钠 ②氧化钠 ③二氧化硅 ④铁 ⑤氧气 ⑥氢氧化钙 ⑦硫酸 请将上述物质按下列要求分类,并将其序号填入空白处:
(1)按组成分类,属于单质的是 ,属于氧化物的是 ,属于酸的是 ,属于碱的是 ,属于盐的是 。
(2)写出①分别与⑥、⑦在溶液中反应的离子方程式:___________________、___________________
在Fe、Fe3+、Fe2+几种微粒中,只有氧化性的是 ,只有还原性的是 ,既有氧化性又有还原性的是 。向黄色的FeCl3溶液中加入 铁粉,溶液颜色变为浅绿色,写出该反应的离子方程式
I.按要求写出对应反应的离子方程式:
(1)硫酸镁溶液与氢氧化钡溶液反应 ;
(2)用氢氧化钠溶液出去CO中少量的 CO2气 ;
(3)用稀硫酸除去铁钉上的铁锈(主要成分是Fe2O3) ;
II.以下8种为中学化学中常见的物质:
①CaO ②H2O ③胆矾 ④CaCO3 ⑤H2SO4 ⑥氨水 ⑦酒精 ⑧Cu
请按下列分类标准回答问题:
(1)属于电解质的是 (2)属于盐的是
(3)属于氧化物的是 (4)属于非电解质的是
过氧化氢是用途很广的绿色氧化剂,它的水溶液俗称双氧水,常用于消毒、杀菌、漂白等。试回答下列问题:
(1)写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式:____________。
(2)Na2O2,K2O2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。则上述最适合的过氧化物是________。
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上,实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛溶液依次加入到质量分数为30%-70%的过氧化氢溶液中,则该反应的化学方程式为________,过氧化氢比理论用量稍多,其目的是________。反应温度最好控制在30 -70℃,温度不易过高,其主要原因是________。
(4)下图是硼氢化钠一过氧化氢燃料电池示意图。该电池工作时,正极附近溶液的pH________(填“增大”、“减小”或“不变”)。
(5)Na2CO3·xH2O2可消毒、漂白。现称取100 g的Na2CO3·xH2O2晶体加热,实验结果如图所示,则该晶体的组成为________。
某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如图(沉淀2为蓝色)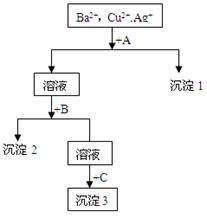
(1)沉淀的化学式:沉淀1 ,沉淀3 ;
(2)写出混合液+A的离子方程式:
溶液+B的离子方程式:
现有下列十种物质:①液态HCl ②NaHCO3 ③NaCl溶液 ④CO2 ⑤蔗糖晶体 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧NH3·H2O ⑨空气 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH- H2O,该反应的化学方程式为 。
H2O,该反应的化学方程式为 。
(2)⑩在水中的电离方程式为 ,
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式: ;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:
(4)写出下列反应的离子方程式
向Ba(OH)2溶液中逐滴加入稀硫酸 。
向Ba(OH)2溶液中通入过量的CO2 。
工业上利用电解污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如下:
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
| |
Fe3+ |
Cu2+ |
Cr3+ |
| 开始沉淀pH |
2.1 |
4.7 |
4.3 |
| 完全沉淀pH |
3.2 |
6.7 |
a |

(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有 。
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:①加入石灰乳调节pH范围为: ~ ;②将浊液加热到80℃, 。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体的离子反应方程式 ,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是 。