现有下列十种物质:①液态HCl ②NaHCO3 ③NaCl溶液 ④CO2 ⑤蔗糖晶体 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧NH3·H2O ⑨空气 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH- H2O,该反应的化学方程式为 。
H2O,该反应的化学方程式为 。
(2)⑩在水中的电离方程式为 ,
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式: ;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:
(4)写出下列反应的离子方程式
向Ba(OH)2溶液中逐滴加入稀硫酸 。
向Ba(OH)2溶液中通入过量的CO2 。
工业上利用电解污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如下:
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
| |
Fe3+ |
Cu2+ |
Cr3+ |
| 开始沉淀pH |
2.1 |
4.7 |
4.3 |
| 完全沉淀pH |
3.2 |
6.7 |
a |

(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有 。
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:①加入石灰乳调节pH范围为: ~ ;②将浊液加热到80℃, 。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体的离子反应方程式 ,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是 。
(方程式每空2分,其余每空1分,共20分。)氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O =" 2NaOH" + H2↑ ②2Na2O2 + 2H2O =" 4NaOH" + O2↑
③Na2O+ H2O =2NaOH ④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O 2H2↑+ O2↑ ⑥2F2 + 2H2O =" 4HF" + O2
2H2↑+ O2↑ ⑥2F2 + 2H2O =" 4HF" + O2
(1)其中不属于氧化还原反应的是 (填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是 (填编号)
水只作还原剂的反应是 (填编号)
水既作氧化剂,又作还原剂是 (填编号)
水既不作氧化剂,又不作还原剂是 (填编号)
(3)根据你的理解,氧化还原反应的实质是( )
| A.分子中的原子重新组合 | B.氧元素的得失 |
| C.电子的得失或共用电子对的偏移 | D.化合价的改变 |
(4)请你运用所学知识分析3NO2+H2O = 2HNO3+NO是否属于氧化还原反应? (填“是”或“不是”),若是,这个反应的氧化剂和还原剂的质量比是 。
(Ⅱ)写出下列反应的离子方程式:
①铜片与稀硝酸的反应:
②过量二氧化碳通入澄清石灰水:
③往氯化铝溶液中加入过量的NaOH溶液:
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:
②制漂白液的反应:
③雕刻花玻璃的反应:
某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是________。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是________ ,有关的离子方程式为________________________________。
(3)取(2)中的滤液,加入过量的稀氨水(NH3·H2O),出现白色沉淀,说明原溶液中肯定有________,有关的离子方程式为____________________________。
(4)原溶液可能大量存在的阴离子是下列的________。
| A.Cl- | B.NO3- | C.CO32- | D.OH- |
2012年4月15日,央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊进入患者腹中。明胶是水溶性蛋白质混合物,溶于水形成胶体。由工业明胶制成的胶囊往往含有超标的重金属Cr,从而对人体造成伤害。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是 价。CrO2-是一种酸根离子,则Fe(CrO2)2属于__________(填“酸”、“碱”、“盐”或“氧化物”)。
明胶的水溶液和K2SO4溶液共同具备的性质是 。
a.都不稳定,密封放置沉淀
b.两者均有丁达尔现象
c.分散质微粒可通过滤纸
(2)已知CN-离子、SCN-离子和Cl-离子有相似之处,氰分子(CN)2和硫氰分子(SCN)2的性质与Cl2也有相似之处,且常温常压均为气体,完成下列反应方程式:
①MnO2和HSCN的浓溶液共热的化学方式:
②(CN)2和NaOH溶液反应的离子方程式:
(3)已知H2O2是二元弱酸、请写出H2O2与Ca(OH)2溶液反应生成酸式盐的化学式
现有下列十种物质:①液态HCl ②NaHCO3 ③NaCl溶液 ④CO2 ⑤蔗糖晶体 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧NH3·H2O ⑨空气 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH- H2O,该反应的化学方程式为 。
H2O,该反应的化学方程式为 。
(2)⑩在水中的电离方程式为 ,
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式: ;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:
(4)向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
①写出反应的离子方程式 。
用离子方程式解释下列过程:
(1)纯碱溶液显碱性:____________________。
(2)泡沫灭火器的反应原理(硫酸铝溶液与小苏打):_______________________。
(3) AgCl的浊液中加入KI溶液,白色沉淀变为黄色:____________________。
(12分)食盐是重要调味品,随着对饮食健康的重视,出现了各种类型的特种食盐。
(1)常说“饮食过咸会伤骨”,长期摄入食盐过多可能导致骨骼脱钙,下列物质中,可以作为补钙药品主要成分的是 (填标号)。
| A.CaCO3 | B.CaO | C.Ca(OH)2 | D.Ca |
(2)低钠盐因含有氯化钾和硫酸镁可防治高血压和心血管病,往其溶液中滴入氨水,发生反应的化学方程式是 。
(3)加硒盐中含有的硒元素是人体微量元素中的“抗癌之王”,写出证明硒元素非金属性比硫元素弱的一个实验事实: 。
(4)加碘盐可防治碘缺乏症,其中的碘酸钾(KIO3)在酸性溶液中可氧化亚硫酸钠,生成物能使淀粉变蓝,1mol KIO3被还原时,转移电子 mol,该反应的离子方程式为 。
某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子中的一种或几种.当向该溶液中加入一定物质的量的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如图所示.
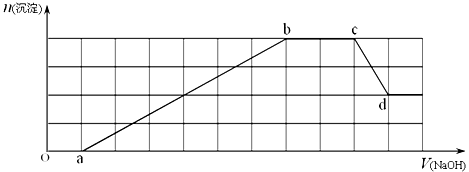
(1)原溶液中一定含有____________,一定不含有____________;
(2)cd段发生的离子反应为___ _________;
(3)原溶液中物质的量浓度最大的阳离子与原溶液中的阴离子的物质的量之比为__________________.
有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W X+H2O+CO2↑
X+H2O+CO2↑
②Z+CO2―→X+O2
③Z+H2O―→Y+O2↑
④X+Ca(OH)2―→Y+CaCO3↓
回答下列问题:
(1)W、Y、Z的化学式分别是:W:________、Y:________、Z:________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是________(写化学式)
(3)若④反应在溶液中进行,写出其离子方程式
某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀CuI。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
已知:I2+2S2O32-=S4O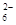 +2I-
+2I-
①可选用_____作滴定指示剂,滴定终点的现象是_______________________________ 。
②CuCl2溶液与KI反应的离子方程式为_______________________________________。
③该试样中CuCl2·2H2O的质量百分数为________。
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,用ClO2替代Cl2对自来水进行消毒是城市饮用水处理新技术。工业上制备ClO2的方法很多,可以用合适的还原剂还原NaClO3制得。
(1)在硫酸酸化的条件下用 草酸还原NaClO3制ClO2,其反应的化学方程式为 。
(2)工业以CH3OH与NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体,已知该反应分为两步进行,第一步为2ClO3-+2Cl-+4H+=2ClO2↑+Cl2↑+2H2O。
①写出第二步反应的离子方程式 。
②工业生产时需在反应物中加少量Cl-,其作用是 。
(3)ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐,写出ClO2与NaOH溶液反应的离子方程式 。
(4)ClO2可用于含CN-废水的处理,产生的两种气体可以直接排入空气。
①已知CN-中C、N的最外层都满足8电子结构,写出CN-的电子式 。
②写出该反应的离子方程式 。
写出下列反应的离子方程式:
(1)Zn粉与稀硫酸溶液的反应:
(2)碳酸钙与稀盐酸溶液的反应:
(3)氢氧化钡溶液与硫酸铜溶液的反应:
除去括号内的杂质,写出除杂的试剂,并写出溶液中反应的离子方程式。
(1)FeSO4(CuSO4)试剂 ,离子方程式__________________。
(2)CO2 (HCl) 试剂 ,离子方程式____________________。
(3)Cu(CuO)试剂 ,离子方程式_______________________。