写出下列反应的离子方程式:
(1)Zn粉与稀硫酸溶液的反应:
(2)碳酸钙与稀盐酸溶液的反应:
(3)氢氧化钡溶液与硫酸铜溶液的反应:
除去括号内的杂质,写出除杂的试剂,并写出溶液中反应的离子方程式。
(1)FeSO4(CuSO4)试剂 ,离子方程式__________________。
(2)CO2 (HCl) 试剂 ,离子方程式____________________。
(3)Cu(CuO)试剂 ,离子方程式_______________________。
工业上为了处理有Cr2O72—的酸性废水,采用下面的处理方法:往工业废水里加入适量的NaCl,以Fe为电极进行电解,经过一段时间后,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中Cr3+的浓度若低于10—5mol/L可符合排放标准。回答下列问题:
(1)电解时阳极上发生的电极反应式: ;
(2)写出Cr2O72—变为Cr3+的离子方程式 ;
(3)工业废水由酸性变为碱性的原因是 ;
(4)已知室温下Cr(OH)3的KSP=1×10—32,则该温度下符合排放标准的溶液的最低pH为 。
写出下列反应的离子方程式:
(1)碳酸钠溶液跟盐酸反应: ;
(2)氢氧化钠溶液与稀硫酸反应: ;
(3)硫酸铜溶液滴入氢氧化钠溶液中: ;
(4)铁加入稀硫酸中: ;
(5)氢氧化钡溶液与硫酸溶液混合: 。
(10分)有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 |
K+ Na+ Cu2+ Al3+ |
| 阴离子 |
SO42- HCO3- NO3- OH- |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴人到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钻玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空
(1)写出B、D的化学式:B ,D 。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为 。
(3)在A溶液中加少入量澄清石灰水,其离子方程式为 。
(4)C常用作净水剂,用离子方程式表示其净水原理 。
(8分)向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
(1)写出反应的离子方程式__________________________________________________
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号).
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用右图中的曲线表示是________(填序号).


(4)若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应.则反应的离子方程式是 _________________________________.
将1mol/L的FeCl3溶液逐滴滴入沸水中,液体变为 色,得到的是 ;反应的化学方为 。向其中逐滴加入稀硫酸至过量,现象是 ,原因是 。
有NaHSO4、Ba(OH)2、NaHCO3三种溶液,已知其中两种溶液的物质的量浓度相同,且分别为另一种溶液的物质的量浓度的2倍;若先将 NaHSO4和NaHCO3溶液各100mL混合反应后,再加入Ba(OH)2溶液100mL,充分反应后,将生成的白色沉淀滤出,得300mL滤液,测得滤液中只含NaOH溶质,其物质的量的浓度为 0.9 mol·L-1(不考虑混合时引起的溶液体积的变化),试回答下列问题:
(1)写出Ba(OH)2溶液与过量NaHCO3溶液反应的离子方程式: ;
(2)写出NaHSO4溶液和NaHCO3溶液反应的离子方程式: ;
(3)通过分析,判断原Ba(OH)2、NaHSO4、NaHCO3三种溶液中哪两种溶液的物质的量浓度不可能相同?(填化学式)。
(4)题中NaHCO3溶液的浓度可能为 。
完成下列反应的离子方程式:
(1)将AlCl3溶液蒸干得到白色固体: ;
(2)用惰性电极电解饱和食盐水: ;
(3)用KOH做电解质溶液的甲烷燃料电池的负极反应式: ;
(4)往AgCl悬浊液中滴加Na2S溶液: ;
元素周期表中第三周期元素的单质及其化合物的用途广泛。
(1)该周期元素中,半径最小的简单离子的离子结构示意图为 。
(2)能证明氯的非金属性(得电子能力)比硫强的化学方程式为 。
(3)NaHSO3溶液呈酸性,其溶液中离子浓度由大到小的顺序为 。
(4)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl—,该反应的离子方程式为 。
(5)已知下列两反应过程中能量变化如图所示:
汽车尾气中含有的少量NO2和SO2在一定条件下会发生反应,该反应的热化学方程式为____________。
现有含NaCl、Na2SO4、Na2CO3和NaHCO3的固体混合物。某同学为测定其中各组分的含量,取部分样品溶于水,并设计了如下实验流程(所加试剂均为过量,反应①~③均为复分解反应)。
请回答: (1)气体W的化学式是 。
(1)气体W的化学式是 。
(2)反应①的离子方程式是  。
。
(3)试剂X、Y、Z依次是 。
(4)下列说法正确的是 (填字母) 。
。
a.溶液A的焰色反应为黄色
b.反应②和③之后均需进行过滤操作
c.若测得气体W的体积(标准状况)、白色沉淀Ⅰ和Ⅱ的质量,可计算出各组分的量
某溶液中含有Ba2+,Cu2+, Ag+,现用NaOH溶液、盐酸和Na2CO3溶液将这三种离子逐一沉淀分离。其流程图如所示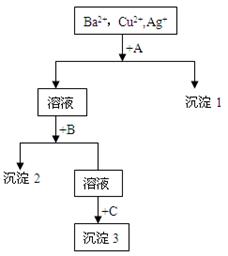
(1)沉淀的化学式(写出最佳答案):
沉淀1 ,沉淀3 ;
(2)写出溶液+B的离子方程式: 。
K2Cr2O7是一种橙红色具有强氧化性的化合物,当它在酸性条件下被还原成正三价铬时,颜色变为绿色。据此,当交警发现汽车行驶不正常时,就可上前阻拦,并让司机对填充了吸附有K2Cr2O7的硅胶颗粒的检验装置吹气。若发现硅胶变色达到一定程度,即可证明司机是酒后驾车。这时酒精被氧化为醋酸其反应原理如下:
2K2Cr2O7+3CH3CH2OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O
请结合上面的描述回答下列问题:
(1)将上述反应改写为离子方程式: 。
(2)如果司机属于醉酒驾车,则检验装置中的硅胶将由 色变为 色。
(3)上述反应中氧化剂是 ,还原剂是 ,氧化产物是 ,还原产物是 。(本题中的四个空都需填写物质的化学式)
(4)在上述反应中当有69g酒精发生反应时消耗K2Cr2O7的物质的量是
已知0.1 mol/L的NaHSO4溶液中H+的物质的量浓度为0.1mo1/L,请下列问题:
(1)写出NaHSO4在水溶液中电离的方程式 。
(2)NaHSO4属于(填“酸”“碱”或“盐”) 。
(3)若将NaHSO4与Ba(OH)2在溶液中按物质的量之比为2:1混合,则反应的离子方程式是 。
(4)若将NaHSO4溶液逐滴滴入Fe(OH)3胶体溶液可观察到的现象是 。
(11分) 铁是人类较早使用的金属之一。运用铁及其化合物的有关知识,同答下列问题:
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是________。(填序号)
A.纯铁硬度比生铁高
B.纯铁耐腐蚀性强,不易生锈
C.不锈钢是铁合金,只含金属元素
D.铁在一定条件下,可与水蒸气反应
E.铁在冷的浓硫酸中钝化
(2)向沸水中逐滴滴加1mol L-1FeCl3溶液,至液体呈透明的红褐色,该反应的离子方程式为 ,所形成该分散系的微粒粒度范围是 。
L-1FeCl3溶液,至液体呈透明的红褐色,该反应的离子方程式为 ,所形成该分散系的微粒粒度范围是 。
(3)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路极。请写出FeCl3溶液与铜反应的离子方程式 。欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液,现有下列试剂:①氯气②铁粉③浓硝酸④浓盐酸⑤烧碱⑥浓氨水,需要用到的一组试剂是_____________。
A.①②④ B.①③④⑥ C.②④⑤ D.①④⑥
(4)高铁酸钠(Na2FeO4)是一种新型净水剂。
①高铁酸钠主要通过如下反应制取:2Fe(OH)3+3X+4NaOH=2Na2FeO4+3NaCl+5H2O,则X的化学式为 。
②高铁酸钠在水中可以发生如下反应:4FeO4 +10H2O==4Fe(OH)3+8OH
+10H2O==4Fe(OH)3+8OH +3O2↑。由此看来,高铁酸钠能够杀菌消毒是因为它具有___________性,而能够除去水中悬浮物是因为 。
+3O2↑。由此看来,高铁酸钠能够杀菌消毒是因为它具有___________性,而能够除去水中悬浮物是因为 。
③下列物质能用作净水剂的有___________。
a.KAl(SO4)2 l2H2O
l2H2O
b.聚合硫酸铁
c.ClO2
d.“84”消毒液