(1)写出下列物质在水溶液中的电离方程式
NaHCO3________________________Fe2(SO4)3___________________________
(2)写出下列反应的离子方程式
稀硫酸与氢氧化钡溶液混合_______________________
碳酸钙与稀盐酸混合_______________________
氧化铜与稀硫酸混合_______________________
写出下列反应的离子方程式:
(1)钠投入到水中反应的离子方程式为:__ ____
(2)服用胃舒平[主要成分是Al(OH)3]治疗胃溃疡,反应的离子方程式为:
(3)铁片插入硫酸铜溶液中: __________________________________。
(4)CH3COOH与NaOH溶液的中和反应:
(5)Ba(OH)2与CuSO4溶液反应:
XeO3是一种不稳定的物质,具有强氧化性。在某一反应体系中有反应物和生成物的微粒共6种,即Mn2+、MnO4—、Xe、XeO3、H+、H2O
发生氧化反应的微粒是_______________。
反应现象为:①有气泡产生,②_____________________________________________。
该反应的离子方程式为:___________________________________________________。
完成下列反应的离子方程式:
(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液,使原溶液中的SO42—恰好完全沉淀:
(2)向明矾溶液中逐滴加入Ba(OH) 溶液,当Al3+恰好全部沉淀时:
溶液,当Al3+恰好全部沉淀时:
(3)向Ca(HCO3) 2溶液中加入过量的NaOH溶液:
某混合物的水溶液,可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH、Cl-、CO、SO,现分别取100 mL的两等份溶液进行如下实验:
①第一份加过量NaOH溶液后加热,收集到0.02 mol气体,无沉淀生成,同时得到溶液甲。
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、干燥、灼烧后,得到1.02 g固体。
③第二份加足量BaCl2溶液后,生成白色沉淀,沉淀经足量盐酸洗涤、干燥后,得到11.65 g固体。
依据实验回答下列问题:
(1)由①可知一定存在的离子为 ,其浓度为 mol·L-1。
(2)写出②中产生沉淀的离子方程式 。
(3)由③可知一定存在的离子为 ,其浓度为 mol·L-1。
(4)综合上面三个实验,该混合物的水溶液中一定不存在的离子是 (填离子符号)。
(5)某同学通过分析认为该溶液中一定存在K+,他的理由是 。
某铝合金中含有铁、铝、镁、铜、硅。为了测定该合金中铝的含量,现设计了如下实验:
已知:Si+2NaOH+H2O=Na2 Si O3+2H2↑,H2Si O3是不溶于水的弱酸。
(1)固体A的成分是:____________,溶液M中的阴离子有:____________________
(2)步骤③中生成沉淀的离子方程式为:_____________________________________
(3)步骤④中,用到的仪器有三脚架、酒精灯以及
(4)在空气中将NaOH溶液滴入FeCl2溶液中,观察到的现象是 ,反应的化学方程式是 ,
(5)该样品中铝的质量分数是:_______________________________(用a、b表示)。
(6)下列因操作不当,会使测定结果偏大的是___________
| A.第①步中加入NaOH溶液不足 | B.第②步中加入盐酸不足时 |
| C.第④步中的沉淀未用蒸馏水洗涤 | D.第④步对沉淀灼烧不充分 |
写出下列反应的离子方程式
(1)含少量NaHCO3的溶液与含过量Ba(OH)2的溶液混合: ;
(2)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式 ;
(3)硫酸铜溶液和氢氧化钡溶液混合
(4)用醋酸除去水壶中的水垢
(本题3个空,每空2分,共6分)
在盛有100mL浓硝酸的试管中加入32g铜片发生反应。请回答:
(1)开始阶段,反应的离子方程式是 。
(2)若二者恰好完全反应,共产生气体11.2L(标准状况)。则浓硝酸的物质的量浓度为 。
(3)反应结束后的试管中,再加入金属铜和入少量20%的稀硫酸,这时溶液中又有气泡产生,请写出反应的离子方程式是 。
某厂废水中含5.00×10−3mol·L−1的Cr2O72-,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Fe的化合价依次为+3、+2),设计了如下实验流程:
(1)第①步反应的离子方程式是
(2)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有
(3)欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4。理论上需要加入 g FeSO4·7H2O。
(1)已知亚氯酸(HClO2)不稳定,可分解,分解反应的离子方程式为:HClO2→ClO2↑+H++Cl﹣+H2O(未配平).当有3.2mol电子发生转移时,发生分解的HClO2的物质的量是 mol.
(2)有Fe2+、NO3﹣、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中氧化剂与还原剂的物质的量之比为 .
(1)通常用小苏打的悬浊液除去CO2中的HCl,反应的离子方程式为: ,
不能用NaOH溶液的原因是 ,也不能用Na2CO3的原因是 (均用离子方程式表示原因)
(2).把下列离子方程式改写成化学方程式:
CO32- + 2H+ = CO2↑ + H2O
Ag+ + Cl-= AgCl↓
向200 mL 某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应后,得到Na2CO3和NaHCO3的混合溶液。向上述所得溶液中,逐滴滴加2 mol·L-1的盐酸,所得气体的体积与所加盐酸的体积关系如图所示: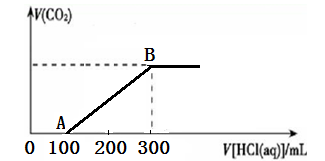
(1)OA段、AB段发生反应的离子方程式__________________、__________________。
(2)B点时,反应所得溶液中溶质的物质的量浓度是______________。