按要求完成下列各题。
(1)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为: 。
(2)ClO2常用子水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式: 。
(3)MnO2可与KOH和KClO3在高温条件下反应,生成K2MnO4,反应的化学方程式为: 。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为 。
(4)(CN)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为 。
(1)下列物质属于电解质的是 ,非电解质的是 ,能导电的物质是_____
①水银 ②液态氯化氢 ③氯气 ④熔融氯化钠 ⑤胆矾 ⑥干冰 ⑦大理石 ⑧盐酸 ⑨蔗糖 ⑩澄清石灰水
(2)写出下列反应的离子方程式:
①实验室制取CO2: ;
②硫酸铜溶液和氢氧化钡溶液: ;
③氢氧化钙溶液与少量碳酸氢钠混合: 。
下图是一些中学常见的物质之间的转化关系(其中部分反应产物省略),其中A和B常温下都是气体,且水溶液都有漂白性;I是一种金属单质;F、M、N均为难溶于水的白色沉淀,其中M和N不溶于稀硝酸;C和D是两种常见的强酸。请回答下列问题:
(1)写①的化学方程式______________________________________
(2)写反应②的离子方程式__________________________________
(3)写出将A通入石灰乳的化学方程式________________________
(4)在①②③④⑤⑥中,属于氧化还原反应的有:_______________(填编号)
已知以下两个氧化还原反应的化学方程式:
①Cl2+H2O===HCl+HClO ②2Al+Fe2O3 Al2O3+2Fe
Al2O3+2Fe
(1)用单线桥法表示反应②中的电子转移情况:______。
(2)若反应②中每生成1 mol Fe,转移电子的物质的量是:________。
(3)将反应①改写成离子方程式:________。
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样
品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
回答下列问题:
(1)试剂Ⅰ的化学式为 ,①中发生反应的离子方程式为 , ;
(2)试剂Ⅱ的化学式为 ,②中加入试剂Ⅱ的目的是 ;
(3)试剂Ⅲ的名称是 ,③中发生反应的离子方程式为 ;
(4)某同学称取提纯的产品0.8000g,溶解后定容在100 mL容量瓶中,每次取25.00 mL溶液,用0.1000 mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62 mL,该产品的纯度为 。
(1)写出下列化学反应的离子方程式
①氢氧化钡溶液和硫酸溶液反应
②碳酸钙和足量稀盐酸反应
(2)根据下列离子方程式,各写一个符合条件的化学方程式
①Zn+2H+==Zn2++H2↑
②HCO3-+ H+==CO2↑+ H2O
某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀CuI。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
已知:I2+2S2O32-=S4O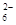 +2I-
+2I-
①可选用_____作滴定指示剂,滴定终点的现象是_______________________________ 。
②CuCl2溶液与KI反应的离子方程式为_______________________________________。
③该试样中CuCl2·2H2O的质量百分数为________。
现有如下九种物质:①H2 ②铝 ③CuO ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3 ⑩NaHSO4
(1)按物质的分类方法,将上述物质的序号填入表格的空白处:
| 分类标准 |
能导电 |
电解质 |
非电解质 |
| 属于该类的物质 |
|
|
|
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH-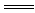 H2O,该离子反应对应的化学方程式为 。
H2O,该离子反应对应的化学方程式为 。
(3)⑨的电离方程式为 。将34.2g ⑨冷却后溶于水配成250mL溶液,SO42-的物质的量浓度为 。
(4)②与⑧发生反应的化学方程式为:Al + 4HNO3(稀)= Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是 (填化学式),还原剂与氧化剂的物质的量之比是 ,当有5.4g Al发生反应时,转移电子的物质的量为 。
利用化合价推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2的性质________________(填序号,下同)
A.只有氧化性 B.只有还原性 C.既有还原性又有氧化性
②SO2通入酸性KMnO4溶液中,溶液由紫色褪至无色。反应后,锰元素被还原成Mn2+,写出上述反应的离子方程式_________________________________
(2)Fe(OH)2很不稳定,露置在空气中容易被氧化,发生反应的离子方程式为__________________________________________________为了获得白色的Fe(OH)2沉淀,可以用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配置的NaOH溶液反应制备。
①用硫酸亚铁晶体配置上述硫酸亚铁溶液时,还需加入_________来防止Fe2+被氧化
②除去蒸馏水中溶解的O2常采用_______的方法
(3)检验Fe3+的方法:_______________________(写出加入试剂的化学式和现象与结论)
按要求写下列化学方程式(1)、(4)或离子方程式(2)(3)
(1)实验室用Ca(OH)2和NH4Cl制取氨气_______________________________
(2)过氧化钠粉末投入水中_____________________________________________
(3)向氯化铝溶液中加入足量氨水_______________________________________
(4)漂白粉在空气中变质_______________________________________________
化学与生产、生活密切相关。从化学视角回答下列问题:
(1)节日焰火利用的是 反应,城市射灯在夜空形成五颜六色的光柱,属于____效应,工业上制造光导纤维的基本原料是 。
(2)pH< 的雨水称为酸雨,我国形成酸雨的主要污染物是 。
(3)化工厂曾用浓氨水来检验氯气管道是否漏气,反应原理为(在有水蒸气存在时):2NH3+3Cl2==6HCl+N2。如果氯气管道某处漏气,用该方法检查时的现象是___________。
(4)碳酸氢铵俗称碳铵,是一种廉价氮肥,它的最大缺点是 。如果向碳酸氢铵溶液中滴加NaOH溶液至过量,反应的离子方程式是_____________________。
某工厂的工业废水中含有大量的FeSO4,较多的Cu2+和少量Na+。该工厂计划从废水中回收FeSO4和金属铜。根据下列流程图,回答问题。
(1)a操作需要用到的玻璃仪器有 。
(2)加入的试剂①为 ,要判断所加试剂①是否过量,其操作方法是 。
(3)加入试剂②发生反应的离子方程式是 。
(4)c操作为 、冷却结晶、 、洗涤、干燥。
无机化合物可根据其组成和性质进行分类:
(1)下图所示的物质分类方法名称是 ;
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面;(只需填一种)
| 物质类别 |
酸 |
碱 |
盐 |
氧化物 |
| 化学式 |
①HCl ② |
③ ④Ba(OH)2 |
⑤Na2CO3 ⑥ |
⑦CO2 ⑧Na2O2 |
(3)写出⑦转化为⑤的离子方程式 ;
NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知 NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中失电子的物质是________,被还原的元素是_________,还原产物与氧化产物的物质的量之比为____________。
(2)已知 NaNO2、NaI 都为可以溶于水的盐,HI为强酸,请将上述反应改写成离子方程式:
________________________________________________________________。
(3)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、 ⑤食醋,你认为必须选用的物质有_____________(填序号)。
(4)某厂废液中,含有 2%~5%的 NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________。
| A.NaCl | B.NH4Cl | C.HNO3 | D.浓H2SO4 |
有以下物质:①Mg ②Al ③C ④稀硫酸 ⑤浓硫酸 ⑥NaOH溶液
(1)写出①与④反应的离子方程式 。
(2)既能跟④又能跟⑥反应的是 (填序号),写出它与⑥反应的化学方程式 。
(3)写出写出③与⑤反应的化学方程式 ,下列关于该反应中⑤体现的性质说法正确的是 。
a.既体现氧化性又体现酸性
b.只体现氧化性
c.只体现酸性
d.体现吸水性