辽宁省五校协作体高一上学期期中化学试卷
下列行为中符合安全要求的是
| A.在汽车加油站见到的油罐车上贴有如图的标志 |
| B.节日期间,在开阔的广场燃放烟花爆竹 |
| C.用点燃的火柴在液化气钢瓶口检验是否漏气 |
| D.进入煤矿井时,用火把照明 |
关于氧化还原反应,下列说法正确的是
①氧化剂发生氧化反应;②氧化剂具有氧化性;③氧化反应的本质是化合价升降;
④物质所含元素化合价变化是判断氧化还原反应的依据;
⑤氧化还原反应的任一反应物不是氧化剂就是还原剂
| A.②④ | B.②③④ | C.①②④ | D.①②④⑤ |
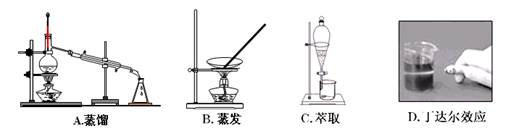
丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,密度小于1 g/mL,沸点约55 oC,分离水和丙酮时最合理的方法是
| A.蒸发 | B.分液 | C.过滤 | D.蒸馏 |
在酸性溶液中能大量共存,并且溶液为无色透明的是
| A.K+、Ca2+、HCO3-、Cl- |
| B.Cu2+、Na+、NO3-、Cl- |
| C.Na+、K+、Mg2+、SO42- |
| D.Mg2+、Fe3+、Cl-、OH- |
下列离子方程式书写正确的是
A.铁与稀盐酸反应:2Fe + 6H+  2Fe3+ + 3H2↑ 2Fe3+ + 3H2↑ |
B.氢氧化钡溶液加入稀硫酸中:OH- + H+  H2O H2O |
C.石灰石加入稀盐酸中:CaCO3 + 2H+ Ca2+ + CO2↑ + H2O Ca2+ + CO2↑ + H2O |
D.铜片插入硝酸银溶液中:Cu + Ag+ Cu2++ Ag Cu2++ Ag |
下列叙述错误的是:
| A.酸、碱、盐、氧化物在组成上的共同点是都含有非金属元素 |
| B.只含有一种元素的物质不一定都是纯净物 |
| C.电离产生H+的化合物叫酸,其分子中氢原子的个数即是该酸的元数 |
| D.压强恒定时,气体在水中的溶解度随温度的升高而降低 |
下列说法正确的是(NA表示阿伏加德罗常数的值):
①28 g氮气所含有的原子数目为NA
②4 g金属钙变成钙离子时失去的电子数目为0.1 NA
③在常温常压下,11.2 L N2含有的分子数为0.5 NA
④在标准状况下, 1 mol氦气含有的原子数为NA
⑤0.5 mol单质铝与足量盐酸反应转移电子数为1.5NA
⑥标准状况下,1 L水所含分子数为1/22.4NA
⑦17 g氨气所含电子数目为10NA
| A.①②⑤⑥⑦ | B.①②④⑤⑥ | C.⑤⑦ | D.④⑤⑦ |
实验室里利用以下反应制取少量氮气:NaNO2+NH4Cl===NaCl+N2↑+2H2O。关于该反应的下列说法正确的是
| A.每生成1 mol N2转移的电子的物质的量为6 mol |
| B.N2既是氧化剂,又是还原剂 |
| C.NH4Cl中的氮元素被还原 |
| D.NaNO2是氧化剂 |
一定量某营养液中溶质的配方分别如下:
配方一:0.3mol KCl,0.2mol K2SO4,0.1 molZnSO4
配方二:0.1 mol KCl,0.3 mol K2SO4,0.1 molZnCl2
对于两种营养液的成分,下列说法中正确的是
| A.只有n(K+)相同 |
| B.只有n(Cl-)相同 |
| C.各离子的物质的量完全不同 |
| D.完全相同 |
下列实验操作正确的是:
| 编号 |
实验 |
操作 |
| A |
实验室用自来水制备蒸馏水 |
将自来水倒入烧杯中,小心给烧杯加热 |
| B |
配制一定浓度的氯化钾溶液100mL |
将称好的氯化钾固体放入100 mL容量瓶中,加水溶解,振荡摇匀,定容 |
| C |
检验溶液中是否含SO42- |
先加入稀盐酸,无明显现象,再加入BaCl2溶液 |
| D |
取出分液漏斗中的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
下列离子方程式正确的是:
| A.氧化铁和稀硫酸反应:Fe2O3+6H+ =2Fe2++3H2O |
| B.碳酸氢钠溶液中加稀硫酸:CO32-+2H+=H2O+CO2↑ |
| C.向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2+ + OH- + H+ + SO42- = BaSO4↓+ H2O |
| D.Cu(OH)2加入H2SO4:2H++Cu(OH)2 = Cu2+ +2H2O |
已知Co2O3在酸性溶液中易被还原成Co2+,且Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列叙述中,正确的是:
| A.Cl2通入FeI2溶液中,可存在反应3Cl2+6FeI2=2FeCl3+4FeI3 |
| B.每1 mol Co2O3在酸性溶液中被氧化生成Co2+时转移2 mol e- |
| C.FeCl3溶液能使淀粉- KI试纸变蓝 |
| D.I2具有较强的氧化性,可以将Co2+氧化成Co2O3 |
粗盐中含Ca2+、Mg2+、Fe3+、SO42—及泥沙等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:① 加入过量的Na2CO3溶液;② 加入过量的BaCl2溶液;③ 加入过量的NaOH溶液;
④ 加盐酸调节溶液的pH;⑤ 溶解;⑥ 过滤; ⑦ 蒸发。正确的操作顺序是
| A.⑤①③②④⑥⑦ | B.⑤①②③⑥④⑦ |
| C.⑤③①②⑥④⑦ | D.⑤③②①⑥④⑦ |
将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下:
| 物 质 |
a |
b |
c |
d |
| 反应前质量(g) |
6.4 |
3.2 |
4.0 |
0.5 |
| 反应后质量(g) |
待测 |
2.56 |
7.2 |
0.5 |
下列说法中错误的是:
A.a和b是反应物,d可能是催化剂
B.反应后a物质的质量为4.64g
C.c物质中元素的种类,一定等于a、b二种物质中元素的种类
D.若物质a与物质b的相对分子质量之比为2:1,则a与b的化学计量数之比为2:1
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.常温常压下,2.3 g Na变成Na2O2时,失去0.2NA个电子 |
| B.常温常压下,32 g氧气和32 g臭氧都含有2NA个氧原子 |
| C.500 mL 0.2 mol/L NaOH溶液中含有NA个Na+离子 |
| D.在20℃、1.01×105Pa时,11.2 L氮气含有NA个氮原子 |
已知在相同条件下进行下列反应:
①Cl2+2KBr=2KCl+Br2
②KClO3 +6HCl=3Cl2+KCl +3H2O
③2KBrO3 +Cl2=Br2 + 2KClO3,下列说法正确的是
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.反应①和反应③中均生成Br2,溴元素发生的变化相同 |
| C.反应②中被氧化与被还原物质的物质的量之比为6:1 |
| D.③中lmol还原剂反应则氧化剂得到电子的物质的量为10mol |
已知A2On2-可与B2-反应,B2-被氧化,产物为B单质,A2On2-被还原,产物为A3+;且知100 mL c(A2On2-)=" 0.3" mol/L的溶液与150 mL c(B2-) =" 0." 6 mol/L的溶液恰好完全反应,则n值为:
| A.4 | B.5 | C.6 | D.7 |
下列说法正确的是
| A.把100mL3mol·L-1的H2SO4跟100mLH2O混合,硫酸的物质的量浓度变为1.5mol·L-1 |
| B.把100g20%的NaCl溶液跟100gH2O混合后,NaCl溶液的溶质质量分数是10% |
| C.把200mL3mol·L-1的BaCl2溶液跟100mL3mol·L-1的KCl溶液混合后,溶液中的C(Cl-)仍然是3mol·L-1 |
| D.把100mL20%的NaOH溶液跟100mLH2O混合后,NaOH溶液的质量分数是10% |
(1)在标准状况下,测得1.32 g某气体的体积为0.672 L。则此气体的摩尔质量为 。
(2)等质量CO、CO2两种气体的的摩尔质量之比为 ;同温同压下的体积比为 ;其中氧元素的原子个数比为 。
(3)常用食醋除去水壶中的水垢,以氢氧化镁为例,表明反应原理(用离子方程式表示) 。
已知以下两个氧化还原反应的化学方程式:
①Cl2+H2O===HCl+HClO ②2Al+Fe2O3 Al2O3+2Fe
Al2O3+2Fe
(1)用单线桥法表示反应②中的电子转移情况:______。
(2)若反应②中每生成1 mol Fe,转移电子的物质的量是:________。
(3)将反应①改写成离子方程式:________。
化学实验中,如果使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如: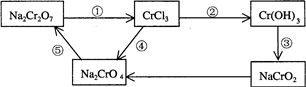
(1)在上述有编号的步骤中,需用还原剂的是 ,需用氧化剂的是 。(填编号)
(2)在 K2Cr2O7 + 14HCl ="===" 2KCl + 2CrCl3 + 3Cl2↑+ 7H2O反应中, 元素被氧化,
="===" 2KCl + 2CrCl3 + 3Cl2↑+ 7H2O反应中, 元素被氧化,
是氧化剂;并用双线桥表明电子转移方向与数目: 。
(3)在(2)的反应中,盐酸的作用: 。
实验室用NaOH固体配制250mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250mL 1.25mol/L的NaOH溶液, 应称取NaOH的质量 g;
(2)容量瓶上标有 ;且使用前第一步操作: ;
(3)溶液注入容量瓶前需冷却到室温,这是因为_____________________________;
(4)定容时的操作 ;
(5)下列配制的溶液浓度偏低的是 ;
| A.称量NaOH时,砝码错放在左盘 |
| B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面 |
| C.定容时俯视刻度线 |
| D.配制前,容量瓶中有少量蒸馏水 |
E.定容后经振荡、摇匀、正置,发现液面下降,再加适量的蒸馏水

 粤公网安备 44130202000953号
粤公网安备 44130202000953号