(10分)霞石是一种硅酸盐,其组成可表示为K2O·3Na2O·4Al2O3·8SiO2,某小组同学设计以霞石为原料制备Al2O3的方案如下:
请回答下列问题:
(1)沉淀1的主要成分的化学式为 。
(2)向滤液1中加入过量NaOH溶液的有关反应离子方程式为 。
(3)由溶液2生成Al(OH)3的离子方程式为 。
(4)某同学提出上述流程较繁琐,可简化流程,其方法是向滤液1中加入足量的试剂X即可得到Al(OH)3,则试剂X为 。
某无色透明溶液中只可能大量存在OH-、Cl-、Na+、Mg2+、Cu2+中的几种离子。
(1)溶液显无色,说明原溶液中不存在的离子是_______;
(2)取少量原溶液加入铝粉有气体放出,说明原溶液中肯定存在的离子是___________;该反应除产生气体外,另一种生成物的化学式是_________________;
(3)另取少量原溶液加入过量稀硝酸,再加几滴AgNO3溶液,出现白色沉淀。
该过程中发生2个反应,对应的离子方程式是 、 。
有以下几种物质:①NaOH ②HCl ③SO2 ④CaCO3 ⑤Fe2O3。回答有关问题:
(1)属于碱性氧化物的是_______(填编号);
(2)具有漂白性的物质是 (填编号);
(3)③与过量①的溶液反应的离子方程式为 ;
(4)①常常用于吸收多余的氯气,反应的化学方程式为 。
某研究性学习小组欲由硫铁矿烧渣(主要成分为Fe、Fe2O3、SiO2、Al2O3)制备绿矾(FeSO4·7H2O)并测定烧渣中铁元素的含量,流程图如下:
(1)操作a的名称是 。
(2)加入足量试剂X后,发生反应的离子方程式为 、 。
(3)向溶液2中滴加KSCN溶液,无明显现象。向固体中加入足量稀硫酸后,发生氧化还原反应的离子方程式是 、 。
(4)硫铁矿烧渣中铁元素的质量分数为 。
(1)请写出下列溶液的离子反应方程式:(13分)
①硫酸氢钠在溶液中的电离:
②氯化铵溶液除铁锈的原因:
③氯化铁溶液与偏铝酸钾溶液混合:
④碳酸钙的溶解平衡:
(2)在配制AgNO3溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,
以 (填“促进”、“抑制”)其水解。在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产是 。把Na2SO3溶液蒸干,灼烧,最后得到的主要固体产是 。
请分别选用一种试剂除去下列物质中的杂质,并写出相应的离子方程式。
| |
物质 |
杂质 |
所选试剂 |
离子方程式 |
| ① |
NaCl溶液 |
Na2CO3 |
|
|
| ② |
Mg粉 |
Al粉 |
|
|
(9分)“三酸两碱”是重要的化工原料,其中的“两碱”为氢氧化钠和碳酸钠。
(1)氢氧化钠不能保存在带玻璃塞的玻璃瓶中的原因是________________________。
(2)实验室配制100mL 1mol/L氢氧化钠溶液时,下列操作会导致浓度偏低的是_____
a.定容时仰视刻度线
b.容量瓶洗涤后没有干燥就直接用于溶液的配制
c.氢氧化钠溶解后没有冷却至室温,就将溶液转移到容量瓶中
d.定容摇匀后,发现液面低于刻度线,又加水使液面与刻度线相平
(3)将足量二氧化碳通入氢氧化钠溶液中的离子方程式为_________________。
(4)向碳酸钠溶液中逐滴加入稀盐酸至过量,碳酸氢根离子浓度变化趋势是_______;碳酸钠溶液中混有少量碳酸氢钠,可用氢氧化钠来除杂,反应的离子方程式为_______。
研究工业废弃物的处理和防治具有重要的意义。
(1)利用反应CH4+2NO2 N2+CO2+2H2O可消除NO2的污染,该反应中氧化剂是____,当消耗CH4的体积是11.2 L(标准状况下)时,理论上可处理____molNO2。
N2+CO2+2H2O可消除NO2的污染,该反应中氧化剂是____,当消耗CH4的体积是11.2 L(标准状况下)时,理论上可处理____molNO2。
(2)治理汽车尾气中CO和NO的一种方法是:在汽车排气管中安装一个催化转化装置,该装置能将CO和NO转化为参与大气循环的无毒气体。该反应的化学方程式为________________.
(3)某无色废水中可能含有Fe3+、Al3+、Na+、Cl-、OH-、SO42-、中的几种离子。分别取三份废水进行如下实验:
I.进行焰色反应实验,火焰为无色。
Ⅱ.取100 mL废水,加入足量的BaCl2溶液,生成2.33g白色沉淀。
Ⅲ.取100 mL废水,逐滴加入1.0 mol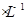 的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如下图所示。
的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如下图所示。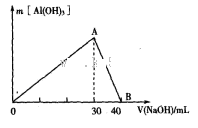
请根据上述信息回答下列问题:、
①该废水中一定不含有的离子是__________.
②实验中需配制1.0 mol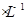 的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器有_______。
的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器有_______。
③写出图中A→B反应的离子方程式:_______________________。
④通过计算,该废水中______Cl-(填“含有”或“不含有”);若含有,则c(Cl-)=________(若不含有,此问不必作答)。
某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:
(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为_________,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
(1)实验室制取Cl2的反应方程式之一为: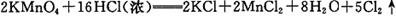 。
。
被氧化的盐酸占反应盐酸总量的 ,用NA表示阿伏加德罗常数的值,当标准状况下有11.2L氯气生成时,该反应的电子转移数为 。
(2)已知下列两个氧化还原反应:O2+4HI 2I2+2H2O 及Na2S+I2══2NaI+S,则三种单质的氧化性顺序由强到弱为:
2I2+2H2O 及Na2S+I2══2NaI+S,则三种单质的氧化性顺序由强到弱为:
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式: ;在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式: 。
(4)医疗上常用小苏打治疗胃酸过多,小苏打溶液与盐酸反应的离子方程式为: 。
炼金废水中含有络离子[Au(CN)2]+,其电离出的CN—有毒,CN-与H+结合生成HCN时,其毒性更强。回答下列问题:
(1)HCN的电离方程式为______________________NaCN溶液的pH_____7(填“< > =”)
(2)与弱电解质的电离方程式相似,[Au(CN)2]+也存在着两步电离,其一级电离方程式为________。
(3)处理这种废水是在碱性条件下,NaClO将CN—氧化为碳酸根和氮气,其离子方程式为:_______。
(4)在酸性条件下,ClO—也能氧化CN--,但实际处理废水时却不在酸性条件下进行的原因是_________。
试样X由氧化亚铁和氧化铜组成,取质量相等的两份试样按图所示进行实验:
(1)请写出步骤③中所发生的全部反应的离子方程式。
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m,则每份试样X中氧化铜的质量为______________(用m表示)。
写出下列离子方程式:
(1)泡沫灭火器原理:__________________________________________________________________
(2)胃舒平治疗胃酸过多:____________________________________________________________
(3)FeS除去废水中铅离子:_____________________________________________________
取来两份等浓度的NaOH溶液A和B,每份10ml,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,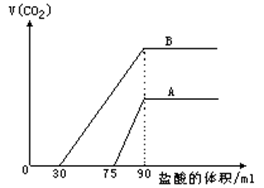
试回答下列问题:
(1)原NaOH溶液的物质的量浓度为 _______________mol/L
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质为(写化学式)___________________;其物质的量之比为_____________。
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸产生CO2气体体积(标准状况)的最大值为________________ml。