完成下列反应的离子方程式:
(1)将AlCl3溶液蒸干得到白色固体: ;
(2)用惰性电极电解饱和食盐水: ;
(3)用KOH做电解质溶液的甲烷燃料电池的负极反应式: ;
(4)往AgCl悬浊液中滴加Na2S溶液: ;
元素周期表中第三周期元素的单质及其化合物的用途广泛。
(1)该周期元素中,半径最小的简单离子的离子结构示意图为 。
(2)能证明氯的非金属性(得电子能力)比硫强的化学方程式为 。
(3)NaHSO3溶液呈酸性,其溶液中离子浓度由大到小的顺序为 。
(4)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl—,该反应的离子方程式为 。
(5)已知下列两反应过程中能量变化如图所示:
汽车尾气中含有的少量NO2和SO2在一定条件下会发生反应,该反应的热化学方程式为____________。
现有含NaCl、Na2SO4、Na2CO3和NaHCO3的固体混合物。某同学为测定其中各组分的含量,取部分样品溶于水,并设计了如下实验流程(所加试剂均为过量,反应①~③均为复分解反应)。
请回答: (1)气体W的化学式是 。
(1)气体W的化学式是 。
(2)反应①的离子方程式是  。
。
(3)试剂X、Y、Z依次是 。
(4)下列说法正确的是 (填字母) 。
。
a.溶液A的焰色反应为黄色
b.反应②和③之后均需进行过滤操作
c.若测得气体W的体积(标准状况)、白色沉淀Ⅰ和Ⅱ的质量,可计算出各组分的量
某溶液中含有Ba2+,Cu2+, Ag+,现用NaOH溶液、盐酸和Na2CO3溶液将这三种离子逐一沉淀分离。其流程图如所示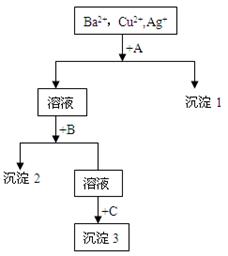
(1)沉淀的化学式(写出最佳答案):
沉淀1 ,沉淀3 ;
(2)写出溶液+B的离子方程式: 。
K2Cr2O7是一种橙红色具有强氧化性的化合物,当它在酸性条件下被还原成正三价铬时,颜色变为绿色。据此,当交警发现汽车行驶不正常时,就可上前阻拦,并让司机对填充了吸附有K2Cr2O7的硅胶颗粒的检验装置吹气。若发现硅胶变色达到一定程度,即可证明司机是酒后驾车。这时酒精被氧化为醋酸其反应原理如下:
2K2Cr2O7+3CH3CH2OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O
请结合上面的描述回答下列问题:
(1)将上述反应改写为离子方程式: 。
(2)如果司机属于醉酒驾车,则检验装置中的硅胶将由 色变为 色。
(3)上述反应中氧化剂是 ,还原剂是 ,氧化产物是 ,还原产物是 。(本题中的四个空都需填写物质的化学式)
(4)在上述反应中当有69g酒精发生反应时消耗K2Cr2O7的物质的量是
(8分)(1)向某溶液中加入KSCN溶液无明显现象,再滴入数滴氯水后,溶液立即变成红色,则原溶液中一定含有________离子,要除去FeCl3溶液中少量的氯化亚铁,可行的办法是________(填字母)。
| A.加入铜粉 | B.加入铁粉 | C.通入氯气 | D.加入KSCN溶液 |
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式
________________________ _______。
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式____________ __________________________。
(3)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是_________,区别该液体和FeCl3溶液可用 方法。
(7*1分)某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:
(1)操作①的名称是 ,操作②的名称是 。
(2)试剂a是 ,试剂b是 ,固体B是 。(填化学式)
(3)加入试剂a所发生的离子方程式为: 。
加入试剂b所发生的离子方程式为: 。
(4*2分)写出下列反应的离子方程式:
(1)氢氧化钠与硫酸反应 ;
(2)实验室制取CO2气体 ;
(3)少量CO2气体通入澄清石灰水 ;
(4)硫酸铜溶液与氢氧化钠反应 。
(12分,每空3分)已知A为金属单质,C为一种强碱。它们有以下相互转化。试回答:
(1)写出B的化学式 ,D的化学式 。
(2)写出由D转变成H的化学方程式 。
(3)写出向G溶液加入A的有关离子反应方程式 。
按要求完成下列化学用语:
(1)NaHSO4的电离方程式: ,
(2)CuSO4溶液和NaOH溶液反应的离子方程式: ,
(3)能用H++OH-=H2O表示的一个化学方程式: 。
氧化还原反应在工农业生产和日常生活中有广泛运用。
(1)罐头厂在装食物罐头时通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类防腐剂应具有 。(填“氧化性”或“还原性”);
(2)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是 。(填“氧化作用”或“还原作用”);
(3)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 。
(4)在下列的空白处填写最适宜的除杂试剂,并写出相应的离子方程式
①FeCl2中含少量FeCl3杂质 , 。
②FeCl3中含少量FeCl2杂质 , 。
③FeSO4中含少量CuSO4 杂质 , 。
某混合物的水溶液,可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH、Cl-、CO、SO,现分别取100 mL的两等份溶液进行如下实验:
①第一份加过量NaOH溶液后加热,收集到0.02 mol气体,无沉淀生成,同时得到溶液甲。
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、干燥、灼烧后,得到1.02 g固体。
③第二份加足量BaCl2溶液后,生成白色沉淀,沉淀经足量盐酸洗涤、干燥后,得到11.65 g固体。
依据实验回答下列问题:
(1)由①可知一定存在的离子为 ,其浓度为 mol·L-1。
(2)写出②中产生沉淀的离子方程式 。
(3)由③可知一定存在的离子为 ,其浓度为 mol·L-1。
(4)综合上面三个实验,该混合物的水溶液中一定不存在的离子是 (填离子符号)。
(5)某同学通过分析认为该溶液中一定存在K+,他的理由是 。
某铝合金中含有铁、铝、镁、铜、硅。为了测定该合金中铝的含量,现设计了如下实验:
已知:Si+2NaOH+H2O=Na2 Si O3+2H2↑,H2Si O3是不溶于水的弱酸。
(1)固体A的成分是:____________,溶液M中的阴离子有:____________________
(2)步骤③中生成沉淀的离子方程式为:_____________________________________
(3)步骤④中,用到的仪器有三脚架、酒精灯以及
(4)在空气中将NaOH溶液滴入FeCl2溶液中,观察到的现象是 ,反应的化学方程式是 ,
(5)该样品中铝的质量分数是:_______________________________(用a、b表示)。
(6)下列因操作不当,会使测定结果偏大的是___________
| A.第①步中加入NaOH溶液不足 | B.第②步中加入盐酸不足时 |
| C.第④步中的沉淀未用蒸馏水洗涤 | D.第④步对沉淀灼烧不充分 |
(本题3个空,每空2分,共6分)
在盛有100mL浓硝酸的试管中加入32g铜片发生反应。请回答:
(1)开始阶段,反应的离子方程式是 。
(2)若二者恰好完全反应,共产生气体11.2L(标准状况)。则浓硝酸的物质的量浓度为 。
(3)反应结束后的试管中,再加入金属铜和入少量20%的稀硫酸,这时溶液中又有气泡产生,请写出反应的离子方程式是 。
A~G各物质间的关系如图,其中B、D为气态单质。
请回答下列问题:
(1)物质C、E分别为 、 。(填名称)
(2)反应①可选用不同的A进行,若反应在常温下进行,其化学方程式为 。
(3)反应②的离子方程式为 。
(4)新配制的F溶液应加入________以防止其转化为G。请设计实验检验F、G的混合溶液中F的金属阳离子。(写出试剂、操作、现象、结论) 。