过氧化氢(H2O2)的水溶液俗称双氧水,近年来倍受人们的青睐,被称为“绿色氧化剂”。
(1)写出H2O2的电子式 。
(2)你认为H2O2被称为“绿色氧化剂”的主要原因是 。
(3)将双氧水加入用盐酸酸化的FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式为 ,反应中H2O2作 剂。
(4)双氧水能使酸性高锰酸钾溶液褪色,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里: MnO4﹣+ H2O2+ H+═ Mn2++ H2O+ 。
(10分)下列六个图中,横坐标为某溶液中加入某物质的物质的量,纵坐标为生成沉淀的物质的量,请把下表中各反应的相应图像的序号填入表中。

| 溶液 |
加入的物质 |
答案序号 |
| ①饱和石灰水 |
通过量CO2 |
|
| ②AlCl3溶液 |
通过量NH3 |
|
| ③MgCl2、AlCl3混合溶液 |
逐滴加NaOH溶液至过量 |
|
| ④AlCl3溶液 |
逐滴加NaOH溶液至过量 |
|
| ⑤含少量HCl的AlCl3溶液 |
逐滴加NaOH溶液至过量 |
|
某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化。
(1)该同学最初的实验操作和现象如下:
| 编号 |
操作 |
现象 |
| I |
先向2 mL 0.1 mol/L FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 |
|
| II |
先向2 mL 0.1 mol/L FeCl3溶液中滴加KSCN溶液,再滴加0.1 mol/L KI溶液 |
|
①实验II的预期现象为 。
②FeCl2溶液与新制氯水反应的离子方程式为 。
(2)该同学在进行实验I时,加入的氯水过多,导致出现的红色又褪去,则可能的原因是 。
氧化还原反应在生产、生话中应用广泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂。用所学知识回答问题( )
(1)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的化学方程式为 ,反应中消耗1mol的MnO4—时转移电子数为 。
(2)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是 mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是 ,又变为棕黄色的原因是 。
已知离子反应:RO3n-+6I - +6H +  R - +3I 2 +3H 2 O,试根据离子方程式必须“质量守恒、电荷守恒”等判断:n=__________,R元素在 RO3n-中的化合价是__________。
R - +3I 2 +3H 2 O,试根据离子方程式必须“质量守恒、电荷守恒”等判断:n=__________,R元素在 RO3n-中的化合价是__________。
现有失去标签的氯化钙,硝酸银,盐酸,碳酸钠四种无色溶液,为了确定四种溶液各是什么,将它们随意编号上A.B.C.D后,,产生的现象如下表所示:
| 实验顺序 |
实验内容 |
实验现象 |
| (1) |
A+B |
没有现象发生 |
| (2) |
B+D |
有气体放出 |
| (3) |
B+C |
有沉淀生成 |
| (4) |
A+D |
有沉淀生成 |
根据实验现象按要求回答:
(1)写出A.B.C.D溶液中溶质的化学式:
A______ B_______ C_____ D______
(2)写出上述实验中有关反应的离子方程式
实验(2)__________________
实验(3)__________________
水处理技术在生产、生活中应用广泛,对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(l)水的净化是用混凝剂将水中的胶体和悬浮物沉淀下来,而水的软化则是 ;
(2)生活用水必须保证安全,自来水厂需要对取自江河湖泊中的淡水进行杀菌消毒、混凝沉淀、过滤等工艺处理,这三项处理的正确顺序是 ;
(3)下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是 (填字母);
| A.福尔马林 | B.漂白粉 | C.氯气 | D.臭氧 |
(4)Na2FeO4是一种新型水处理剂,工业上可用FeSO4制备Na2FeO4,其工艺流程如下:

①硫酸亚铁常用作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加入绿矾。用离子方程式解释这一原因: ;
②写出由Fe(OH)3制取Na2FeO4的化学方程式: ;
(5)石灰纯碱法是常用的硬水软化方法,已知25℃时Ksp(CaCO3)=2.8×10-9,现将等体积的Ca(OH)2溶液与Na2 CO3溶液混合(假设溶液体积具有加和性),若Na2 CO3溶液的浓度为5.6 x10一5mol·L一1,则生成沉淀所需Ca(OH)2溶液的最小浓度为 。
元素周期表中第3周期元素的单质及其化合物的用途广泛。

(1)该周期元素中,半径最小的简单离子的结构示意图为 ,最活泼金属元素和最活泼非金属元素形成的化合物的电子式为 ;
(2)氯的氧化物具有强氧化性,其中ClO2可将弱酸性废水中的Mn 2+转化为MnO2而除去,同时ClO2被还原为Cl--,该反应的离子方程式为 ;
(3)已知SO2,NO分别与O2反应过程中能量变化如图所示:写出NO2和SO2在一定条件下发生反应的热化学方程式 。
向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式:__________________。
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液中显中性
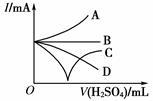
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的_______曲线表示(填序号)。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将___ 。
(1)中学常见的某有色物质,全部由短周期元素组成,能与水发生氧化还原反应,但反应中水既不作氧化剂也不作还原剂。试写出符合条件的两种物质(写化学式)________、________。
(2)在一定条件下,RO3n-和I-发生反应,离子方程式为: RO3n-+6I-+6H+=R-+3I2+3H2O , RO3n-中R元素的化合价为 ,R元素的原子最外层电子有 个。
利用I2的氧化性可测定钢铁中硫的含量。做法是将钢铁中的硫转化为H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为 ,该滴定反应的离子方程式为 。
2014年8月3日16时30分在云南省昭通市鲁甸县(北纬27.1度,东经103.3度)发生6.5级地震,震源深度12千米,已致589人遇难。饮用水安全在灾后重建中占有极为重要的地位,某研究小组提取三处被污染的水源进行了如下分析:并给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E五种常见化合物都是由下表中的离子形成的:
| 阳离子 |
K+、Na+、Cu2+、Al3+ |
| 阴离子 |
SO 、HCO 、HCO 、NO 、NO 、OH- 、OH- |
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入Ba(NO3)2溶液,再加入过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验现象填写下列空白:
(1)写出化学式:A________ 、B________、C ________ 、D________。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为________。
(3)写出实验②发生反应的离子方程式__________________、________________。
(4)C常用作净水剂,用离子方程式表示其净水原理_________________________。
以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
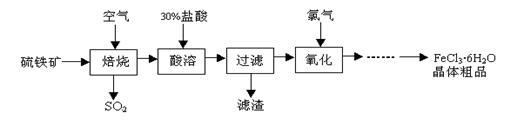
请回答下列问题:
(1)硫铁矿“焙烧”中反应的化学方程式为3FeS2 +8O2 + 6SO2,则 中的化学式为 ,反应中化合价升高的元素有 。
+ 6SO2,则 中的化学式为 ,反应中化合价升高的元素有 。
(2)“酸溶”中反应的化学方程式为 。
(3)“过滤”后滤液中金属阳离子有 。
(4)“氧化”中反应的离子方程式为 。
(5)该工艺流程中产生的SO2会污染空气,常用烧碱溶液来吸收。写出吸收过程中反应的化学方程式 。
(10分)完成下列离子方程式
(1)Ba(OH)2溶液与(NH4)2SO4溶液混合__________________
(2)Ca(HCO3)2溶液与NaOH溶液反应
①NaOH不足:_________________________
②NaOH过量:_________________________
(3)Ba(OH)2溶液与NaHSO4溶液的反应
①溶液呈中性:_________________________
②此时溶液呈碱性:________________________
(5分)向盛有1 mL 0.1 mol/L MgCl2溶液的试管中滴加1~2滴2 mol/L NaOH溶液,观察到有白色沉淀生成,该反应的离子方程式是________________。再滴加2滴0.1 mol/L FeCl3溶液,观察到白色沉淀转化为红褐色沉淀,该反应的离子方程式是___________________。由以上现象可以推知,相同条件下Mg(OH)2和Fe(OH)3中溶解度较大的是_________________。
I.有以下物质:
①石墨;②铝;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;
⑦氢氧化钡溶液;⑧纯醋酸;⑨氯化氢气体。
(1)其中能导电的是 ;
属于非电解质的是 ;
属于强电解质的是 ;
属于弱电解质的是 。
(2)写出物质⑥溶于水的电离方程式: 。
(3)写出物质⑥和⑧在水中反应的离子方程式: 。
Ⅱ.今有K2SO4和Al2(SO4)3的混合溶液,已知其中K+浓度是0.2mol•L-1,SO42- 的浓度是0.7mol•L-1。
(4)则 Al3+ 物质的量浓度应等于 。
Ⅲ.根据反应8NH3+3Cl2 → 6NH4Cl+N2,回答下列问题:
(5)该反应中氧化剂是 ,氧化产物是 。
(6)该反应中被氧化的物质与被还原的物质物质的量之比为 。
(7)用单线桥法标出电子转移的方向与数目。
IV.有一包白色固体,可能含有K2CO3、NaNO3、KCl、BaSO4、CuSO4。按下列步骤实验:①取少量固体溶于水,得到无色溶液;②在所得的溶液中滴加硝酸银溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解,并有气体产生。根据上述实验现象判断:
(8)一定存在的物质是 ;
(9)一定不存在的物质是 ;
(10)可能存在的物质是 ;