近期发现, 是继NO、CO之后第三个生命体系气体信号分子,它具有参与调解神经信号传递、舒张血管减轻高血压的功能.回答下列问题:
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是(填标号).
| A. | 氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以 |
| B. | 氢硫酸的导电能力低于相同浓度的亚硫酸 |
| C. | 的氢硫酸和亚硫酸的pH分别为4.5和2.1 |
| D. | 氢硫酸的还原性强于亚硫酸 |
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理.

通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为________、________,制得等量H 2所需能量较少的是________.
(3) 与 在高温下发反应:生 .在610k时,将 与 充入2.5L的空钢瓶中,反应平衡后水的物质的量分数为0.02.
① 的平衡转化率 =________%,反应平衡常数K=________.
②在620K重复试验,平衡后水的物质的量分数为0.03, 的转化率 ________ , 该反应的△H________0.(填">""<"或"=")
③向反应器中再分别充入下列气体,能使 转化率增大的是________(填标号)
| A. |
|
B. |
|
C. |
COS |
D. |
|
下列离子方程式书写正确的是( )
| A.向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
| B.碳酸钠溶液与硫酸氢钠溶液反应:CO32-+H+=CO2↑+H2O |
| C.Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D.向FeBr2溶液中通入足量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
下列离子方程式与所述事实相符且正确的是( )
A.实验室用MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓) Mn2++2Cl﹣+Cl2↑+2H2O Mn2++2Cl﹣+Cl2↑+2H2O |
| B.Ca(HCO3)2溶液中加入少量烧碱溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| C.向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42﹣+Ba2++2OH﹣=2H2O+BaSO4↓ |
| D.向次氯酸钠溶液中通入SO2:2ClO−+SO2+H2O=SO32-+2HClO |
能正确表示下列反应的离子方程式是
| A.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2=2NH4++SO32-+H2O |
| B.NaHSO3溶液中通入少量Cl2:HSO3- + Cl2+ H2O=3H+ +SO42- +2Cl- |
C.氯化钠与浓硫酸混合加热:H2SO4+2Cl- SO2↑+Cl2↑+H2O SO2↑+Cl2↑+H2O |
| D.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O |
已知实验室制取Cl2的反应为:MnO2+4HCl(浓)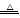 MnCl2+Cl2↑+2H2O,又已知Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,也能氧化浓盐酸生成Cl2;
MnCl2+Cl2↑+2H2O,又已知Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,也能氧化浓盐酸生成Cl2;
(1)写出PbO2与浓盐酸反应的化学方程式 ,其中表现还原性的HCl与表现酸性的HCl的物质的量之比为
(2)已知硫酸铅不溶于水,铅蓄电池的工作原理为Pb+PbO2 +2H2SO4 =2PbSO4+2H20,写出该反应的离子方程式 ;溶液中硫酸根离子检验的方法为 。
(3)已知PbSO4不溶于水,但可溶于醋酸铵溶液,反应方程式如下:PbSO4 +2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4.
①PbSO4与CH3COONH4能进行反应的原因是符合了复分解反应条件之一的生成了 ,现将Na2S 溶液与醋酸铅溶液混合有沉淀生成,则其反应的离子方程式应为 。
②已知+2价Sn的化合物具有强还原性。等物质的量的PbO2和SnO的混合物溶于过量的稀硫酸中,溶液中存在的主要金属阳离子是 (填序号)。
| A.Pb2+ | B.Pb4+ | C.Sn2+ | D.Sn4+ |
A、B、C、D为可溶于水的四种固体,B的水溶液呈浅绿色,D为含氧酸盐,组成它们的离子有:
| 阳离子 |
Fe2+、Na+、Ba2+、Al3+ |
| 阴离子 |
Cl-、SO42-、NO3-、OH- |
Ⅰ.将四种固体溶于水,分别取它们的水溶液进行实验,结果如下:
(1)A溶液的颜色反应为黄色,则A溶液中含有的金属离子是___________(填离子序号)。
(2)将A的水溶液逐滴加入C中,先生成白色沉淀,后白色沉淀逐渐溶解,请写出白色沉淀逐渐溶解的离子方程式___________________。
(3)B溶液与D溶液反应生成不溶于稀硝酸的白色沉淀,请写出该反应的离子方程式_____________。
Ⅱ.(4)据此推断它们是(写化学式)A______________;D_____________。
(5)A溶液与B溶液反应的现象为________________________。
海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

请填写下列空白:
(1)步骤①所需要的硅酸盐仪器是___________ ,步骤③的实验操作是___________。
(2)步骤⑤中,某学生选择用苯来提取碘水中的单质碘的理由是 _______ 。(选填序号)
a.单质碘与苯不发生化学反应 b.碘在苯中溶解度小
c.碘在苯中溶解度大 d.苯与水互不相溶
(3)提取碘的过程中,不能使用的有机溶剂是 ___ 。(选填序号)
a.酒精 b.汽油 c.四氯化碳
(4)步骤④中所发生的离子反应方程式 _____________。
(5)已知:2Fe3++2I-→2Fe2++I2 氯气既可以氧化Fe2+,也可以氧化I-。 往FeI2溶液中通入一定量的 Cl2,反应完成后,溶液中有1/2Fe2+被氧化,请写出该反应的化学反应方程式:__________。
某课外活动小组的同学,在实验室做锌与浓硫酸的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两同学的判断是否正确,丙同学设计了如下图所示的实验装置,已知C装置为黑色的粉末状物质(锌与浓硫酸共热时产生的气体X,且该反应装置已略去)。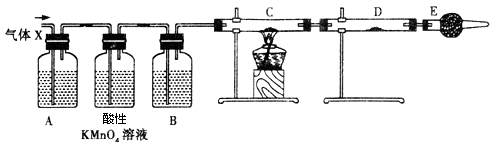
请回答:
(1)乙同学认为还可能产生氢气的离子方程式是_______________
(2)丙同学在安装好装置后,必不可少的一步操作是_______________
(3)A中加入的试剂作用是____________;B中加入的试剂可能是____________, E中加入的试剂如果是碱石灰,其作用为__________________。
(4)可以证明气体X中含有氢气的实验现象:C中:黑色粉末变成红色,D中:____________。
下列反应的离子方程式书写正确的是
| A.钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B.向Al2(SO4)3溶液中加入过量NH3∙H2O:Al3++4NH3∙H2O=AlO2-+4NH4++2H2O |
| C.酸性溶液中KClO3与KCl反应生成Cl2:ClO3-+Cl-+6H+=Cl2↑+3H2O |
| D.向含1molNaHSO3的溶液中加入1molNa2O2:Na2O2+HSO3-=2Na++SO42-+OH- |
下列离子方程式正确的是
| A.向碘化亚铁溶液中滴加溴的四氯化碳溶液2Br2+2Fe2++2I-=I2+4Br-+2Fe3+ |
| B.向含等物质的量浓度AgNO3和Cu(NO3)2的溶液中缓慢加入镁粉4Cu2++2Ag++5Mg=4Cu+2Ag+5Mg2+ |
| C.氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
| D.向0.3mol/LNaClO溶液中滴加等体积的0.2mol/LNaHSO3溶液: |
2HSO3-+4ClO-=2SO42-+2Cl-+2HClO
有一包白色固体粉末,可能含有K2SO4、Na2CO3、NH4Cl、BaCl2、CuSO4中的一种或几种,按以下步骤进行实验:
①取少量固体粉末加到足量水中,得到无色溶液;
②取①中溶液少量继续往其中加入足量稀硫酸,有气泡产生;
③继续向②中的溶液加Ba(NO3)2溶液,有白色沉淀生成;
④取①中溶液少量,加入NaOH溶液并加热,产生刺激性气味的气体,并用湿润的红色石蕊试纸检验气体,试纸变蓝。
根据以上事实判断:
(1)肯定存在的是______________。
(2)肯定不存在的是____________。
(3)不能确定是否存在的是_____________。请简述证明该物质是否存在的实验方案(实验方法、现象、结论)__________________________。
(4)写出上述实验④中产生刺激性气味反应的离子方程式:_____________________。
下列指定反应的离子方程式正确的是
| A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
| B.向CuSO4溶液中加入NaOH:Cu2++2OH-=Cu(OH)2↓ |
| C.在酸性溶液中,KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O |
| D.向Al2(SO4)3溶液中加入过量的NH3∙H2O:Al3++4NH3∙H2O=AlO2-+4NH4++2H2O |
玻璃容器被下列物质沾污后,需要洗涤。如洗涤方法属于物理方法的,请写出所需试剂;洗涤原理属于化学反应的,写出有关反应的离子方程式;若无法用试剂使容器复原者,请说明原因。
(1)盛石灰水后的沾污:
(2)碘的沾污:
(3)硫的沾污:
(4)长期盛强碱溶液的试剂瓶变“毛”了。
现有一包白色粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3、Na2SO4现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀产生:
②向①的悬浊液中加入过量稀盐酸,白色沉淀部分溶解,并有气泡放出:
③取少量②的上层清液滴入硝酸银溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题:
(1)判断原白色粉末中肯定含有, ,可能含有 。
(2)写出上述实验中一定发生的有关反应的离子反应方程式: 。
现有下列十种物质:①液态氯化氢②小苏打 ③固体纯碱 ④二氧化碳⑤葡萄糖 ⑥氢氧化钾 ⑦氢氧化铁胶体 ⑧氨水 ⑨空气 ⑩硫酸铁溶液
(1)上述十种物质中,属于电解质的有 ,属于非电解质的有 。
(2)有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为 。
(3)除去③中少量②的操作是 ,化学方程式为 。
(4)标准状况下,___________L ④中含有0.4mol 氧原子。
(5)现有100 mL⑩溶液中含Fe3+ 5.6g,则溶液中SO42-的物质的量浓度是 。
(6)若在⑦中缓慢加入⑥,产生的现象是 。
(7)将①加入到⑧中,⑧的导电能力变化为__________(填“增强”、“减弱”或“基本不变”)。