河南省信阳市高一上学期期末教学质量监测化学试卷
2015年10月,屠呦呦因发现青蒿素(化学式:C15H22O5)获诺贝尔医学奖。受东晋葛洪药典启发,屠呦呦用乙醚为溶剂在低温下从黄花蒿中成功提取青蒿素,成为目前国际高效抗疟药。下列有关说法错误的是
| A.青蒿素是含有三种元素的有机化合物 |
| B.青蒿素分子中CxHyO原子个数比为15:22:5 |
| C.从黄花蒿提取青蒿素发生了化学变化 |
| D.PM2.5由于颗粒小,在空气中存在时间长,对人体健康危害大提取过程中用到了萃取原理 |
下列关于实验安全的说法中正确的是
| A.实验室可用燃着的酒精灯去点燃另一只酒精灯 |
| B.蒸馏实验时,在烧瓶内加几粒沸石以防止暴沸 |
| C.化学品仓库保存的金属钠着火时可用水灭 |
| D.盛放浓盐酸的试剂瓶上要贴上如图的标志 |

下列变化过程不涉及氧化还原反应的是
| A |
B |
C |
D |
 |
 |
 |
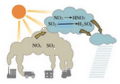 |
| 镁条的燃烧 |
人工吹制玻璃器皿 |
铜狮表面出现铜绿 |
酸雨的形成 |
下列各组溶液不能通过互滴实验进行鉴别的是
| A.碳酸钠稀盐酸 | B.碳酸氢钠稀盐酸 |
| C.氢氧化钠氯化铝 | D.偏氯酸钠稀硫酸 |
某学生课外活动小组利用右图装置作如下实验:在试管中注入某无色溶液,加热试管,溶液颜色变为红色。冷却后变为无色,则原溶液可能是
| A.溶有SO2的品红溶液 | B.溶有NH3的酚酞溶液 |
| C.溶有SO2的酚酞溶液 | D.溶有Cl2的品红溶液 |
向含有Fe2+、Fe3+、Mg2+、NH4+的水溶液中,加入足量的Na2O2固体,充分反应后再加入过量的稀盐酸,上述离子数目没有变化的是
| A.Fe2+ | B.NH4+ | C.Fe3+ | D.Mg2+ |
氯气的水溶液称“氯水”,氯水中含有多种分子和离子,因此氯水有多重性质,下列有关新制氯水的说法中不正确的是
| A.新制氯水呈黄绿色,且有刺激性气味,说明氯水中含有Cl2 |
| B.新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,可说明氯水中含有Cl2 |
| C.向淀粉碘化钾溶液中加入氯水,溶液变成蓝色,说明Cl2可以与盐发生置换反应 |
| D.新制氯水滴到Na2CO3溶液中,有气体产生,说明氯水中含有H+ |
下列关于纯净物、混合物、电解质、非电解质的正确组合是( )
| |
纯净物 |
混合物 |
电解质 |
非电解质 |
| A |
盐酸 |
冰水混合物 |
硫酸 |
干冰 |
| B |
蒸馏水 |
蔗糖溶液 |
氧化铝 |
二氧化硫 |
| C |
明矾 |
盐酸 |
铁 |
碳酸钙 |
| D |
胆矾 |
食盐水 |
氯化铜 |
碳酸钠 |
下列叙述正确的是( )
| A.某元素由化合态变为游离态时,该元素一定被还原 |
| B.金属阳离子被还原不一定得到金属单质 |
| C.生成非金属单质的反应一定是氧化反应 |
| D.在氧化还原反应中,非金属单质一定是氧化剂 |
已知有如下反应:
①ClO3-+5Cl-+6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,
③2FeCl2+Cl2=2FeCl3,判断下列各微粒氧化能力由强到弱的顺序正确的是( )
| A.Cl2>ClO3->Fe3+>I2 | B.Cl2>ClO3-> I2 > Fe3+ |
| C.ClO3- > Cl2 >Fe3+>I2 | D.ClO3->Fe3+ Cl2>I2 |
淀粉溶液是一种胶体,并且淀粉遇到碘单质,可以出现明显的蓝色特征。现将淀粉和稀Na2SO4溶液混合,装在半透膜中,浸泡在盛蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是( )
| A.加入BaCl2溶液产生白色沉淀 | B.加入碘水不变蓝 |
| C.加入BaCl2溶液没有白色沉淀产生 | D.加入碘水变蓝 |
在下列各溶液中离子一定能大量共存的是
| A.强碱溶液中:K+、Al3+、Cl-、SO42- |
| B.含0.1mol∙L-1Fe3+的溶液中:K+、Ba2+、NO3-、SO42- |
| C.含0.1mol∙L-1Ca2+的溶液中:Na+、K+、CO32-、Cl- |
| D.室温下c(H+)=0.1mol∙L-1的溶液中:Na+、Fe3+、NO3-、SO42- |
下列离子方程式书写正确的是
| A.AlCl3溶液中加入过量氨水:Al3++4NH3∙H2O=AlO2-+4NH4++2H2O |
| B.澄清石灰水与少量苏打溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| D.氯化亚铁中通入氯气:2Fe2++Cl2=2Fe3++2Cl- |
下列关于物质的量浓度表述正确的是
| A.0.3mol∙L-1的Na2SO4溶液中含有Na+和SO42-的总物质的量为0.9mol |
| B.当1L水吸收22.4L氨气时所得氨水的浓度不是1mol∙L-1,当22.4L氨气溶于水制得1L氨水时,其浓度才是1mol∙L-1 |
| C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同 |
| D.10℃时,100mL 0.35mol∙L-1的KCl饱和溶液蒸发掉5g水,冷却到10℃时,其体积小于100mL。它的物质的量浓度仍为0.35mol∙L-1 |
加热21.2gKOH和KHCO3的混合物使其充分反应后冷却,称得固体质量减少1.8g,则下列说法正确的是(n表示物质的量)
| A.n(KOH)=0.1mol | B.n(KOH)<n(KHCO3) |
| C.n(KHCO3)=0.2mol | D.n(KOH)>n(KHCO3) |
在一定条件下,将等体积的NO和NO2充入试管,并将试管倒立于水槽,充分反应后剩余气体的体积缩小为原体积的
| A.1/2 | B.1/3 | C.3/8 | D.2/3 |
24mL0.05mol∙L-1的Na2SO3恰好与20mL0.02mol∙L-1的K2R2O7溶液完全反应,则R元素在还原产物中的化合价为
| A.0 | B.+2 | C.+3 | D.+6 |
铜既不溶于稀硫酸,也不溶于NaNO3溶液,但可溶于其混合液。现将1.92gCu放入足量的稀硫酸中,若要使铜完全溶解,理论上至少应加入NaNO3晶体的物质的量为
| A.0.02mol | B.0.045mol | C.0.06mol | D.0.08mol |
下列是用98%的浓H2SO4(ρ=1.84g/cm3)配制500mL 0.5mol∙L-1的稀硫酸的实验操作,请按要求填空:
(1)实验中量取浓硫酸的体积为_________mL。
(2)如果实验室有10mL、20mL、50mL的量筒,应选_______规格的量筒最好,如果量取浓硫酸时仰视读数,所配溶液浓度将(填“偏高”、“偏低”或“无影响”)__________。
(3)将量取的浓硫酸沿烧杯内壁慢慢注入盛有约少量水的烧杯里,并不断搅拌,搅拌的目的是_____________________。
(4)将冷却至室温的上述溶液沿玻璃棒注入_______中,并用50mL蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液要转入到容量瓶中,并振荡;在转移过程中有少量液体洒在桌子是,则最终所配浓度将(填“偏高”、“偏低”或“无影响”)__________。
(5)加水至距刻度线1~2cm处,改用______加水至刻度线,使溶液的凹液面恰好跟容量瓶刻度线相平,把容量瓶塞好,反复颠倒振荡,摇匀溶液。
金属及其化合物在化学中扮演着重要的角色,同学们应该熟练掌握它们的性质。
(1)钠与水反应时,钠漂浮在水面上。甲同学用刺有小孔的铝箔将4.6g的钠包裹,而后投入到水中,使钠沉入水底与水(足量)反应。该过程中发生反应的离子方程式有___________,充分反应生成的气体体积_________(填“大于”、“小于”或“等于”)2.24L(标准状况下)。
(2)乙同学将足量的铜粉投入到500mL18.4mol/L的浓硫酸中并加热制取SO2,写出该反应的化学方程式__________,生成的SO2物质的量小于4.6mol的原因是_____________。
(3)丙同学向MgCl2、AlCl3的混合溶液中逐滴滴加2mol/L的NaOH溶液,并绘制出沉淀与NaOH溶液体积的关系图像如图,则a=_________,b=________。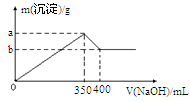
某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从废水中回收硫酸亚铁和金属铜。请根据流程图回答下列问题,完成回收的简单实验方案。
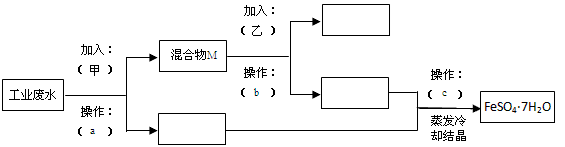
(1)操作a的名称为__________。
(2)加入的甲、乙物质分别为________、_________。
A.浓H2SO4 B.稀H2SO4 C.Fe粉 D.稀HCl
(3)操作c过程中用到的仪器是_______________。
A.坩埚 B.蒸发皿 C.玻璃棒 D.酒精灯
(4)Fe2+具有较强的还原性,易变质,检验产品FeSO4∙7H2O变质的方法是_____________________。
(5)为方便处理废液,检测人员取废水样10mL,做相应如图流程处理。加入加入甲物质质量为4.2g,最终得到FeSO4∙7H2O27.8g(不考虑处理过程中的损失),则原试样中c(Fe2+)=__________。
有一包白色固体粉末,可能含有K2SO4、Na2CO3、NH4Cl、BaCl2、CuSO4中的一种或几种,按以下步骤进行实验:
①取少量固体粉末加到足量水中,得到无色溶液;
②取①中溶液少量继续往其中加入足量稀硫酸,有气泡产生;
③继续向②中的溶液加Ba(NO3)2溶液,有白色沉淀生成;
④取①中溶液少量,加入NaOH溶液并加热,产生刺激性气味的气体,并用湿润的红色石蕊试纸检验气体,试纸变蓝。
根据以上事实判断:
(1)肯定存在的是______________。
(2)肯定不存在的是____________。
(3)不能确定是否存在的是_____________。请简述证明该物质是否存在的实验方案(实验方法、现象、结论)__________________________。
(4)写出上述实验④中产生刺激性气味反应的离子方程式:_____________________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号