氮及其化合物与人们的生活息息相关。
(1)实验室可用铜与稀硝酸反应制取NO,其离子方程式是。为防止环境污染,可用碱液吸溶液完全吸收后得到一种钠盐收氮的氧化物。N O与NO2按物质的量之比1:1被NaOH,该化学方程式是。
O与NO2按物质的量之比1:1被NaOH,该化学方程式是。
(2)已知:① CH4(g) + 4 NO2(g) =" 4" NO(g) + CO2(g) +2 H2O(g)△H=" -574" kJ·mol-1
② CH4(g) + 4 NO(g) =" 2" N2(g) + CO2(g) + 2 H2O(g)△H=" -1160" kJ·mol-1
根据①和②,标准状况下的4.48 L CH4恰好将NO2转化为N2时,△H=。
(3)同温同压下,3.5 L NH3恰好将3.0 LNO和NO2的混合气完全转化为N2,则原混合气中NO和NO2的体积比是 。
(4)向含有1mol HNO3的稀硝酸中逐渐加入铁粉,所得氧化产物a、b与铁粉物质的量关系如图所示。n3 =p= 。
化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求。某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即用表面皿盖好。(已知2KMnO4+16HCl(浓) 2KCl+2MnCl
2KCl+2MnCl 2+5Cl2↑+8H2O)
2+5Cl2↑+8H2O)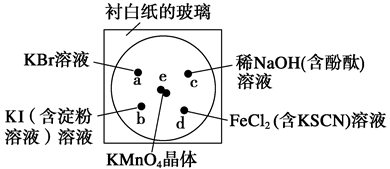
(1)e处反应的离子方程式为_________________________________________。该反应中氧化剂和还原剂的物质的量之比为_______________________。
(2) d处的实验现象:__________________________________________。
(3)c处反应的化学方程式为_________________________________。标准状况下,当有0.224 L Cl2被NaOH溶液吸收后,转移电子的物质的量为__________mol。
(4)通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?__________(填“能”或“不能” ),若能,其氧化性由强到弱的顺序是____________________。
淀粉的化学式是:;油脂在体内水解后的产物是:
体内缺乏易造成甲状腺肿大的元素是易患龋齿的元素的是。
盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
________________
用下列仪器的编号回答问题
①容量瓶②蒸馏烧瓶③分液漏斗 ④量筒⑤烧杯 ⑥托盘天平
④量筒⑤烧杯 ⑥托盘天平
⑴加热时必须垫石棉网的有,
⑵使用时必须检查是否漏水的有,
⑶标有零刻度的有。
观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
( 1)属于离子结构示意图的是 、 (填编号)。
1)属于离子结构示意图的是 、 (填编号)。
(2)性质最稳定的原子是(填写编号,在本小题中下同) ,最容易失去电子的原子是 ,最容易得到电子的原子是 。
(3)A、D两种元素形成的化合物在水溶液中的电离方程式 。
(4)在核电荷数1-18的元素内,列举两个与B核外电子层排布相同的离子,写出离子的符号 、 。
(4分) ①NaCl(S) ②HCl(l) ③Cu ④酒精 ⑤液态醋酸⑥KNO3溶液,填空回答(填序号):以上物质中能导电的是;属于电解质的是;属于非电解质的是;属于弱电解质的是;
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇。已知H2(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解5mol水消耗的能量是______kJ;
(2)写出甲醇燃烧热的热化学方程式:
(3)在容积为 2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况 下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于 300℃);
下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于 300℃);
下列说法正确的是(填序号)
①温度为T2时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=nB/tBmol·L- 1·min-1
1·min-1
②该反应在T1时的平衡常数比T2时的大
③该反应为吸热反应 ④该反应为熵增加的反应
④该反应为熵增加的反应
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中 ,充分反应达到平衡后,若容器内的压强与起始压强之比为0.8,则平衡时甲醇的体积分数为
,充分反应达到平衡后,若容器内的压强与起始压强之比为0.8,则平衡时甲醇的体积分数为
(10分)现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+ n_________p(填“>”“=”“<”)。
n_________p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率_________,B的转化率_________。
(4)若升高温度,则平衡时B、C的浓度之比 将_________。
将_________。
(5)若加入催化剂,平衡时气体混合物的总物质的量_________。 (6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______,而维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______,而维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
(9分)现有A、B、C三种均含同一种元素的无机物,它们之间的转化关系如下图所示(部分产物已略去)。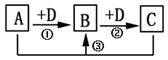
(1)若A、D为非金属单质:
①当M(A)>M(D)时,D为:;
②当M(D)>M(A)时,A为: ;
;
(2)若A为非金属单质,D为金属单质时,A为:;
(3)若D为非金属单质,A、B、C为卤化物时,写出①的化学反应方程式:。
(14分,每空2分)向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:2X(g) Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y的物质的量浓度变化表示的速率为mol/(L·min)。
(2)若上述反应在 甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:①甲v(X)=3. 5mol/(L·min);②乙v(Y)=2mol/(L·min);
甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:①甲v(X)=3. 5mol/(L·min);②乙v(Y)=2mol/(L·min);
③丙v(Z)=4.5mol/(L·min);④丁v(X)=0. 075mol/(L·s)。若其它条件相同,温度不同,则温度由高到低的顺序是(填序号)。
(3)若向达到(1)的平衡体系中充入氩气,则平衡向(填"左"或"右"或"不移动");若向达到(1)的平衡体系中移走部分混合气体,则平衡向(填" 左 " 或 " 右 " 或 " 不移动")。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率⑷与⑴的平衡中的X的转化率相比较。
| A.无法确定 | B.⑷一定大于⑴ |
| C.⑷一定等于⑴ | D.⑷一定小于⑴ |
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,则a、b 、c应该满足的
、c应该满足的 关系为
关系为
。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为。
已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种
①c(Cl-)>c(NH4+ )>c(H+)>c(OH-)②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
)>c(H+)>c(OH-)②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
则:(1)上述关系一定不正确的是(填序号)
(2)若溶液中只有一种溶质,则该溶质为,该溶液中离子浓度的大小关系为(填序号)
(3)若关系③正确,则溶液中溶 质为。
质为。
(4)若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显(填“酸性”、“碱性”、“中性”)。
(5)25℃,pH=a的盐 酸VamL与pH=14-a的氨水VbmL混合,若溶液显中性,则VaVb(填“>”、“<”、“=”、“无法确定”)
酸VamL与pH=14-a的氨水VbmL混合,若溶液显中性,则VaVb(填“>”、“<”、“=”、“无法确定”)
下表是A、B、C、D、E五种有机物的有关信息;
 根据表中信息回答下列问题:
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称叫做;写出在一定条件下,A生成高分子化合物的化学反应方程式_______。
(2) A与氢气发生加成反应后生成分子F,F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n=__________时,这类有机物开始出现同分异构体。
(3) B具有的性质是(填号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:。
(4) E反应能生成(C3H4O2)n的物质,该反应类型为 ;工业生产中使用镍作催化剂。但要求原料中含硫量小于5×10
;工业生产中使用镍作催化剂。但要求原料中含硫量小于5×10
 %,其目的是。
%,其目的是。
(5) 写出由C氧化生成D的化学反应方程式:。