用实验确定某酸HA是弱电解质,两同学的方案是:
甲:①称取一定质量的 配制
配制 的溶液
的溶液 ;
;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各 ;
;
②分别取这两种溶液各 ,加水稀释为
,加水稀释为 ;
;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是_________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH_______1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是_________(多选扣分)
(a)装 溶液的试管中放出
溶液的试管中放出 的速率快;
的速率快;
(b)装HA溶液的试管中放出 的速率快;
的速率快;
(c)两个试管中产生气体速率一样快。
(3)请你再提出一个合理且比较容易进行的方案(药品可任取),作简明扼要表述____________________________________。
在一定温度和压强下,有如下反应:

 ,将
,将 放入一体积可变的密闭容器中,测得容器的起始容积为
放入一体积可变的密闭容器中,测得容器的起始容积为 。经一段时间后,反应达到平衡,测得混合气体的体积为80L,请回答下列问题:
。经一段时间后,反应达到平衡,测得混合气体的体积为80L,请回答下列问题:
(1)达平衡时 的转化率为______________;
的转化率为______________;
(2)若起始时加入 、
、 ,且
,且 ,在同样温度和压强下,反应达到平衡时,测得混合气体的容积为120L。则a、b的值分别为:a=_______,b=_______。
,在同样温度和压强下,反应达到平衡时,测得混合气体的容积为120L。则a、b的值分别为:a=_______,b=_______。
(3)若容器为体积不变的密闭容器,其容积为100L,起始时加入 、
、 和
和 ,反应达平衡时,温度和压强与(2)完全相同,容器内各气体的体积分数也与(2)达平衡时的情况完全相同,则x、y应该满足的关系式为______________,x、z应该满足的关系式为_____________________。
,反应达平衡时,温度和压强与(2)完全相同,容器内各气体的体积分数也与(2)达平衡时的情况完全相同,则x、y应该满足的关系式为______________,x、z应该满足的关系式为_____________________。
(10分)、Ⅰ:(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%一30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是 。
Ⅱ:探究家庭制备次氯酸钠溶液的发生器如右图,原理是用石墨做电极电解饱和食盐水。
(1)若通电后,为使氯气被全部吸收,则电源的a极的名称是 。
(2)电解饱和食盐水的离子方程式为 ,所得的次氯酸钠溶液中加入几滴石蕊试液,观察到的现象是 ,
用离子方程式和简要文字说明理由 。
(10分)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。 (1)向该溶液中加入少量盐酸时,发生反应的离子方程式是 ,
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是 ,
向其中加入少量KOH溶液时,发生反应的离子方程式是 ;
(2)现将0.04 mol·L-1HA溶液和0.02 mol·L-1NaOH溶液等体积混合,得到缓冲溶液。
①若HA为HCN,该溶液显碱性,则溶液 中c(
中c( Na+) c(CN-)(填“<”、“=”或“>”),你得出该结论的依据是 ;
Na+) c(CN-)(填“<”、“=”或“>”),你得出该结论的依据是 ;
②若HA为CH3COOH,该溶液显酸性。溶液中所有的离子按浓度由大到小排列的顺序是 。
(9分)已知:A、B、C、D四种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题。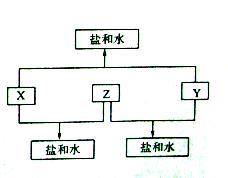
(1)D元素原子的结构示意图为 ;
(2)A、B、C三种元素的原子半径由小到大的顺序为 (用元素符号表示) ;
(3)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式为 ;
(4)A与D两元素的气态氢化物之间可以反应生成一种盐,该盐的水溶液呈
(填“酸”、“碱”或“中”)性;
(5)实验室中,应将X的浓溶液保存在棕色试剂瓶中,其原因是
(用化学方程式表示)。
有机物A的结构简式为 ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。
请回答下列问题:
(1)指出反应的类型:A→C: 。
(2)在A~E五种物质中,互为同分异构体的是 (填代号)。
(3)写出由A生成B的化学方程式
(4)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有的原子有可能都在同一平面的物质是 (填序号)。
(5)C能形成高聚物,该高聚物的结构简为 。
(6)写出D与NaOH溶液共热反应的化学方程式
。
(8分)在一容积固定的密闭容器中,保持一定条件进行以下反应:X(g)+2Y(g) 3Z(g),已知向容器中加入2molX和3molY达到平衡后,生成amolZ。
3Z(g),已知向容器中加入2molX和3molY达到平衡后,生成amolZ。
(1)在相同实验条件下,若在同一容器中改为加入4molX和6molY,达到平衡后,z的物质的量为 。
(2)在相同实验条件下,若在同一容器中改为加入3molX和2molY,若要求平衡时混合气体中Z的体积分数不变,则还需加入Z mol。
(3)在相同的实验条件下,若在同一容器中改为加入0.5molX,则需加 molY, molZ,才能使平衡时Z为0.6amol。
(每空2分,共8分)
(1) 除去NaHCO3溶液中混有的Na2CO3,相应的化学方程式_____________。
(2) 除去Na2CO3固体中混有的NaHCO3,相应的化学方程式_____________。
(3) 除去CO2气体中混有的HCl,相应的离子方程式___________________。
(4) 除去Fe2O3中混有的Al2O3,相应的离子方程式_____________________。
有一包白色粉末可能由K2SO4、NaHCO3、BaCl2、FeCl3、KCl五种物质中的某几种组成,现进行如下实验:
① 将白色粉末加水溶解,得无色溶液。
② 向①中所得的无色溶液中加入NaOH溶液,观察到有白色沉淀A生成,过滤后,向滤液中滴加硝酸酸化的AgNO3溶液,又得到白色沉淀B。
根据上述现象判断:
(1)A的化学式是
(2)B的化学式是
(3)原白色粉末中一定含有 ,可能含有 ,对可能含有的物质,可通过 (填实验名称)进一步检验。
某温度下,在2 L容器中3种物质间进行反应, X、Y、Z的物质的量随时间的变化曲线如图。反应在t1 min时到达平衡,依图所示:
⑴①该反应的化学方程式是_____________________。
②在t1 min时,该反应达到了__________状态,下列可作为判断反应已达到该状态的是__________
| A.X、Y、Z的反应速率相等 |
| B.X、Y的反应速率比为2︰3 |
| C.生成3 mol Y的同时生成1 mol Z |
| D.生成1 mol Z的同时生成2 mol X |

 ⑵①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1 mol氨气分解成氮气和氢气要吸收46 kJ的热量,则至t1 min时,该反应吸收的热量为:__________;在此t1 min时间内,用H2表示反应的平均速率v(H2)= __________。
⑵①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1 mol氨气分解成氮气和氢气要吸收46 kJ的热量,则至t1 min时,该反应吸收的热量为:__________;在此t1 min时间内,用H2表示反应的平均速率v(H2)= __________。 ②两位同学讨论放热反应和吸热反应。甲说加热后才能发生的化学反应是吸热反应,
②两位同学讨论放热反应和吸热反应。甲说加热后才能发生的化学反应是吸热反应, 乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是______同学。
乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是______同学。
(12分)某烃类化合物A的相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢。
(1)A的结构简式为 ;
(2)A中的碳原子是否都处于同一平面? (填“是”或者“不是”);
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
反应②的化学方程式为 ;
C的名称为 ;
E2的结构简式是 ;
④、⑥的反应类型依次是 
 ; 。
; 。
碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸钠俗称 ,等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者 后者(填>、<或=)。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为:
。
(3)现有以下物质:①NaCl晶体 ②熔融的KNO3 ③氨水 ④铝 ⑤Cl2 ⑥酒精(C2H5OH)
请回答下列问题(用序号):
以上物质中能导电的是 ;以上物质中属于强电解质的是 。
(4)SiO2广泛存在自然界中 ,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。写出工业上用石英制备粗硅的化学
,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。写出工业上用石英制备粗硅的化学 反应方程式
反应方程式
已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl 和水的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:(250C时AgCl,Ag2S的溶解度分别为1.5 ×10-4 g, 1.3 × 10-16g)
(1)写出白色固体转化成黑色固体的化学方程式:
(2)白色固体转化成黑色固体的原因是:
250C时,如果取0.1 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因 (用离子方程式表示);
(2)混合溶液中由水电离出的c(H+) 0.1 mol·L-1 NaOH溶液中由水电离出的c(H+);(填>、<、=)
(3)求出混合液中下列算式的计算结果(填具体数字):
c (HA)+c (A-)= mol·L-1;
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH 7 (填>、<、=);
(5)将相同温度下相同浓度的四种盐溶液:
A.NH4HCO3 B.NH4A C.(NH4)2SO4 D.NH4Cl
按pH由大到小的顺序排列 (填序号)