(10分)今有①CH3COOH ②HCl ③H2SO4三种溶液。根据要求回答下列问题:
(1)当它们pH相同时,其物质的量浓度由大到小排列是________________(填序号)
(2)当它们的物质的量浓度相同时,其pH由大到小的顺序是______________(填序号)
(3)中和等量的同一烧碱溶液,需相同的物质的量浓度的①②③三种酸溶液的体积比为
___________________________________。
(4)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱的体积比为_____________________;此时所得到的三种溶液的pH大小关系为______________________。
(10分)
(1)常温下,0.1 mol/L的甲酸和0.1 mol/L的盐酸各100 mL,分别与足量的同浓度氢氧化钾溶液反应所需氢氧化钾溶液的体积前者__________后者(选填“>”、“<”或“=”)。
(2)常温下,0.1 mol/L的甲酸和pH=1的甲酸各100 mL,分别与足量的碳酸氢钠溶液反应,产生的气体前者比后者__________(选填“多”、“少”或“=”)。
(3)在25 ℃条件下,将pH=10的偏铝酸钠溶液稀释100倍,稀释后溶液的pH为(填选项字母,下同)__ ___。
A.10 B.8 C.10~12之间 D.8~10之间
(4) 25 ℃时,向0.1 mol/L的甲酸溶液中加入少量甲酸钠晶体,当晶体溶解后测得溶液pH将____。
A.增大 B.减小 C.不变 D.无法确定
(5) 室温下,向0.1 mol/L的H2SO4中加入足量的锌粒,若想减慢H2产生的速率,但又不影响H2的体积,可以向硫酸溶液中加入__________试剂。
A.硫化钠晶体 B.甲酸钠晶体 C.少量银粉 D.硫酸钠溶液
(8分)在25 ℃时,有pH为x的盐酸和pH为y的NaOH溶液,取Vx L该盐酸同该NaOH溶液中和,需Vy L NaOH溶液。问:
(1)若x+y=14, =___________(填数值);
=___________(填数值);
(2)若x+y=13, =__________(填数值);
=__________(填数值);
(3)若x+y>14, =____________________________________(表达式),
=____________________________________(表达式),
且Vx________Vy(填“>”、“<”或“=”)(题中x≤6,y≥8)。
有一学生在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测:
(1)该学生的操作是 (填“正确的”或“错误的”),其理由是 。
(2)若用此方法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 ,原因是 。
(3)该学生以上述方式测定下列溶液的pH,无误差的是( )
| A.NaOH | B.CH3COONa | C.NaCl | D.NaHSO4 |
一定温度下,有a.盐酸、b.硫酸、c.醋酸三种酸(用a、b、c回答)。
(1)当其物质的量浓度相同时。c(H+)由大到小的顺序是 ,pH由大到小的顺序是 。
(2)同体积、同物质的量浓度的三种酸溶液,中和NaOH的能力由大到小的顺序是 。
(3)当c(H+)相同时,物质的量浓度由大到小的顺序为 。
(4)当pH相同、体积相同时,分别加入足量锌,相同状况下产生的气体体积由大到小的顺序为 。
(普通班)(13分)(1)常温下, CH3COONa溶液呈 性,用离子方程式解释其原因 。
(2)室温下,若将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示。
①NH3·H2O的电离方程式是 。
②b点所示溶液中的溶质是 。
③c点所示溶液中,离子浓度从大到小的关系为 ,在该溶液中存在多种守恒关系,其中c(NH4+)+c(H+)= (用离子浓度表示)。
水溶液中存在多种平衡,请根据所学化学知识回答下列问题:
(1)在浓度均为0.1mol/L①CH3COONH4 ②NH4HSO4 ③NH3.H2O ④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为 (填序号)
(2)浓度均为0.1 mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。
(3)恒温下,向pH=6的蒸馏水中加入2.3g金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH= 。
(1)FeCl3的水溶液呈____(填“酸”、“中”、“碱”)性,实验室在配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以____(填“促进”、“抑制”)其水解。
(2)氯化铝溶于水的反应(用离子方程式表示):_______________________;把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是 。
(3)物质的量浓度均为0.10 mol·L-1的三种溶液:a.CH3COONa b.Na2CO3 c.NaHCO3
pH由小到大排列的顺序是 (用编号填写)。
(4)NaHCO3溶液显 性,原因是_______________________(用离子方程式表示)。
(1)25℃时,pH=12.0的KOH溶液中,由水电离出的c(OH-)=_______mol/L;pH=12.0的K2CO3溶液中,由水电离出来的c(OH-)=_______mol/L。
(2)常温下0.1mol·L-1 CH3COONa溶液PH=8
①用离子方程式表示CH3COONa溶液PH=8的原因: 。
②按物质的量浓度由大到小顺序排列该溶液中各种微粒(水分子除外) 。
(3)FeCl3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): 。
若100 ℃时纯水电离出的H+浓度为1.0×10-6 mol·L-1,则此时KW= ,c(OH-)= ;25 ℃时的c(H+)=10-2 mol·L-1的硫酸溶液和c(H+)=10-12 mol·L-1的氢氧化钠溶液温度均升高到100 ℃,H+浓度分别是多少?
(1)某温度时,水的离子积Kw=1×10-13,则该温度_________25℃(填“>”、“<”或“=”)。在此温度下,某溶液中由水电离出来的H+浓度为1×10-10 mol•L-1,则该溶液的pH可能为________;
(2)若温度为25℃时,体积为Va、pH=a的H2SO4与体积为Vb、pH=b的NaOH混合,恰好中和,此溶液中各种离子的浓度由大到小的排列顺序是_____________。
(10分)(1)同浓度的下列溶液:①NH4Al(SO4)2 ②NH4Cl ③CH3COONH4,其中c(NH4+) 由小到大的顺序是 (填序号,下同)。
(2)同浓度的下列溶液:①(NH4)2SO4 ②NH4Cl ③Na2CO3 ④NaHCO3,其中pH 由大到小的顺序是 。
(3)现有下列物质①NaCl晶体 ②液态SO2 ③纯醋酸 ④硫酸钡固体⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KCl ⑧NaOH溶液 请用以上物质回答下列问题。
属于强电解质且在上述状态下能导电的是 ;
属于弱电解质的是 ;
属于非电解质,但溶于水后的水溶液能导电的是 。
现有浓度均为0.1 mol·L-1的下列溶液:①盐酸 ②醋酸 ③氢氧化钠 ④氯化铵 ⑤硫酸氢铵 ⑥氨水,请回答下列问题:
(1)已知t ℃时,Kw=1×10-13,则t ℃(填“>”“<”或“=”)____________25 ℃。
(2)②③④三种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_________。
(3)④⑤⑥四种溶液中NH4+浓度由大到小的顺序是(填序号)__________________。
(4)常温下,将①和③按体积比2:1混合后,溶液的pH约为_______(已知lg3 = 0.5)。
已知水在25℃和95℃时,其电离平衡曲线如下图所示:
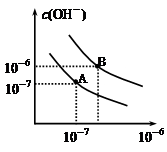
(1)则95℃时水的电离平衡曲线应为 (填“A”或“B”)。
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,所得溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为
(3)95℃时,若1体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是(用含a、b的等式表示):