下列是初中化学部分重要的实验或实验装置。请按要求填空: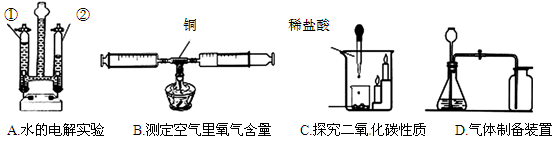
(1)A实验玻璃管②中产生的气体是 ;
(2)B实验如果实验数据小于21%,可能原因是 、 (写出两点);
(3)C实验说明二氧化碳具有的性质是 、 ;
(4)写出用D装置制取二氧化碳气体的化学方程式 。
20℃时,将等质量的甲、乙两种固体物质,分别加人到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3。请结合图示回答下列问题: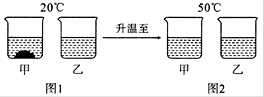
(1)图1中一定为饱和溶液的是 _______。
(2)图2中甲、乙两溶液中溶质质量分数的大小关系为________________。
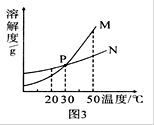
(3)图3中表示乙的溶解度曲线是________;
在实验课中,各小组作了如下实验:
| 实验编号 |
1 |
2 |
3 |
4 |
| 实验操作 |
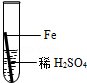 |
 |
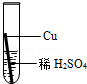 |
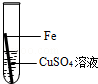 |
实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁…,应该可以从中提炼出铁和铜.经思考后,他设计了如图所示的实验,并设法使滤液甲和乙所含的溶质相同.
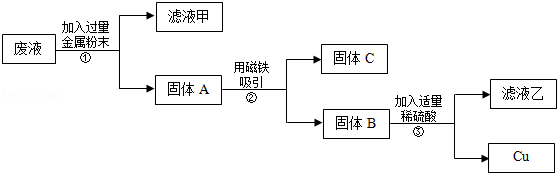
则固体C是,操作③的名称是,实验中所加的过量金属粉末是.
碘是人体必须的微量元素,海带因富含碘元素而成为补碘的常用食物之一.小李想设计实验验证海带中含有碘元素.他查阅了相关资料,得到以下信息:
①碘化钠(
)与氯化钠性质相似,两者的溶液都是盐溶液,碘化银为黄色难溶于水的固体.
②工业上将适量氯气通人无色碘化钠溶液就能置换出单质碘,溶液变为棕黄色.
③少量碘((
)溶于水的溶液,能使淀粉溶液变蓝,碘的化合物不能使淀粉溶液变蓝.
④灼烧海带后残留的灰烬中含有可溶性碘化钠、氯化钠等化合物.
小李的实验步骤如下:
将海带灰用蒸馏水充分浸泡后过滤,得滤液;然后用以下3种方法,去检验海带灰中是否含有碘元素.
方法一:取滤液,通入适量氯气后与淀粉糊混合,观察是否变蓝.
方法二:取滤液,通入适量的氯气,观察溶液有无颜色变化.
方法三:取滤液,和淀粉糊混合,观察是否变蓝.
请回答下列问题:
(1)氯气和碘化钠反应的化学方程式:.
(2)上述3种方法中,方法是一定不可行的,说出不可行的理由:。
(3)取滤液,滴人硝酸银溶液,若观察到,则证明滤液中含碘离子.
有三种元素
、
、
,已知
元素的离子
结构示意图为: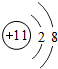 ;
元素原子核内只有一个质子,
元素和
元素组成一种氧化物,该氧化物是常用的溶剂.
;
元素原子核内只有一个质子,
元素和
元素组成一种氧化物,该氧化物是常用的溶剂.
(1)
、
、
三种元素可组成一种化合物
,
的化学式是;这种化合物的俗名是(只填一种);
(2)化合物
溶于水所得溶液的
(填"大于"、"小于"或"等于"):化合物
曝露在空气中容易吸收水分,表面
(3)将一种硫酸盐溶液加入到化合物 的溶液中发生反应,有一种蓝色的沉淀生成,写出这一反应的化学方程式:.
化学使世界变得绚丽多彩.如图是物质之间发生化学反应的颜色变化.
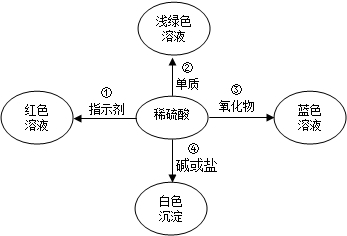
(1)请你在编号②、③处各填入一种物质.②是;③是;
(2)根据上图可以总结出稀硫酸的五个化学性质.请你写出编号①稀硫酸的化学性质.
(3)若编号④的物质是盐.请你写出符合编号④的一个化学方程式:,反应类型是.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应。
(1)配制100g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的 盘,称量其质量。然后按需要添加砝码、移动游码,再将氢氧化钠固体加入烧杯中,直至天平平衡。该步骤中用烧杯而不用纸称量氢氧化钠的原因是 。
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(2)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
【实验方案】
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且最终小至小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
①用pH试纸测定NaOH溶液pH时,正确的操作是: 。
②简述强调“测得的pH小于7”的理由: 。
方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。该组同学在没使用温度计的情况下,通过下图所示装置完成了实验。则该组同学根据 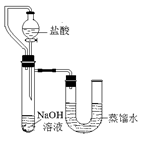
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(主要含有FeCl2和CuCl2)处理和资源回收的过程简述如下:
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
试回答下列问题:
⑴过程I加入铁屑的主要作用是 ;试写出其对应的化学方程式: ;
⑵从固体中分离出铜需采用的方法是 ;
⑶滤液中溶质主要为 (写出化学式);已知过程II生成的最终产物为Fe(OH)3,则Fe(OH)2与氧气和水反应的化学方程式为: 。
A、B、C、D、E、F、G、H均为初中化学常见物质,其中C、D、F为单质,其余为化合物,B、E为气体,反应①是重要的工业反应,下图是它们之间的相互转化关系。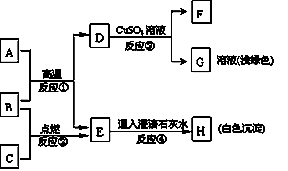
请回答:
⑴写化学式:A 、E 、G ;
⑵写出反应①、④的化学方程式:
反应①________________________ ______________
反应④______________________________________ 。
利用铝土矿(只考虑含Al2O3及Fe2O3)生产Al的工艺流程如下,请回答下列问题:
【查阅资料】:1、铝土矿中Al2O3可以和NaOH溶液反应,反应的化学方程式为:
Al2O3 + 2NaOH ="=" 2NaAlO2 + 2H2O;2、Fe2O3不和NaOH溶液反应。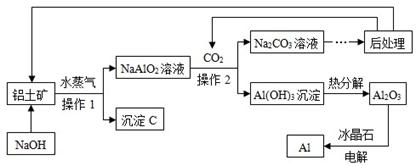
(1)工业生产中,要将铝土矿细磨预处理,目的是 ;
(2)沉淀C的化学式是 ;
(3)操作1、操作2的名称是 ,实验室完成此操作时,需要的玻璃仪器的是玻璃棒、烧杯和 ;
(4)此工艺中,可循环使用的物质是CO2、H2O和 ;(填化学式)
(5)电解Al2O3的化学方程式为 ;
(6)NaAlO2溶液中通入CO2反应的化学方程式是 。
右图表示某些物质间转化关系(反应条件和部分产物已省略)。其中A、E为固体氧化物,且A为黑色粉末;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属。请回答下列问题: 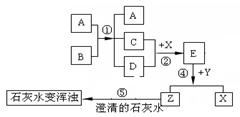
(1)反应①中A物质的作用是 ;
(2)反应③、④的化学方程式:③ ;④ ;
(3)在日常生活中为防止反应②的发生,可采取的措施是 (写一点即可);
下列物质由H、C、O、Fe四种元素中的一种或几种组成,它们是初中化学常见的物质。
(1)若某单质为最清洁的燃料,它的化学式是 。
(2)若某化合物能燃烧,则化合物中一定含有的元素是 。
(3)甲、乙、丙三种物质在一定条件下存在如下转化关系(图中已略去部分物质)。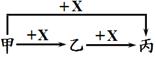
①若只有甲为固体,其他物质均为气体,则X是 ,乙→丙反应的化学方程式是 。
②若甲、乙、丙均为固体,且甲为红色,乙和丙为黑色,在甲与X 生成乙的反应中甲与X的质量比为120︰7。甲→丙反应的化学方程式是 ,甲→乙反应的化学方程式是 。
NaCl 和KNO3在不同温度时的溶解度如下,回答下列问题。
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
| 溶解度/g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
| KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
(1)10℃时,在100 g水里溶解_________g KNO3时,溶液恰好达到饱和状态。
(2)右图为NaCl 和KNO3的溶解度曲线,则表示NaCl的溶解度曲线是_________(填“甲”或“乙”);其中温度t的范围可能在________(填字母序号)。 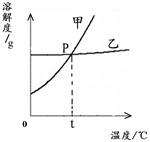
A.10℃~20℃ B.20℃~30℃
C.30℃~40℃ D.40℃~50℃
(3)10℃时,分别在100 g水中加入35 g NaCl 和KNO3固体,加热到60℃时,NaCl溶液为__________(填“饱和”或“不饱和”)溶液。加热前后,有关两溶液的说法正确的是____________(填字母序号)。
A.10℃时,两溶液中溶质的质量分数相同
B.60℃时,两溶液中溶质的质量分数相同
C.加热前后,NaCl溶液中溶质的质量分数不变
D.加热前后,KNO3溶液中溶质的质量分数不变
理解、掌握质量守恒定律是学好化学的基础。
(1)某同学按右图装置对质量守恒定律进行实验探究,观察到反应后天平不平衡,请你用质量守恒定律解释其原因是 ;发生反应的化学方程式是 。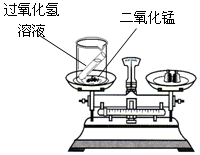
(2)由质量守恒定律可知,在化学反应前后,一定不变的
是 (填序号)。
①分子种类②原子种类③分子数目④原子数目⑤物质质量⑥元素种类
(3)4.14玉树地震给当地人民造成巨大损失。为防止灾后发生疫情,必须对灾区进行消毒,其中的一种消毒剂是漂白粉,它的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙能与水和二氧化碳发生反应,请完成这个反应的化学方程式:
Ca(ClO)2 +CO2 + H2O=CaCO3↓+2 。
(4)A、B、C三种物质各15 g,它们化合时只生成30 g新物质D。若增加10 g A,则反应停止后,原反应物中只剩余B。根据上述条件推断下列说法中正确的是 (填字母)。
A.该反应中,B是催化剂
B.第一次反应停止后,C剩余9 g
C.第二次反应后,D的质量为50 g
D.反应中A和B的质量比是5∶2
E.反应中A和C的质量比是5∶2