硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO等,工艺流程图如下:
【查阅资料】①一般情况下,难溶性碱受热易分解,生成对应的金属氧化物和水;
②Mg(OH)2和Zn(OH)2开始沉淀和沉淀完全时的pH如下表所示:
| |
Mg(OH)2 |
Zn(OH)2 |
| 开始沉淀的pH |
10.4 |
6.4 |
| 沉淀完全的pH |
12.4 |
8.0 |
| 开始溶解的pH |
—— |
10.5 |
根据上图回答下列问题:
(1)将菱锌矿研磨成粉的目的是 ;
(2)针铁矿的组成元素是Fe、O和H,相对分子质量是89,针铁矿中铁原子数︰氧原子数︰氢原子数= ;(提示:氢原子数目小于氧原子数目)
(3)“滤液4”之前加入锌粉的目的是 ;
(4)工业上从“滤液3”制取MgO过程中,合适的反应物是 (选填序号);
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(5)完成这个流程中发生的化学反应方程式:
4Fe(OH)2+Ca(ClO)2+2 =4Fe(OH)3+CaCl2,
某化学兴趣小组设计了一组有关气球变化的实验,三套装置如下图: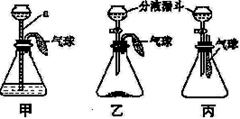
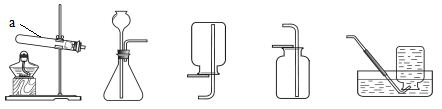
(1)甲装置:若该装置的气密性良好,则向a中加水会看到 。
(2)乙装置:若锥形瓶中装有生石灰,由分液漏斗加入少量水,则气球胀大的主要原因是_________。
(3)丙装置:若锥形瓶中盛满CO2,通过发生化学变化使气球胀大,且生成物之一属于盐类,则分液漏斗中的液体可以是________。该反应的化学方程式为 。
氯气(Cl2)是黄绿色气体,溶于水时部分以Cl2分子存在于溶液中,部分与水反应Cl2 + H2O =" HCl" + HClO。产物中,次氯酸(HClO)是一种弱酸。氯气溶于水所得溶液称为氯水,它具有很强的漂白性。把品红试纸(染有品红颜料的滤纸)放入氯水中,品红试纸褪色。晓红同学对“氯水使品红试纸褪色”产生浓厚兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】猜想1:氯水中的水使品红试纸褪色;
猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;
猜想4:氯水中的__________使品红试纸褪色。
【实验探究】
| 实验操作 |
实验现象 |
结论 |
| ①把品红试纸放入水中 |
|
猜想1不成立 |
| ② |
试纸不褪色 |
猜想2不成立 |
| ③ |
试纸不褪色 |
猜想3不成立 |
【结论】学习小组通过讨论,找到了氯水中使品红试纸褪色的物质。
【反思】向氯水中滴加几滴紫色石蕊试液,会观察到的现象是 。
【拓展】铁能在氯气中燃烧生成氯化铁,请写出该反应的化学方程式 。
溶液是生产生活中常见的物质,依据相关信息回答问题:
资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如下表所示:
| 温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
| 溶解度/g |
21 |
32 |
46 |
64 |
86 |
110 |
138 |
(1)农业上,硝酸钾用作水溶性肥料,为作物补充氮和钾元素。硝酸钾溶液中的溶质是______。
(2)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。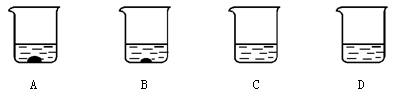
①(填字母序号) 中盛的一定是饱和溶液。
②使B烧杯的溶液升温至50℃时,溶液的质量为 g。
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是 (填字母序号)。
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(3)工业上利用电解饱和氯化钠溶液可制得重要化工产品氢氧化钠。氢氧化钠溶液可用于治理含二氧化硫的废气并回收二氧化硫,反应的主要流程如下: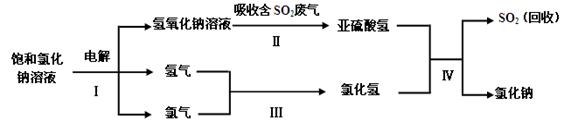
①实际生产中,在一定温度下,配制100t溶质的质量分数为25%的饱和氯化钠溶液,需水的质量为 t。
②以上流程中,可循环使用的物质是 。
③亚硫酸氢钠(NaHSO3)中硫元素的质量分数为 %(计算结果精确到0.1%)。
(9分)我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下: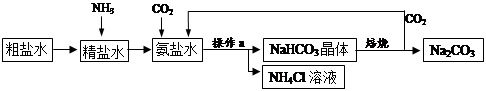
【资料】四种盐在不同温度下的溶解度表
| |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
| NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
| NH4HCO3 |
15.8 |
21.0 |
27.0 |
—— |
—— |
| NaHCO3 |
8.1 |
9.6 |
11.1 |
12.7 |
—— |
| NH4Cl |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
⑴检验粗盐水是否为硬水的方法是加入 ;
⑵操作a是 ,生产流程中被循环利用的物质是 ;
⑶在精盐水中先通入NH3,使溶液呈 性,再通入CO2,有利于对CO2的吸收;
⑷氨盐水中通入二氧化碳后,在常温条件下,易析出NaHCO3晶体而不析出NH4Cl晶体的可能原因是 ;
⑸粗盐水中主要含有CaCl2、MgCl2等杂质,工业上常加入下列物质除杂、精制,则加入下列三种试剂合理的顺序为 (填序号);
A.适量的盐酸 B.稍过量的Na2CO3溶液 C.稍过量的Ca(OH)2溶液
⑹副产品NH4Cl可做 肥,若加入氢氧化钠加热,反应的化学方程式为 。
构建知识网络是一种重要的学习方法。下图是关于X物质化学性质的知识网络,“——”表示相连的两种物质能发生反应,“ ”表示一种物质转化成另一种物质,X的水溶液遇硝酸钡溶液产生不溶于硝酸的白色沉淀,D是生活中常见金属,与X反应产生气泡,溶液变浅绿色,A、B、C、D属于不同类别的物质。完善这个知识网络:
”表示一种物质转化成另一种物质,X的水溶液遇硝酸钡溶液产生不溶于硝酸的白色沉淀,D是生活中常见金属,与X反应产生气泡,溶液变浅绿色,A、B、C、D属于不同类别的物质。完善这个知识网络: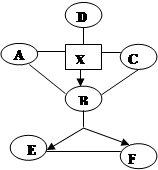
(1) 写出A、B的化学式: A ;B 。
(2) 根据自己得出的知识网络写出一个复分解反应
化学方程式:
(3)写出E与F反应的反应化学方程式:
____________________________________
有一包白色粉末,可能含有碳酸钙、碳酸钠和氢氧化钠中的一种或几种,某学生为了确定其组成,作如下实验,请根据下列实验现象进行推断:
(1)在试管中加入少量粉末,注入足量的蒸馏水充分振荡,得到无色透明溶液;
(2)取(1)中少量溶液,滴入稀盐酸,有气泡产生;
(3)取(1)中少量溶液,滴入石蕊,溶液变蓝色;
则该白色粉末一定含有________,可能含有________。
(10本溪20).(3分)某化工厂排放的废液中只含有ZnCl2和CuCl2两种溶质,为回收金属Cu并得到 ZnCI2固体,化学小组的同学们设计并进行了如下实验: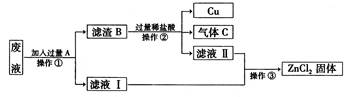
(1)滤液I中的溶质是 ;
(2)B中含有的物质是 ;
(3)操作③名称是 。
甲同学对有关盐的知识进行了以下的整理。
(1)上述盐的排列是依据 顺序归纳整理的。
(2)上述盐因组成上相似而具有某些共同的化学性质,如都能与BaCl2溶液反应生成硫酸钡沉淀,该反应的化学方程式为 (任选其中一种盐即可)。
(3)甲同学通过查阅资料,发现许多反应都有盐类物质生成。他将这些知识间相互关系整理成右图,请将右图补充完整a ,b 。
(4)乙同学提出可用如图指导进行物质的制备:请写出2个有关硫酸亚铁生成的化学反应方程式。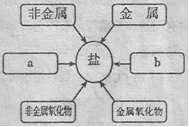
答: ;
。
(6分)某化学实验小组实验结束时,将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,为回收有关金属和盐,同学们设计了如下实验方案: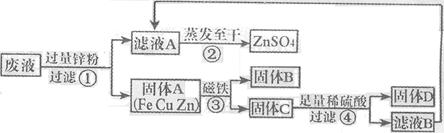
试回答:
(1)步骤①中锌粉必须过量的原因是 。
(2)写出步骤①中任一反应的化学方程式 。
(3)要检验步骤④中加入的稀硫酸是否足量的方法是
。
(4)若实验过程中的物质损失可以忽略,最终所得硫酸锌的质量 (填“>”、“<”或“=”)原废液中硫酸锌的质量。要计算该废液中硫酸铜质量,必须要称量 的质量。
、
、
、
、
、
都是初中化学中常见的物质。它们的转化关系是:

请回答下列问题:
(1)检验集气瓶内气体甲的操作方法是。
(2)在反应②③中,固体
起作用。
(3)写出反应①和④的化学方程式:
①;④。
(4)溶液
的溶质是。
一包白色粉末,由
、
、
、
、
中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液。则原白色粉末中一定不含有。
(2)取实验(1)滤出的白以沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体。则原白色粉末中一定含有。根据上述实验可推断:原白色粉末的组成有种可能。为进一步探究原白色粉末的组成,取实验(1)得到的滤液,向其中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有。
已知:①金属钠是一种活泼的金属,与水反应生成氧氧化钠和氢气;②难溶于水的碱受热分解生成相应的氧化物和水。A、B、C、D、E、F、G、H是初中化学中常见的物质,甲、乙、丙是三种金属。其中甲最活泼,乙是红色金属,丙能被磁铁吸引。各物质间相互转化关系如下图:
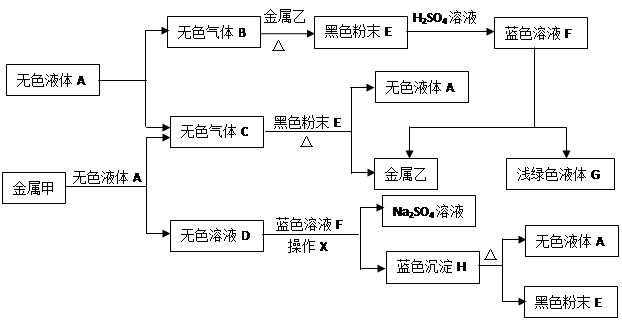
请回答下列问题:
(1)写出A、E、G的化学式:A ,E,G。
(2)操作X的名称是。
(3)①无色溶液D与蓝色溶液F反应的化学方程式为;
②金属甲与无色液体A反应的化学方程式为,该反应的基本类型;
③蓝色沉淀H受热分解反应的化学方程式为。
(4)甲、乙、丙三种金属的活动性由强到弱的顺序是,无色气体C在点燃或加热前必须进行的操作是。
金属材料、无机非金属材料、有机高分子材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
(1)金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于变化。钢铁是制造轮船的主要金属材料,船身外通常装上一定数目比铁更活泼的金属块以防止腐蚀,该金属块可以选择(选填"铜块"、"锌块"、"铅块")。
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:

请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,其基本反应类型为。
②实验室常采用操作进行沉淀分离。
③生产高纯碳酸钙时,选择"220℃恒温干燥"而不选择"灼烧"的原因是。
④高纯氧化钙生产过程中,"干燥"的主要目的是为了防止(用化学方程式表示)。
(3)有机高分子材料"玉米塑料",因其可降解被广泛用来替代一次性泡沫塑料,"玉米塑料"的使用可减少污染。20世纪30年代,尼龙因其抽成细丝极像蚕丝而被推向世界,生活中可采用方法区分尼龙和蚕丝。
(7分)下图是对生成氯化钠反应关系的归纳与整理。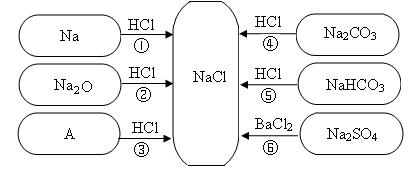
请回答下列问题:
(1)物质A是常见的碱,写出A的化学式:______。
(2)写出反应①的化学方程式:___________________。
(3)说出NaHC03在医疗上的一种用途:______________ 。
(4)反应③、④、⑤、⑥能够进行的原因是_______________。
(5)实验室配制200g 8%的NaCl溶液,需要水的质量是___________g,配制过程中为了加快NaCl的溶解,可以采取的措施是_____________。