江苏省金坛市5月初三教学情况调研考试化学试卷
下列厨房里烧鸡蛋汤的操作中,发生化学变化的是
| A.打破蛋壳倒入碗中 | B.加水搅拌 | C.下锅烧开 | D.盛入碗中 |
将下列四种家庭常用的调味品分别放入足量水中,不能形成溶液的是
| A.花生油 | B.味精 | C.食盐 | D.蔗糖 |
下列物质的化学名称与俗名,对应错误的是
| A.汞——水银 | B.乙醇——酒精 |
| C.碳酸氢钠——纯碱 | D.氢氧化钠——烧碱 |
下列实验现象的描述正确的是
| A.高锰酸钾溶液中通入二氧化硫后褪色 | B.木炭在空气中燃烧生成黑色固体 |
| C.点燃羊毛纤维能闻到烧纸气味 | D.米汤中滴加碘酒呈红色 |
下图所示的化学实验基本操作正确的是



| A.点燃酒精灯 | B.称量NaCl | C.向试管中滴加液体 | D.取用液体药品 |
下列化学符号中数字“2”表示的意义不正确的是
| A.Ca2+:一个钙离子带2个单位正电荷 | B.SO2:二氧化硫含2个氧原子 |
| C.2HCl:2个氯化氢分子 | D. :氧化锌中锌元素化合价为+2 :氧化锌中锌元素化合价为+2 |
工业明胶中含有毒的重铬酸钠(Na2CrO4),其中Cr元素的化合价为
| A.+1价 | B.+2价 | C.+4价 | D.+6价 |
化学与生活密切相关,生活中的下列做法不合理的是
| A.菜刀用后洗净擦干 | B.用活性炭吸附冰箱中的异味 |
| C.坐公交车代替开私家车 | D.管道天然气泄漏,打开电灯检查 |
人体中化学元素含量的多少会直接影响人体健康。下列人体所缺元素与引起的健康问题关系错误的是
| A.缺钙会引起侏儒症 | B.缺碘会引起甲状腺疾病 |
| C.缺铁钴易得贫血症 | D.缺锌会使儿童发育停滞 |
对生活中下列现象的解释错误的是
| |
现 象 |
解 释 |
| A |
冰糖在热水中比冷水中溶解得快 |
温度升高,分子运动加快 |
| B |
汽油洗涤油污 |
汽油具有乳化作用 |
| C |
硫酸溶液能导电 |
溶液中存在自由移动的H+和SO42- |
| D |
二氧化碳和水生成碳酸 |
分子本身改变,生成新的分子 |
金坛是我国著名的绿茶产地,“金坛青峰”“金坛雀舌”等众多品牌的绿茶香飘四海。茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压、提高记忆力、保护神经细胞等。下列有关茶氨酸的说法中错误的是
A.茶氨酸由C、H、O、N四种原子构成 B.茶氨酸由C、H、O、N四种元素组成
C.茶氨酸中氢元素与氮元素的质量比为1:2 D.茶氨酸中碳元素质量分数最大
4月12日,云南省保山市隆阳区永昌街道呢喃山发生森林火灾,起火原因系当地村民上坟烧纸引起。下列说法错误的是
| A.森林为火灾提供可燃物 | B.烧着的纸提高了草木的着火点 |
| C.大风为燃烧提供了充足的氧气 | D.用水浇是降低燃烧物的温度 |
二甲醚(CH3OCH3)可由一氧化碳和物质X在一定的条件下制得。反应的化学方程式为:2CO+4X ===CH3OCH3+H2O,则X的化学式为
| A.C2H5OH | B.H2O2 | C.H2 | D.C2H4 |
下列说法正确的是
| A.单质是由一种元素组成的,由多种元素组成的物质一定不是单质 |
| B.浓盐酸长时间露至在空气中,溶质质量分数减小,原因是溶剂增加 |
| C.中和反应后溶液酸碱性消失,纯碱和盐酸混合后呈中性,发生了中和反应 |
| D.当溶液中有晶体析出时,其溶质质量减小,所以溶质的质量分数一定减小 |
实验考查中小明配制了50g15%的食盐水,经检测质量分数偏高,可能原因是
| A.食盐中含有不溶杂质 | B.取水时俯视读数 |
| C.称量时物码放反 | D.转移至细口瓶时洒出 |
初中化学知识中有许多关系,下列各组不符合甲与乙、丙是包含关系的是
| A.甲:磷单质乙、丙:红磷、白磷 |
| B.甲:分子构成的物质乙、丙:氨气、冰水 |
| C.甲:有机化合物乙、丙:甲烷、淀粉 |
| D.甲:“三酸两碱”乙、丙:硝酸、熟石灰 |
下列转化不能一步完成的是
| A.Cu→Cu(NO3)2 | B.HCl→FeCl3 | C.CaCO3→Ca(OH)2 | D.C6H12O6→C |
下列实验中,所用试剂或方法正确的是
| A.除去CaO中少量CaCO3:加入适量盐酸后过滤 |
| B.证明碳酸钠溶液中含氢氧化钠:加过量氯化钙溶液后加酚酞,观察是否变红 |
| C.检验集气瓶中的氧气已收满:将带火星的木条插到集气瓶底部,观察木条是否立刻剧烈燃烧 |
| D.测定某溶液的酸碱度:取少量样品,滴加紫色石蕊试液 |
质量法是化学实验中测定物质组成时常用的一种方法。现有11 g气体,经测含碳元素3g,其余都是氧元素。下列有关说法正确的是
| A.气体可能是CO2和O2的混合物 |
| B.气体可能是CO和CO2的混合物 |
| C.气体组成有4种情况 |
| D.若气体由三物质组成,则三物质质量比可能是7:3:4 |
(4分)从C、H、O、Cu、Na五种元素中选择,写出符合下列要求的化学式:
⑴水电解负极产生的气体 ;⑵最简单的有机物 ;
⑶实验室制氧气的氧化物 ;⑷难溶于水的碱 。
(4分) 用“>”“<”“=”号填空
⑴铜块硬度 青铜硬度;
⑵葡萄糖中元素种类 油脂中元素种类;
⑶20℃饱和石灰水浓度 50℃饱和石灰水浓度;
⑷加入铁钉前硫酸铜溶液质量 加入铁钉后溶液质量。
(6分)下图是A、B、C三种固体物质的溶解度曲线图,结合图示回答下列问题:
⑴60℃时B的溶解度为 ;
⑵10℃时A、B、C三固体溶解度由大到小次序是 ;
⑶P点是70℃时A的 溶液(填“饱和”或“不饱和”);
⑷70℃A的饱和溶液150g降温至60℃,析出晶体 g;
⑸室温下将盛有C的饱和溶液的试管放入盛水的烧杯中,
再向烧杯内的水中加入一定量的氢氧化钠固体并搅拌,
试管内可以观察到的现象是 ;
⑹当A中混有少量B时,可用 方法提纯A。
(4分)A、B、C、D、E为初中五种常见物质, 其中A是生活中最常见液体, B、D是气体,只有E含金属元素,B是常见单质(反应条件与其他物质均已略去)。“→”表示按方向一步转化,“——”表示两种物质间可以发生反应,所有反应都是初中常见反应。
⑴写出物质化学式:A: ,C: ;
⑵写出化学方程式:D+E 。
现将一定质量含氢氧化钠的碳酸钠固体中加入100g水充分溶解,向该溶液中逐滴加入溶质质量分数为10%的盐酸,生成气体的质量与加入盐酸的质量关系如图所示。
⑴当盐酸质量为150g时,溶液中溶质化学式为 ;
⑵求固体中碳酸钠的质量?(写出计算过程,保留一位小数)
⑶当充分反应后溶液中氯化钠的质量为 g。
(9分)我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下: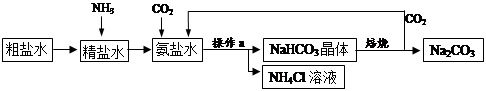
【资料】四种盐在不同温度下的溶解度表
| |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
| NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
| NH4HCO3 |
15.8 |
21.0 |
27.0 |
—— |
—— |
| NaHCO3 |
8.1 |
9.6 |
11.1 |
12.7 |
—— |
| NH4Cl |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
⑴检验粗盐水是否为硬水的方法是加入 ;
⑵操作a是 ,生产流程中被循环利用的物质是 ;
⑶在精盐水中先通入NH3,使溶液呈 性,再通入CO2,有利于对CO2的吸收;
⑷氨盐水中通入二氧化碳后,在常温条件下,易析出NaHCO3晶体而不析出NH4Cl晶体的可能原因是 ;
⑸粗盐水中主要含有CaCl2、MgCl2等杂质,工业上常加入下列物质除杂、精制,则加入下列三种试剂合理的顺序为 (填序号);
A.适量的盐酸 B.稍过量的Na2CO3溶液 C.稍过量的Ca(OH)2溶液
⑹副产品NH4Cl可做 肥,若加入氢氧化钠加热,反应的化学方程式为 。
(6分)某小组设计了下图所示的实验装置。
⑴当打开K1、关闭K2时,利用装置,可进行的实验是 (填字母)。
a.锌与稀硫酸反应制取氢气 b.二氧化锰与双氧水制取氧气
⑵当打开K2、关闭K1时,实验室可以利用A、B、C、D装置制得二氧化碳并进行相关实验。
①A中反应的化学方程式 ;
②若原氢氧化钠溶液中滴加酚酞,气体通入并充分反应后溶液颜色 ;
A.始终呈红色 B.由红变为无色 C.变为蓝色 D.变为紫色
③当C中液体大部分排出时,装置D中反应的化学方程式为 。
(6分)不锈钢是在铁中加入铬镍,改变内部结构,从而起到防锈作用。小明为了探究铬(Cr)与镁、铜的活动性强弱关系,进行如下探究活动:
【提出猜想】三种金属在金属活动性顺序中的相对位置关系:
①Mg Cu Cr ②Mg Cr Cu ③
【查阅资料】铬能被空气中的氧气氧化成Cr2O3,也能溶于稀盐酸生成蓝色CrCl2溶液。
【实验过程】
(1)取相同的三种金属薄片,用砂纸打磨;
(2)把三金属薄片分别与等质量10%的盐酸混合,观察到如下现象:
铬表面缓慢产生气泡,溶液变成蓝色;铜表面无明显变化;镁表面较快产生气泡。
【实验结论】猜想 正确(填猜想序号)。
【实验讨论】
⑴铬与盐酸反应的化学方程式是 。
⑵小明还想用硫酸铜溶液代替上述实验中的盐酸,在两试管中分别与镁片、铬片混合得出三种金属的活动性关系。小花认为不可行,理由是 。
【拓展迁移】若只有一支盛有少量稀盐酸的试管,只需合理安排金属片的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铬、镁、铜这三种金属的活动性顺序,则三金属片的插入顺序为 。
(10分)为了测定某样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不溶于水和酸),某兴趣小组的同学进行了如下的实验,请你参与过程分析。
【查阅资料】
1.草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为H2C2O4  CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
2.碱石灰能吸收二氧化碳和水蒸气
【实验设计及操作】用下图所示装置进行实验: 
【问题讨论】
⑴装药品前应先 ,实验中观察到E中现象是:固体颜色 ;
⑵进入E中的气体是纯净、干燥的CO,则B、C、D中依次是 (填序号)。
① 浓硫酸、石灰水、氢氧化钠溶液 ② 石灰水、氢氧化钠溶液、浓硫酸
③ 氢氧化钠溶液、石灰水、浓硫酸
⑶ G的作用是 ;E中反应的化学方程式是 ;
⑷当E中固体完全反应后,先熄灭 灯(A、E);
⑸实验装置有一明显缺陷是: 。
【数据处理】称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g。则样品中氧化铁质量分数为 。
【实验反思】当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数 (填“偏大”,“偏小”,“无影响”)。
(6分)常州亿晶光电是一家专业从事光伏发电产品的研发、生产和销售的高新技术企业,主要从事硅片切割、电池制备、组件封装和光伏发电等业务。
⑴硅在地壳中含量位于氧和 元素之间;
⑵太阳能电池是把太阳能直接转化为 能的装置;
⑶二氧化硅是玻璃的主要成分,也是生产高纯硅的原料。玻璃属于 材料;
⑷二氧化硅与碳在高温下反应生成粗硅(Si)和一有毒气体的化学方程式是: ;
⑸粗硅生产过程必须在无氧的容器中进行,除了考虑到硅易被氧化成二氧化硅外,还有一个可能原因是 。
(6分)长荡湖为江苏十大淡水湖之一,湖中芦苇遍遍,荷叶莲莲。中华绒螯蟹深受食客喜爱。但近年来受到严重污染,常有鱼、虾、蟹死亡。
⑴中华绒螯蟹能为人体提供的营养素主要是 ;
⑵下列工业废水中会使人体蛋白质失去生理活性的物质是 (填序号);
①饱和硫酸铵溶液 ②甲醛 ③乙酸铅溶液
⑶含 两元素的物质排放会导致绿藻(化学式为C106H263O110N16P)迅速繁殖,使水中的含氧量急剧下降,而造成鱼类等水生动物因缺氧而死亡;
⑷目前有一种治理水污染的新技术,是在厌氧微生物作用下,使水中的有机物与水反应,生成二氧化碳气体和甲烷气体。有机物以C6H10O5为代表转化的化学方程式为:
;
⑸下列治理长荡湖的措施错误的是 。
①关停沿湖所有化工企业 ②将湖上餐饮船集中安置和管理
③建设污水处理设施 ④种植氮磷高效富集植物

 粤公网安备 44130202000953号
粤公网安备 44130202000953号