[江苏]2013年江苏省南京市鼓楼区中考二模化学试卷
下面是某学生学完化学用语后一次练习的部分内容,其中理解不正确的是
| A.2MnO4—:表示2个锰酸根离子 |
| B.Ar:表示氩气、氩元素和一个氩原子 |
| C.2CO2:表示2个二氧化碳分子 |
| D.维生素C(C6H8O6):表示该物质由碳、氢、氧三种元素组成。 |
下列化肥中,属于复合肥料的是
| A.NH4H2PO4 | B.NH4NO3 | C.K2SO4 | D.Ca(H2PO4)2 |
下列现象的描述错误的是
| A.木炭在氧气中燃烧发出白光 | B.磷在氧气中燃烧生成白雾 |
| C.硫磺在空气中燃烧发出淡蓝色火焰 | D.铁丝在氧气中燃烧剧烈火星四射 |
燃烧是生活中的一种常见现象。下列有关燃烧或灭火的说法错误的是
| A.用水可以灭火,是因为降低了可燃物的着火点 |
| B.任何可燃性气体跟空气充分混合后遇火时都有可能发生爆炸,因此当氢气、天然气、煤气等发生泄漏时应杜绝一切火源、火星,以防发生爆炸。 |
| C.锅里的油着火时可用锅盖盖灭,是因为隔绝了氧气 |
| D.镁可以在二氧化碳中燃烧,说明燃烧不一定要有氧气参与 |
小点同学对所学部分化学知识归纳如下,其中完全正确的一组是
| A.环境问题 |
B.资源问题 |
| 造成温室效应的气体不只是CO2 ②不合理使用化肥也会造成大气污染 ③白色污染是由于废弃塑料引起的 |
保护空气要减少有害气体和烟尘的排放 ②爱护水资源要节约用水和防治水体污染 ③保护金属资源只能通过防止金属腐蚀实现 |
| C.物质之最 |
D.健康问题 |
| 地壳中含量最多的物质是O2 ②人体中含量最多的物质是H2O ③从自然界中提取最多的金属是Fe |
缺乏某种维生素将使人患病 ②霉变食物洗净后可以食用 ③青少年缺钙会得佝偻病和发育不良 |
碘原子的结构示意图如右图所示。生活中常见的是碘-127(127为相对原子质量),而核反应中产生的则是碘-131(131为相对原子质量)。下列有关它们的说法不正确的是
| A.碘-127与碘-131所含质子数均为53 |
| B.碘-127与碘-131所含电子数相同 |
| C.碘-127与碘-131属于不同元素 |
| D.碘元素人体摄入不足或过多均会造成甲状腺肿大 |
下列现象和事实,可用金属活动性作出合理解释的是
①金属镁在空气中比铝更易点燃,说明镁比铝活动性强;
②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强;
③硫酸铜、熟石灰配制农药波尔多液,不宜用铁制容器;
④金属铜能与硝酸银溶液反应,说明铜比银活动性强。
| A.①② | B.③④ | C.①③④ | D.①②③④ |
下列各组离子能大量共存的是
| A.NH4+、 Na+、SO42- | B.H+、 Na+、 CO32- |
| C.Ba2+、 OH-、 H+ | D.Cu2+、NO3-、OH- |
下图是a、b、c三种固体物质的溶解度曲线。下列说法中正确的是
| A.a的溶解度大于c的溶解度 |
| B.在tl℃时,a、c两种溶液中溶质的质量分数相同 |
| C.c的不饱和溶液由t2℃降温至t1℃时,变成饱和溶液 |
| D.要从b溶液中得到b,通常可采用蒸发溶剂结晶的方法 |
实验测得某(NH4)2SO4化肥的样品中氮的质量分数为18.7%,则其中可能混入了
| A.NH4HCO3 | B.CO(NH2)2 | C. NH4NO3 | D. NH4Cl |
抗震救灾,众志成城。用于雅安震后防疫的众多消毒剂中,有一种高效消毒剂的主要成分为三氯异氰尿酸(C3O3N3C13),又称高氯精。下列有关高氯精的说法不正确的是
A.高氯精是有机高分子化合物
B.高氯精中C、O、N、Cl的原子个数比为1:l:1:1
C. 高氯精中氯元素的质量分数为25%
D.高氯精中C、N两种元素的质量比为12:14
下表列出了除去物质中所含少量杂质的方法,其中正确的是
| |
物质 |
所含杂质 |
除去杂质的方法 |
| A |
CO气体 |
CO2 |
通过足量氢氧化钠溶液,并干燥 |
| B |
NaOH溶液 |
Na2CO3 |
加入足量稀盐酸至不再产生气泡 |
| C |
CaO固体 |
CaCO3 |
加水溶解,过滤 |
| D |
FeSO4溶液 |
CuSO4 |
加入足量锌粒,充分反应,过滤 |
向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法:
①向滤渣中加入稀盐酸,一定有气泡产生。 ②向滤液中加入稀盐酸,一定有沉淀产生。
③滤渣中一定含有Ag。 ④滤液中一定含有Fe ( NO3)2,一定不含AgNO3,可能含有Al(NO3)3。以上说法正确的个数为
| A.0个 | B.l个 | C.2个 | D.3个 |
二氧化碳的捕捉与封存是实现温室气体减排的重要途径之一,科学家利用NaOH溶液喷淋“捕捉”空气中的CO2(如下图)。则关于该方法的叙述正确的是
| A.该方法中包含复分解反应、分解反应、置换反应等 |
| B.物质①是Ca(OH)2溶液 |
| C.操作①是过滤 |
| D.整个过程至少有NaOH和CO2两种物质可以循环利用 |
请根据下列装置图,回答有关问题:
(1) 写出图中有标号仪器的名称:a ,b 。
(2) 实验室用B、D装置制取氢气的化学方程式为 。
(3)如选用装置A作为制取氧气的发生装置,其化学方程式为
(4) 实验室用C装置收集二氧化碳时,验满的方法是 。
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应。
(1)配制100g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的 盘,称量其质量。然后按需要添加砝码、移动游码,再将氢氧化钠固体加入烧杯中,直至天平平衡。该步骤中用烧杯而不用纸称量氢氧化钠的原因是 。
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(2)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
【实验方案】
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且最终小至小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
①用pH试纸测定NaOH溶液pH时,正确的操作是: 。
②简述强调“测得的pH小于7”的理由: 。
方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。该组同学在没使用温度计的情况下,通过下图所示装置完成了实验。则该组同学根据 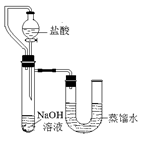
(1)从C、H、O、S、Cl、Na、N、Ca、Cu等9种元素中选择恰当的元素,用元素符号、化学式或化学方程式按下列要求填空:
①地壳中含量最多的元素 ; ② 造成硫酸型酸雨的气体 ;
③炉具清洁剂中的碱 ; ④三种元素组成的有机物 。
⑤生成两种非金属氧化物的分解反应 。
⑥难溶性盐溶于盐酸的化学方程式 。
(2)A、B、C、D表示四种物质,其微观示意图如下所示:
①从微观角度看,B图表示:3 (填化学符号)
②从宏观角度看,图中表示混合物的是 (填字母符号)
(3)在一定的条件下,A和B能发生化学反应生成E和F,其微观示意图如下所示:
①若F为空气中体积分数最大的气体,则该反应中生成的E和F的质量比 。
②若F为氧化物,且参加反应的A和B的分子个数比为5:4,则该反应的化学方程式为
。
水是一种重要的自然资源,是人类赖以生存的物质,水质的优劣直接影响人体的健康。请回答下列问题:
(1)天然水中溶解的气体主要有____ ___,利用_____ __方法可以将水中溶解的气体除去。
(2)含有较多_ ___ ___的水称为硬水,实验室中将硬水软化常用 操作。
(3)区分软水和硬水常用的物质是 。
(4)保护水环境、珍爱水资源,是每个公民应尽的责任和义务。下列做法有利于保护水资源的是 (填序号)。
| A.大量使用化肥农药 | B.工业废水处理达标后排放 |
| C.使用含磷洗衣粉 | D.生活污水直接排放 |
硫铁矿烧渣(主要成分Fe2O3、Fe3O4、FeO、SiO2等)是工业生产硫酸的废渣,利用硫铁矿烧渣制备铁红(氧化铁)等产品的部分流程如下图所示: 
(1)硫铁矿是 物(填“纯净”或“混合”)。
(2)写出碳与Fe3O4反应的化学方程式 .
(3)酸浸过滤后滤液中的溶质主要是 。
(4)反应Ⅰ的反应温度一般需控制在35℃以下,其目的是 。
(5)实验探究:产品a的主要成分是K2SO4,试设计实验探究产品a中是否含有氯化物(Cl-)杂质。
实验过程:
| 操 作 |
现 象 |
结 论 |
| ①取产品a的溶液少许,加入 |
|
目的是除尽产品中的K2SO4,避免干扰 Cl-的检验 |
| ②过滤,向滤液中加 AgNO3溶液 |
|
原样品中含有氯化物(Cl-)杂质 |
下图中的A—I所表示物质均为初中化学常见的纯净物。其中A、D是非金属单质;B、E、H 是氧化物;B中氧元素质量分数为20%且为黑色粉末;G是天然气的主要成分;C、F、I是三种不同类别的无机化合物;F常用于改良酸性土壤。图中“——”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系。(部分反应物或生成物已略去)
(1) C属于 (填“酸”、“碱”或“盐”);
D的用途 (只举一例)。
(2) 写出A与B反应的化学方程式 ,
(3) 写出E→F反应的化学方程式
(4) 写出I分解反应的化学方程式
某研究性学习小组对某珍珠粉进行了如下探究。
【查阅资料】①珍珠的化学成分主要是:碳酸钙及少量碳酸镁和壳角蛋白(蛋白质的一种);
②壳角蛋白不溶于水,加入浓硝酸加热后会变黄色;
③假珍珠粉其实就是“贝壳粉”,主要成分就是碳酸钙。
【分析讨论】①真珍珠中所含壳角蛋白在物质类别上属于 (填 “有机”或“无机”)化合物。
②假珍珠粉中的碳酸钙含量要比真珍珠粉大。
【实验探究】研究性学习小组设计了如下两个方案:
方案一 检验珍珠粉的真假
取少量珍珠粉样品于试管中, ,若观察到 ,则该珍珠粉是真珍珠粉。
方案二 检验该珍珠粉中的碳酸钙含量
步骤Ⅰ:连接仪器组成如图所示实验装置。某学生夹住C左侧的橡胶管,在A中装入少量水并取下上部塞子,打开玻璃活塞,A中水不能全部滴下,你认为该装置是否漏气? 。
步骤Ⅱ:准确称取6.000 g珍珠粉样品装入仪器B中,在A中装入稀盐酸。
步骤Ⅲ:向B中珍珠粉样品中滴加足量的稀盐酸。在仪器B、C中可观察到的现象为 、 。
步骤Ⅳ:完全反应后C中的浊液经 、 、干燥,称得白色固体的质量为11.820g,则珍珠粉样品中碳酸钙的质量分数为100%。
【实验反思】获得此测定结果,可能的原因有 。(填数字序号)
①样品中含有碳酸镁
②盐酸未滴加足量
③CO2气流速度太快导致未被Ba(OH)2完全吸收
④装置B中水蒸气、HCl等进入装置C中
【拓展延伸】有同学提出在方案二中不需要装置C,只要用电子天平准确称量装置A、B反应前后的质量,就可以得到珍珠粉样品中碳酸钙的含量。你认为是否可行 ,请说明理由 。
某同学为测定10g某赤铁矿石中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3 2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
得到如下数据:
| 装置 |
B |
C |
| 反应前质量 |
84.3g |
294.1g |
| 反应后质量 |
81.9g |
296.8g |
(1)请计算该赤铁矿石样品中氧化铁的质量分数。(写出计算过程)
(2)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为_______________________________________________(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会__________(选填“偏大”、“偏小” 或“不变”)。




 粤公网安备 44130202000953号
粤公网安备 44130202000953号