钢铁是使用最多的金属材料.
(1)利用一氧化碳与氧化铁反应,要制得5.6g铁,最少需要多少克一氧化碳?
(2)现有一种铁碳合金,其中的碳元素全部以Fe3C的形式存在,且合金中Fe3C的质量分数为36%,计算合金中碳的质量分数,并判断该合金属于生铁还是钢.
实验室常用稀盐酸与大理石反应来制取二氧化碳气体,现需制取4瓶二氧化碳气体。已知每个集气瓶的实际容积约是150mL,二氧化碳气体的密度为2g/L,大理石中碳酸钙的质量分数是80%。请计算:
(1)这4瓶二氧化碳气体的质量为 g。
(2)制取这些二氧化碳气体所需大理石的质量(写出计算过程,结果精确到0.1g)
有一不纯的白色固体氯化镁中含有少量氯化钠。化学兴趣小组的同学为了测定该固体氯化镁中氯化钠的质量分数。进行了以下实验:称量10g样品置于烧杯中,向其中加入90g水,搅拌,使其完全溶解为止。然后取该溶液一半,往其中滴加10%的氢氧化钠溶液,产生沉淀的质量与所滴入氢氧化钠溶液的质量关系曲线如图所示。
试计算:(计算结果保留小数后1位)
(1)样品中氯化镁的质量;
(2)当滴入10%的氢氧化钠溶液至A点时,所得溶液中氯化钠的质量分数。
人被蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,引起刺痛.蚁酸学名叫甲酸,它的化学式是HCOOH.请回答下列问题:
(1)甲酸属于 (填"氧化物"、"无机化合物"或"有机化合物").
(2)甲酸的相对分子质量是 .
(3)甲酸中碳、氢、氧三种元素质量比是 (最简整数比).
一瓶未贴标签的粉末状常见金属
。为了测定
的相对原子质量,准确称取一定量金属粉末,在坩埚内加强热使其完全氧化,冷却后再称重。重复实验,获得如表数据。请回答:
| 实验次数 |
金属质量(
) |
金属氧化物质量(
) |
| l |
45.0 |
84.9 |
| 2 |
45.0 |
85.1 |
| 3 |
45.0 |
85.O |
| 平均值 |
45.0 |
(1)表格中
。
(2)该金属氧化物中,
元素和氧元素的质量比为。
(3)已知
的化合价为+3价,则
的相对原予质量为。
家庭中长期使用的热水壶底部有一层水垢,主要成 分是碳酸钙和氢氧化镁,可用酸溶液来清除水垢。小明同学想通过实验测定水垢中碳酸钙的含量,他将过量的稀盐酸加入到200 g水垢中(假定水垢中杂质不与酸反应),并将产生的CO2气体全部通入到足量的NaOH溶液中(不考虑盐酸的挥发性),NaOH溶液增加的质量与反应时间的关系如图所示,
试根据题意回答下列问题:
(1)在滴入稀盐酸的过程中,观察到的一项明显现象是 。
(2)从图中可知,NaOH溶液吸收的CO2气体的总质量为_______g。
(3)在水垢中加入稀盐酸时,所发生的中和反应的化学方程式为 。
(4)计算水垢中碳酸钙的质量分数(写出相应的计算过程,结果精确到0.1%)。
现有一瓶久置的标有质量分数为10%的NaOH溶液样品,为探究其变质(NaOH易和空气中的CO2反应生成Na2CO3)的相关问题,利用U形管设计如下图所示的装置进行实验。
(1)如图甲所示,若此溶液变质,分别在U形管的两端滴入HCl溶液和澄清的石灰水时,观察到的现象:a端______ __ __,____ _______,b端___________________。
(2)如图乙所示,取此NaOH样品溶液20g放于U形管中,并在其中加入适量的酚酞试液,通过分液漏斗向U形管中滴入HCl溶液,当滴入20gHCl溶液时,恰好反应完全。
①滴入稀盐酸过程中,U形管中的溶液颜色变化为______________________________。
②恰好完全反应时,生产气体0.22g,试计算该溶液中Na2CO3的质量分数。
我国科学家侯德榜发明了联合制碱法,为世界科学发展做出了重要贡献。该制碱法以食盐为原料制备纯碱,产品中会混有少量氯化钠。某学习小组为了探测产品中纯碱的质量分数,将5g纯碱样品溶于20g水中配成溶液,再加入30g氯化钙溶液恰好完全反应( ),反应后静置、过滤、洗涤、干燥,称得沉淀质量为4.5g。请回答下列问题:
(1)过滤后的滤液质量为 g。
(2)求纯碱样品中纯碱的质量分数。(写出计算过程)
火力发电厂用石灰石泥浆吸收废气中的二氧化硫以防止污染环境,其反应方程式:2CaCO3+2SO2+O2==2CaSO4+2CO2。
(1)若1000克废气中含1.6克二氧化硫,则处理1000克这种废气需要多少克碳酸钙?
(2)处理上述1000克废气,可得到含85%CaSO4的粗产品多少克?
钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂说明书的部分信息如图所示。
现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图像如下。请根据有关信息回答问题。
| |
第1次 |
第3次 |
第4次 |
| 加入盐酸的质量(g) |
20 |
20 |
20 |
| 剩余固体的质量(g) |
35 |
a |
20 |
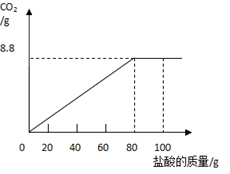
(1)该品牌补钙药剂中CaCO3的质量分数是 ,a的数值为 。
(2)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数)。
(5分)某水下供氧设备中供氧剂是过氧化钠(Na2O2)。过氧化钠能与水反应,生成氧气,反应的化学方程式为:2Na2O2 + 2H2O ="=" 4NaOH + O2↑
某同学为进一步探究过氧化钠与水的反应中各物质质量关系,将15.6g过氧化钠加入盛有147.6g水(过量)的烧杯中充分反应,直至固体完全消失,不再有气泡产生。请计算:
(1)反应生成的氧气质量;
(2)反应后所得溶液中溶质的质量分数。
某化工厂怀疑采购来的烧碱有部分变质,工厂技术员为了测定其变质情况,即测定烧碱的纯度(假设样品中只有氢氧化钠和碳酸钠这两种成分,且碳酸钠是变质产生的),做了如下实验:取烧碱样品20g,分四次加入到36.5g一定浓度的稀盐酸中,数据如下表所示
| 实验次数 |
1 |
2 |
3 |
4 |
| 每次加入样品的质量/g |
5 |
5 |
5 |
5 |
| 反应后剩余物质的总质量/g |
40.4 |
44.3 |
M |
54.3 |
请根据提供的数据,回答下列问题:
(1)表格中m的数值为 .
(2)请计算烧碱样品中烧碱的纯度.
某快递公司违反国家规定快递有毒化学品,因化学品泄露,导致多人伤亡,被称为“夺命快递”,“夺命快递”中的化学品是氟乙酸甲酯(化学式为C3H5FO2),是有毒液体,在燃料、医药、农药等工业领域有着广泛的用途.
(1)氟乙酸甲酯中氟元素的质量分数是 。
(2)一般成人接触400mg氟乙酸甲酯就会急性中毒,如果检测到被氟乙酸甲酯污染的某物品上含有氟元素57mg(氟元素都来自氟乙酸甲酯),则接触该污染物品的成年人至少接触到了 mg氟乙酸甲酯.
某兴趣小组为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:
①在三个烧杯中分别加入11.0g样品及足量的水配成溶液;
②向三个烧杯中分别加入一定质量氯化钙溶液;
③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体。
实验所得数据见下表,请你分析并进行有关计算:
| |
烧杯Ⅰ |
烧杯Ⅱ |
烧杯Ⅲ |
| 加入氯化钙溶液的质量(g) |
50.0 |
110.0 |
150.0 |
| 白色固体的质量(g) |
5.0 |
10.0 |
10.0 |
(1)样品中碳酸钠的质量分数是多少?(结果精确到0.1%)
(2)求所加入的氯化钙溶液的溶质质量分数?