某化学兴趣小组欲检验当地石灰石中碳酸钙的纯度。在实验室将25克石灰石样品(杂质不参加反应,也不溶于水)放入盛有100克稀盐酸的烧杯中,恰好完全反应。测得烧杯中物质的总质量为116.2克。求:
(1)生成二氧化碳的质量。
(2)样品中碳酸钙的质量分数。
(3)所用稀盐酸中溶质的质量分数。
在做电解水实验时,常在水中加入氢氧化钠来增强溶液的导电性,但氢氧化钠本身不会发生化学反应,质量也不会发生改变。现将含有8g氢氧化钠的水溶液109g通电一段时间后,生成1g氢气,请你计算(要有计算过程):
(1)电解所消耗的水的质量;
(2)电解水后的氢氧化钠溶液的质量分数。
实验室中有一瓶存放时间过长的
药品,其中一部分已转化为
。取lOg该药品放入烧杯中,加154g水配成溶液,将400g一定溶质质量分数的
溶液分四次加人该烧杯中,充分反应后,测得生成沉淀质量的数据记录如下表:

(1)m=,
(2)求10g该药品中
的质量,
(3)第三次加入
溶液充分反应后,所得溶液中溶质质量分数是多少?
小雨从超市买同一包纯碱,其包装说明如图1所示。他称取了11g纯碱样品溶于
水中配制成50g溶液,然后向溶液中滴加氯化钙溶液,其产生沉淀的质量与滴加氯化钙溶液
的质量关系如图2所示。

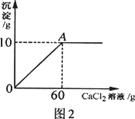
(1)通过计算判断纯碱样品中碳酸钠的质量分数是否与包装说明相符。
(2)计算A点时,所用溶液中溶质的质量分数。(计算结果保留一位小数)
氯化镁是制取镁的原料之一。现要测定某化工产品(含MgCl2和KCl)中所含的氯化镁质量分数,进行实验:先将10g样品完全溶于水,然后把50g一定质量分数的氢氧化钾溶液平均分五次加入样品溶液中,充分振荡,实验所得数据见下表:

请分析上述数据,回答下列问题:
(1)表中a为。
(2)样品中的氯化钾属于化肥中的肥,可回收利用。
(3)所用的氢氧化钾溶液中溶质的质量分数是。
(4)计算样品中氯化镁的质量分数是多少?(写出计算过程)
(11分)某合金可能由铜与镁、锌中的一种组成,现欲测定其组成,进行如下实验:取该合金样品10.0 g放入烧杯中,然后将56.0 g溶质质量分数为14.0%的稀硫酸平均分四次依次加入该烧杯中,每次均充分反应。实验数据记录如下表:
试求:
(1)该合金中铜的质量分数是__________。
(2)该合金除了铜外,另一种金属的是什么呢?(写出过程)
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?(写出计算过程,结果精确到0.1%)
(5分)某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数。取20 g石灰石样品(假设杂质既不溶于水,也不与其他物质反应),向其中加入100 g一定溶质质量分数的稀盐酸,恰好完全反应,称得固液混合物的质量为113.4 g。请回答下列问题:
(1)写出发生反应的化学方程式________________________________________;
(2)列出求解该样品中参加反应的碳酸钙质量(x)的比例式________________;
(3)该样品中碳酸钙的质量分数为________;
(4)向反应后的固液混合物中加入113.6 g水,充分搅拌后过滤,得到只含一种溶质的不饱和溶液,则所得不饱和溶液中溶质的质量分数为_____;
(5)欲配制150 g上述实验所用的稀盐酸,需要36.5%的浓盐酸质量为_______________---。
在一定条件下可转化为 : ,反应前 的质量为160克,反应过程中, 的转化率(参加反应的 与反应前的 的质量比)用 表示,固体中铁元素与氧元素的质量比用 表示.
(1)填写下表中的空格:
|
|
|
|
|
| 固体成分 |
|
|
|
| 转化率 |
0 |
|
|
(2)如果
转让为
的反应分两步进行:
;
反应后的固体中 时固体的成分可能有三种情况:
(1) ;
(2)(填化学式、下同);
(3).
元明粉是重要的化工原料,右图是某品牌元明粉包装袋上的部分标签。
为测定该元明粉中
含量是否符合标签要求,把15.0
样品(假设只含不溶性杂质)
加入一定量的水溶解,过滤得100.0
滤液。取10.0
滤液,加入10%的
溶液20.8
g,恰好完全反应,反应的化学方程式:
。
(1)计算10.0
滤液中
的质量。
(2)根据这一次检测,计算并判断样品
的含量是否符合标签要求。

一天,老师给了小粱一包含有氯化钠杂质的氯化钙粉末,让他探究氯化钙的
质量分数,小粱进行了如下探究:称取该粉末
.把它完全溶于
水中,然后向所
得溶液中滴加质量分数为l0.6%的碳酸钠溶液,反应完全后,得到
沉淀,请按要求回
答问题:
(1)所加碳酸钠溶液质量与产生沉淀质量的关系图是(填序号)
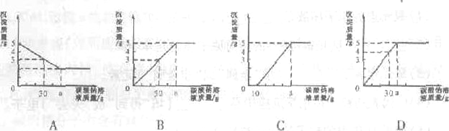
(2)这包混合物粉末中氯化钙的质量分数是。(精确到0.1%)
(3)当混合物中氯化钙和碳酸钠恰好完全反应时,所得溶液中溶质的质量分数是多少?(要求写出计算过程)