有一不纯的白色固体氯化镁中含有少量氯化钠。化学兴趣小组的同学为了测定该固体氯化镁中氯化钠的质量分数。进行了以下实验:称量10g样品置于烧杯中,向其中加入90g水,搅拌,使其完全溶解为止。然后取该溶液一半,往其中滴加10%的氢氧化钠溶液,产生沉淀的质量与所滴入氢氧化钠溶液的质量关系曲线如图所示。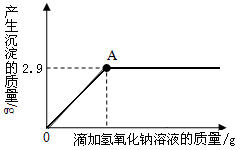
试计算:(计算结果保留小数后1位)
(1)样品中氯化镁的质量;
(2)当滴入10%的氢氧化钠溶液至A点时,所得溶液中氯化钠的质量分数。
有一不纯的白色固体氯化镁中含有少量氯化钠。化学兴趣小组的同学为了测定该固体氯化镁中氯化钠的质量分数。进行了以下实验:称量10g样品置于烧杯中,向其中加入90g水,搅拌,使其完全溶解为止。然后取该溶液一半,往其中滴加10%的氢氧化钠溶液,产生沉淀的质量与所滴入氢氧化钠溶液的质量关系曲线如图所示。
试计算:(计算结果保留小数后1位)
(1)样品中氯化镁的质量;
(2)当滴入10%的氢氧化钠溶液至A点时,所得溶液中氯化钠的质量分数。