山东省济南市槐荫区九年级一模化学试卷
“低碳减排,绿色生活”是2015年世界环境日的中国主题。大气中PM2.5(指大气中直径不超过2.5μm的可吸入颗粒物)的增多会导致雾霾天气,对人体健康和环境质量影响较大。下列做法中,不应提倡的是
| A.大量植树造林 | B.大力发展露天烧烤 |
| C.充分利用太阳能 | D.尽量采用环保出行 |
化学实验是进行化学研究的重要方法。下列实验操作中,符合操作规范的是
| A.烧碱溶液不慎沾到皮肤上,应先用大量水冲洗,再涂上盐酸 |
| B.加热蒸发结晶过程中,当溶液全部蒸干后停止加热 |
| C.为防止液体流出,将胶头滴管伸入试管内滴加液体 |
| D.洒在桌上的酒精燃烧起来,应立即用湿抹布盖灭 |
化学与生产、生活、社会发展紧密相连。下列说法中,不正确的是
| A.香肠中加入大量的亚硝酸钠作防腐剂 |
| B.冬天室内用煤炉取暖要严防煤气中毒 |
| C.做面包时可用适量的小苏打作发酵粉 |
| D.使用燃煤脱硫技术能有效防止酸雨的形成 |
通过初中化学的学习,我们总结或发现了许多知识具有一定的规律性。下列有关规律性知识的描述中,正确的是
| A.所有的酸中都一定含有氢元素 |
| B.燃烧都是剧烈的发光、发热的化合反应 |
| C.含碳元素的化合物一定是有机物 |
| D.能使燃烧的木条熄灭的气体一定是氮气 |
甲、乙两物质发生反应的微观示意图如下,则下列说法中,不正确的是
| A.该反应属于化合反应 | B.该反应前后原子个数保持不变 |
| C.该反应遵循质量守恒定律 | D.甲和丙中同种元素的化合价均相等 |
下列实验方法中,不能达到实验目的的是
| A.用水鉴别硫酸铜固体和氢氧化钠固体 |
| B.用AgNO3溶液检验H2中混入的少量HCl气体 |
| C.用Ba(OH)2溶液除去NaCl溶液中的Na2CO3杂质 |
| D.用稀盐酸检验暴露在空气中的NaOH固体是否变质 |
有一瓶无色液体X,分成三等份,向其中分别加入少量的氯化钡溶液、氧化铜粉末、氢氧化钠溶液,产生的现象如下表。则物质X是下列选项中的
| |
氯化钡溶液 |
氧化铜粉末 |
氢氧化钠溶液 |
| 物质X |
白色沉淀 |
溶解,溶液变蓝 |
无明显现象 |
A.硫酸钠溶液 B.稀硫酸 C.稀硝酸 D.澄清的石灰水
向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入一定质量的锌粉,充分反应后过滤,滤液为蓝色。根据上述实验现象分析判断,下列说法中,不正确的是
| A.滤液中一定存在Zn(NO3)2 | B.滤液中可能存在Ag+ |
| C.滤渣中一定含有单质Ag | D.滤渣中一定含有单质Cu |
将13.7g Na2CO3和NaHCO3的固体混合物,加热至固体质量不再减少,然后向此固体中加入一定量的氯化钙溶液,恰好完全反应后过滤,得到117g溶质质量分数为10%的不饱和溶液,则原固体混合物中钠元素的质量为
| A.2.3g | B.4.6g | C.6.9g | D.9.2g |
化学就在我们身边,它与我们的生活紧密相连。现有氧气、氢气、盐酸、氢氧化钠、硝酸钾、氧化铁六种物质。请按要求用化学式填空:
(1)理想的清洁能源 ;
(2)胃酸的主要成分 ;
(3)铁锈的主要成分 ;
(4)可作复合肥料的盐 。
丙三醇(其化学式为C3H803)是无色、味甜、粘稠的液体,俗称甘油。甘油极易氧化,热稳定性好。在造纸、化妆品、照相、印刷、金属加工和橡胶等工业中都有着广泛的用途。请根据以上信息按要求回答下列问题:
(1)从物质分类:丙三醇属于 (填“纯净物”、“混合物”、“氧化物”、“有机物”中的两项)。
(2)从分子构成:丙三醇中氧、氢原子个数比 (填最简整数比)。
(3)从物质组成:丙三醇中质量分数最大的元素是 。
(4)从物质性质:丙三醇的物理性质是 (写一条即可)。
春暖花开,正是踏青游玩的好时节。同学们自发组织到郊外游玩、野炊。他们携带了铁锅、食盐、食醋、面条、西红柿、去污粉(有效成份为碳酸钠)等必备物品。
(1)同学们在游玩时常闻到花香的气味,从微观角度解释原因: 。
(2)在携带物品过程中,小刚同学不慎将装食盐、去污粉的瓶子混淆了。有的同学建议,用所携带物品中的 (填名称)就可以将它们区分开来。
(3)野炊时,小明生火后,小心地调节铁锅到合适的高度,他这样做的主要原因是_______(填字母序号)。
A.避免铁锅被烤坏 B.使用外焰加热 C.避免做汤时溅出
(4)野炊结束时,小辉用干布抹去铁锅表面的水珠。他这样做的目的是 。
溶解度是物质溶解性的定量表示,溶解度曲线可表示物质在不同温度下的溶解度。甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:
(1)甲、乙两种物质中溶解度受温度影响较大的是 物质。
(2)若甲物质中混有少量的乙物质,提纯甲物质最好采取的方法是 (填“降温结晶”或“蒸发结晶”)。
(3)t2℃时,乙物质的溶解度为 g;t2℃时,若将30g乙物质加入到50g水中,所得溶液的溶质质量分数是 (计算结果精确到0.1%)。
(4)将t1℃的甲、乙两物质的饱和溶液(均无固体物质剩余)升温到t2℃时,所得甲物质溶液的溶质质量分数 乙物质溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
下图所示为实验室中常见气体的制备、干燥、收集和性质实验的部分仪器,某校化学兴趣小组的同学欲用它们完成如下探究实验。试根据题目要求回答下列问题: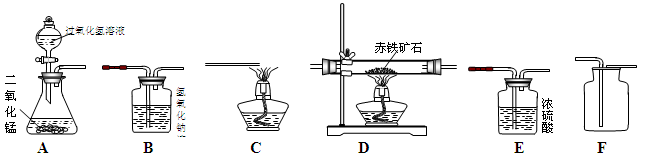
(1)第一组的同学以过氧化氢溶液为原料(MnO2为催化剂),在实验室中制备并收集一瓶干燥的氧气。
①所选仪器的连接顺序为 (填写装置序号字母)。
②仪器A中所发生反应的化学方程式为 。
③收集气体时,导气管要伸到集气瓶底部的目的是 。
(2)第二组的同学欲用含少量二氧化碳的一氧化碳气体,测定赤铁矿石中氧化铁的含量(杂质不参加反应)。所选仪器的连接顺序为:混合气体→B1→E→D→B2→C。试回答下列问题:(假设过程中氧化铁全部参加反应;仪器B1、B2吸收气体完全。)
①仪器D中的现象为 。
②若通过测量反应前、后仪器B2的质量变化,来计算赤铁矿石中氧化铁的含量,如果不连接仪器B1,则这样计算出的氧化铁含量与实际值比较将 (填“偏小”“ 偏大”“ 基本一致”之一)。
③实验结束后,若测得仪器B1中溶液增加的质量与仪器D中固体减少的质量相等。那么仪器B1中溶液增加质量与仪器B2中溶液增加质量之比为 (填最简整数比)。
④化学实验操作的先后顺序,对化学实验的结果及安全等可能会有一定的影响。第二组同学所做实验开始时,先点燃装置C处酒精灯的原因是 。
现欲探究一固体混合物A的成分,已知其中可能含有NH4Cl、Cu(OH)2、BaSO4、CaO、NH4 NO3五种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应均恰好完全反应)
试根据实验过程和发生的现象判断:
(1)常温下,气体B的水溶液显_________(填“酸性”“中性”“碱性”之一)。
(2)滤渣D的化学式是_________________。
(3)固体混合物A中,一定存在的物质是(写化学式)___________________________。
(4)滤液C中,一定大量存在的金属离子是(写离子符号)________________________。
(5)写出过程③中可能发生的一个化学方程式: 。
(6)固体混合物A中还不能确定存在的物质是(写化学式) ,得出此结论的理由是 。
家庭中长期使用的热水壶底部有一层水垢,主要成 分是碳酸钙和氢氧化镁,可用酸溶液来清除水垢。小明同学想通过实验测定水垢中碳酸钙的含量,他将过量的稀盐酸加入到200 g水垢中(假定水垢中杂质不与酸反应),并将产生的CO2气体全部通入到足量的NaOH溶液中(不考虑盐酸的挥发性),NaOH溶液增加的质量与反应时间的关系如图所示,
试根据题意回答下列问题:
(1)在滴入稀盐酸的过程中,观察到的一项明显现象是 。
(2)从图中可知,NaOH溶液吸收的CO2气体的总质量为_______g。
(3)在水垢中加入稀盐酸时,所发生的中和反应的化学方程式为 。
(4)计算水垢中碳酸钙的质量分数(写出相应的计算过程,结果精确到0.1%)。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号