如右图所示,打开止水夹,将液体A滴入试管②中与固体B接触,若试管①中的导管口有气泡产生,则液体A和固体B的组合不可能是
| A.稀盐酸和锌粒 | B.过氧化氢溶液和二氧化锰 |
| C.水和氢氧化钠 | D.水和硝酸铵 |
A~F是初中化学所学的常见物质,其转化关系如图所示(部分反应物和生成物、反应条件已略去)。B是白色难溶固体,其中金属元素的质量分数为40%,C俗称纯碱,F是最常见溶剂。
请回答:A的一种用途是 ;反应①的化学方程式为 ;反应④发生时的一个明显现象是 。
过氧化钠(Na2O2)可用作呼吸面具的供氧剂.实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】1.过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+02↑, 2Na202+2C02==2Na2CO3+O2.
【提出问题】1.过氧化钠是否变质?
【猜想与假设】
假设1:过氧化钠未变质; 假设2:过氧化钠部分变质; 假设3:过氧化钠全部变质.
【实验探究】
【提出新问题】部分变质的过氧化钠中是否含有氢氧化钠?
【实验探究】③取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】
(1)由实验③可以确定①中溶液含有的溶质是___ ____(填化学式);
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是_________。
【定量研究】称取6.04g的过氧化钠样品于锥形瓶中,加入足量的蒸馏水,共收集到气体0.64g,再向上述锥形瓶中加入足量的澄清石灰水,充分反应后,经过沉淀、过滤、干燥等,得到固体2.00g。
(1)写出加入澄清石灰水的反应方程式_____________________
(2)6.04g上述样品中,含氢氧化钠的质量_______________。
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为 (填化学式)
如下图所示,A-G是初中化学常见的其中物质。图中" "表示转化关系,"
"表示转化关系," "表示相互能反应。F可以用于改良酸性土壤,D、E组成元素相同,B、C、G常温下为气体,在实验室中常用A制取G。
"表示相互能反应。F可以用于改良酸性土壤,D、E组成元素相同,B、C、G常温下为气体,在实验室中常用A制取G。

(1)F的化学式是;物质A的一种用途是。
(2)D C反应的化学方程式是。
C反应的化学方程式是。
(3)F G反应的化学方程式是。
G反应的化学方程式是。
(4)图中涉及B物质的反应中,未出现的基本反应类型是。
某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如下图),有一瓶溶液的试剂瓶未盖瓶盖且标签破损,于是决定利用现有药品对这瓶溶液进行实验探究:
【提出问题】这瓶溶液是什么溶液?
【获得信息】1.性质实验中用到含用钠元素的物质是氢氧化钠、碳酸钠和硫酸钠
2.硫酸钠溶液、氯化钡溶液都呈中性
【提出问题】这瓶溶液是:
猜想①: ;
猜想②:氢氧化钠溶液;
猜想③:碳酸钠溶液;
【实验探究】
(1)小丽取样滴加 溶液,溶液呈红色,得出结论:猜想 不成立。理由是 。
(2)小刚另取样品滴加BaCl2溶液,有 产生,小刚得出结论:猜想②不成立。小组同学讨论后认为结论不正确,理由是 。
小组同学讨论后一致认为应如下进行实验:
【继续探究】
(3)取样品加入过量的BaCl2溶液,加“过量”的目的是 ;静置后,取上层清液滴入酚酞试液,溶液呈红色。在剩余物质中滴入足量的稀盐酸,固体全部溶解,固体溶解的反应的化学方程式是 。
【实验结论】
(4)这瓶溶液是 。
【探究启示】
(5)实验取完药品后应 。
己知
为初中化学中常见的五种不同类别的物质,其中
为年产量最高的金属单质,各种物质间的反应和转化关系如图所示("公,表示相连的两种物质之间可发生反应,"一表示一种物质可以转化为另一种物质;反应条件、部分反应物和生成物己略去),请写出:
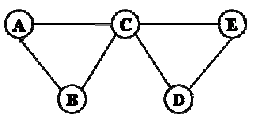
(1)
的化学式.
(2) 与 反应的化学方程式.
下列各组物质两两之间都能互相发生化学反应的是( )
| A.C CuO H2SO4(稀) |
| B.Ba(OH)2 HCl(稀) K2CO3 |
| C.Fe HCl(稀) CuSO4 |
| D.CO2 Ca(OH)2 HCl(稀) |
化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
| 实验操作 |
实验现象 |
实验结论 |
| 取少量该溶液于试管中,向溶液中滴加 , 并不断振荡. |
有 产生. |
氢氧化钠溶液一定变质了. |
【提出问题2】该氢氧化钠溶液是全部变质还是部分变质呢?
【猜想与假设】
猜想1:氢氧化钠溶液部分变质.
猜想2:氢氧化钠溶液全部变质.
【查阅资料】
(1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl
【实验探究2】
| 实验步骤 |
实验现象 |
实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的 溶液,并不断振荡. |
有 生成. |
说明原溶液中一定有碳酸钠. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. |
溶液变红色. |
说明原溶液中一定有 . |
【实验结论】该氢氧化钠溶液 (填“部分”或“全部”)变质.
【反思与评价】
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式: .
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案 (填“可行”或“不可行”).
海洋是一个巨大的资源宝库,海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钠等.如图为综合利用海水制备金属镁的流程.
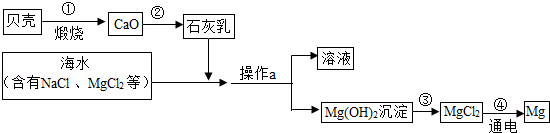
该流程中没有涉及的化学反应是( )
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
如图所示,在盛有稀硫酸的烧杯中,滴加几滴氯化钡溶液后,在烧杯里的溶液中离子数目的变化是
| A.Cl-增多了,SO42-减少了 | B.Ba2+增多了,H+减少了 |
| C.Cl-增多了,H+减少了 | D.H+减少了,SO42-减少了 |
化学老师交给某研究性学习小组一个任务:测定实验室里一瓶久置的NaOH固体是否变质。该小组的同学进行了如下实验探究:
【提出问题】 猜想I:没变质,全部是NaOH;猜想II:部分变质,既含有NaOH又含有Na2CO3:猜想Ⅲ:完全变质,全部是Na2CO3。
【查阅资料】①已知反应:BaCl2+Na2CO3=2NaCl+BaCO3↓
②部分盐溶液在常温下的pH如下:
| 盐溶液 |
NaCI |
Na2CO3 |
BaCl2 |
| pH |
等于7 |
大于7 |
等于7 |
【设计方案并进行实验】请你与他们一起共同完成,并回答所给问题:
| 实验步骤 |
实验现象 |
实验结论 |
| ①称取上述氢氧化钠固体样品8.0g溶于50ml,水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置。 |
产生白色沉淀 |
说明久置固体中,一定含有 (填化学式)。 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH |
pH=11 |
说明久置固体中,还一定含有 (填化学式)。 |
上述步骤①中,所用称量仪器的名称是 ,滴加过量BaCl2溶液的目的是
【实验结论】通过实验,说明上述猜想中 是正确的。
【反思】久置的氢氧化钠变质的原因是
(用化学方程式表示)。
【表达与交流】在实验室里氢氧化钠需要密封保存。药品密封保存的原因很多,请你写出浓盐酸需要密封保存的原因 。
下列实验设计能达到实验目的是( )
| 选项 |
实验目的 |
实验方案 |
| A |
检验某气体是否为二氧化碳 |
用燃着的木条 |
| B |
稀释浓硫酸 |
将水缓慢加入浓硫酸中,并搅拌 |
| C |
区分氧化钙与碳酸钙 |
取样品,加入适量水 |
| D |
除去K2S04溶液中的K0H |
加入适量稀盐酸 |
除去下列物质中的少量杂质,方法错误的是
| 选项 |
物质 |
所含杂质 |
除杂质的方法 |
| A |
通过足量的氢氧化钠溶液,干燥 |
||
| B |
加入足量的稀硫酸,过滤,洗涤,干燥 |
||
| C |
加入适量的稀盐酸,过滤,洗涤,干燥 |
||
| D |
溶液 |
加入适量的氢氧化钾溶液,过滤 |
某化学兴趣小组在做完制取二氧化碳的实验后(用石灰石和稀盐酸制取),对反应后反应器内的剩余溶液的溶质成分产生了兴趣,他们继续进行了以下实验探究。
【分析推断】根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙。但其中是否含有氯化氢需要通过实验来证明。若剩余溶液显酸性(含有H+),说明含有氯化氢。
【查阅资料】碳酸钙不溶于水,氢氧化钙微溶于水,氯化钙溶液呈中性。
【实验过程】将剩余的溶液倒入烧杯中,微热后冷却到室温。
| |
实验操作 |
实验现象 |
实验结论 |
| 甲同学 |
取烧杯中溶液少许于试管中,向其中滴加①____________ |
现象:溶液变为红色 |
溶液显酸性(含有H+);溶质中有氯化氢。 |
| 乙同学 |
取烧杯中溶液少许于试管中,向其中加入少量锌粒 |
现象:②_____________ |
|
| 丙同学 |
取烧杯中溶液少许于试管中,向其中加入少量石灰石 |
现象:③_________________ 化学方程式为: ④______________________ |
【拓展提高】若要从剩余溶液中得到尽可能多的纯净的氯化钙固体,同学们认为可以向剩余溶液中加入稍过量的 ⑤__________(填化学式),经 ⑥___________、蒸发等操作后即可完成。