山东省滨州市部分学校九年级上学期12月联考化学试卷
以下各类物质中一定含有氢元素的是( )
①酸 ②碱 ③盐 ④氧化物.
| A.①② | B.①②③ | C.①②④ | D.①②③④ |
以下家庭食品制作中,发生了化学变化的是( )
| A.萝卜风干 | B.凉水冻冰 | C.葡萄酿酒 | D.辣椒剁碎 |
玻璃棒在化学实验中有重要用途,下列有关玻璃棒的使用不正确的是( )
| A.过滤时用玻璃棒轻轻搅动漏斗中的液体,以加快过滤 |
| B.过滤时用玻璃棒引流,让液体沿玻璃棒慢慢流下,以防液体飞溅 |
| C.蒸发溶液时用玻璃棒不断搅拌,使液体均匀受热,以防液滴飞溅 |
| D.配制溶质质量分数一定的溶液时用玻璃棒搅拌,可以加快溶质溶解 |
如图所示实验操作正确的是( )
A. 闻气味 闻气味 |
B.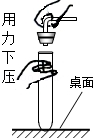 塞紧橡皮塞 塞紧橡皮塞 |
C.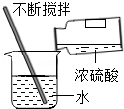 稀释浓硫酸 稀释浓硫酸 |
D.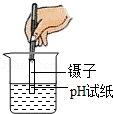 测定溶液的酸碱度 测定溶液的酸碱度 |
一些食物近似pH如下表
| 食物 |
番茄 |
牛奶 |
鸡蛋清 |
苹果汁 |
| pH |
4.0~4.4 |
6.3~6.6 |
7.6~8.0 |
2.9~3.3 |
则下列说法不正确的是( )
A.胃酸过多的人应少食苹果 B.番茄汁属于酸性食品
C.牛奶和鸡蛋清均为碱性食品 D.苹果汁酸性比牛奶强
甲、乙两种不含结晶水的固体物质溶解度曲线如图,下列说法中不正确的是( )
| A.t1℃时,50g甲的饱和溶液中溶解了10g的甲 |
| B.将t2℃甲、乙两种物质的饱和溶液升温至t3℃(溶剂的量不变),两种溶液中溶质的质量分数相等 |
| C.t2℃时,要使接近饱和的乙溶液达到饱和状态,可采用蒸发溶剂的方法 |
| D.分别将t2℃甲、乙两种物质的溶液降温至t1℃,一定都有晶体析出 |
我省盛产茶叶,“雪青”“清润名茶”等绿茶享誉省内外.绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46.下列说法不正确的是( )
| A.单宁酸由碳、氢、氧三种元素组成 |
| B.1个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成 |
| C.单宁酸分子中碳、氢、氧原子数比38:26:23 |
| D.1个单宁酸分子中含26个氢分子 |
某同学的实验报告中,有以下实验数据,其中不合理的是( )
| A.用pH试纸测得溶液的pH值为3.5 |
| B.用体温计测得体温为37.5℃ |
| C.用10ml量筒量取5.6ml稀盐酸 |
| D.用托盘天平称得12.8g食盐 |
下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( )
| A.紫色石蕊溶液 | B.氯化钠溶液 | C.铁粉 | D.pH试纸 |
关于化学反应A+B=C+D,下列说法中正确的是( )
A.若生成物C和D分别是盐和水,则反应物一定是酸和碱
B.若C是单质、D为化合物,则A和B中一定有一种是单质,一种是化合物
C.若A和C是单质,B和D是化合物,则该反应类型属置换反应
D.若A、B各取10g混合,使其充分反应,则C、D质量的总和一定等于20g
Sb2O5是一种重要的阻燃剂.用X来生成该阻燃剂的化学方程式为:X+2H2O2═Sb2O5+2H2O.根据质量守恒定律,推断X的化学式为( )
| A.SbO2 | B.Sb2O3 | C.HSbO3 | D.H3SbO4 |
森林着火时,救火员开辟防火隔离带的目的是( )
| A.隔绝空气 |
| B.开辟道路以利于运水灭火 |
| C.隔离可燃物 |
| D.使可燃物温度降低到着火点以下 |
下列关于海水晒盐原理的分析正确的是( )
| A.利用阳光照射,使海水升温得到食盐 |
| B.利用海风降温析出食盐晶体 |
| C.利用海水在阳光下发生分解反应制得食盐 |
| D.利用阳光和风力使水分蒸发得到食盐 |
在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如表.下列说法中不正确的是( )
| 物质 |
甲 |
乙 |
丙 |
丁 |
| 反应前物质质量/g |
8 |
32 |
5 |
4 |
| 反应后物质质量/g |
16 |
4 |
x |
24 |
A.该反应为分解反应
B.丙可能为该反应的催化剂
C.甲、乙两种物质间参加反应的质量比为1:4
D.乙、丁两种物质间反应的质量比为7:5
海洋是一个巨大的资源宝库,海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钠等.如图为综合利用海水制备金属镁的流程.
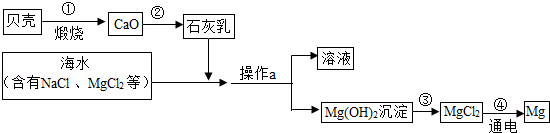
该流程中没有涉及的化学反应是( )
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
重结晶后的食盐中往往还含有少量的硫酸钠、氯化镁、氯化钙等杂质,它们在溶液中主要以SO2﹣4、Ca2+、Mg2+的形式存在,为将这些杂质除净,可向食盐溶液中加入过量的氢氧化钠、碳酸钠、氯化钡溶液,然后加入盐酸调至溶液pH=7,最后经过过滤、蒸发得到精盐.下列操作及加入溶液顺序错误的是( )
| A.BaCl2、NaOH、Na2CO3、过滤、HCl |
| B.BaCl2、Na2CO3、NaOH、过滤、HCl |
| C.NaOH、BaCl2、Na2CO3、过滤、HCl |
| D.Na2CO3、BaCl2、NaOH、过滤、HCl |
用化学用语填空.
(1)2个氧分子 ;
(2)亚铁离子 ;
(3)地壳中含量最多的元素 ;
(4)氢氧化铝中铝元素显+3价 ;
(5)2个硝酸根离子 .
将生锈的铁钉放入过量的盐酸中,首先看到铁锈溶解,溶液呈 色,这是因为(用化学方程式表示) ,不一会儿,又看到溶液中有 的现象,这是因为(用化学方程式表示) .
已知A、B、C、D、E五种物质之间存在以下转化关系.其中A、C两种物质的组成元素相同,且常温下是液体,E是天然气的主要成分(甲烷).

请回答:
(1)写出DE两种物质的化学式:D ,E .
(2)写出A→B+C的化学方程式: .
(3)写出D物质的一种用途: .
如图1为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.

(1)当温度为10℃时,碳酸钠的溶解度为 ;
(2)当温度 时,氯化钠的溶解度大于碳酸钠的溶解度;
(3)我国北方盐湖“夏天晒盐,冬天产碱”,“冬天产碱”的原因原理是 .
(4)如图2所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是 (填字母序号).
| A.氢氧化钠 | B.生石灰 | C.硝酸铵 | D.浓硫酸. |
如图中的①、②分别是钠元素、;氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图.
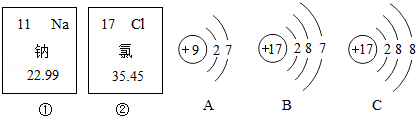
试回答下列问题:
(1)钠元素的原子序数为 ,画出它的原子结构示意图 ;
(2)A、B、C中属于同种元素的粒子是 ;
(3)A和B两种粒子的 相同,所以它们具有相似的化学性质;
(4)钠原子和氯原子反应所形成的化合物是由 (填“分子”、“原子”、“离子”)构成的.
如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:

(1)用图中表示的序号表示配制溶液的正确操作顺序 .
(2)图②中,有一种塑料仪器,其名称是 .
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数见图⑥,则称取的NaCl质量为 .
(4)根据计算需要量取水的体积是 (水的密度为1g/mL).
(5)称量NaCl质量完毕放回砝码时,发现有一个砝码缺损了一个小角,若其他操作步骤正确,则所配溶液的溶质质量分数 (填“大于”、“小于”或“等于”)10%.
根据如图所示装置回答问题:
实验室制取二氧化碳最好选择的发生装置是 ,装置优点是 ,反应的化学方程式 .实验室用D来收集二氧化碳,二氧化碳应从 进(选“a”或“b”).

化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
| 实验操作 |
实验现象 |
实验结论 |
| 取少量该溶液于试管中,向溶液中滴加 , 并不断振荡. |
有 产生. |
氢氧化钠溶液一定变质了. |
【提出问题2】该氢氧化钠溶液是全部变质还是部分变质呢?
【猜想与假设】
猜想1:氢氧化钠溶液部分变质.
猜想2:氢氧化钠溶液全部变质.
【查阅资料】
(1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl
【实验探究2】
| 实验步骤 |
实验现象 |
实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的 溶液,并不断振荡. |
有 生成. |
说明原溶液中一定有碳酸钠. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. |
溶液变红色. |
说明原溶液中一定有 . |
【实验结论】该氢氧化钠溶液 (填“部分”或“全部”)变质.
【反思与评价】
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式: .
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案 (填“可行”或“不可行”).

 粤公网安备 44130202000953号
粤公网安备 44130202000953号