电解水的装置如图,回答下列问题:
①写出电解水的化学方程式(12) ;
②实验取用180mL水,这些水的物质的量约为(13) ;
③试管C中的气体是(14) ,A 处是电源的(15) 极(填写“正”或“负”);
④为了使电解顺利进行需要向水中加入硫酸,若向100g水中加入l0g 质量分数为0.1的稀硫酸,此时溶液的质量分数为(16) 。
⑤有同学想知道:若向水中加入食盐,是否同样可以实现电解水?他仍用右图装置进行食盐溶液的电解,发现D中也有气体,且有黄绿色,则该气体是(17) (选填编号)。
| A.氧气 | B.氢气 | C.氯化氢 | D.氯气 |
电解结束后向溶液滴入酚酞,溶液变红,说明还有(18) (填写化学式)生成。
2015年3月22日是第二十三届“世界水日”,主题是“水与可持续发展”。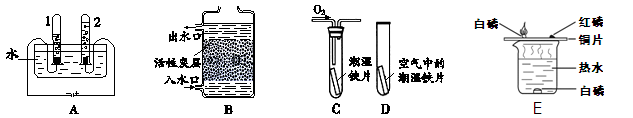
(1)根据下图回答问题。
①A图所示的是水的电解实验,试管2中收集的气体是 (填名称)。
②B图所示的是活性炭净水器的示意图,其中活性炭的作用是 。
③C、D图所示的是探究铁生锈条件的实验,一段时间后发现C中铁片变红,D中铁片依然光亮,对比C、D中的现象,说明决定铁生锈快慢的一个重要因素是: 。
④E图所示的是探究燃烧条件实验,其中热水作用 。
(2)若用质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3)配制110g质量分数为5%的氢氧化钠溶液。
①计算:需10%的氢氧化钠溶液体积为 mL。
②量取:用量筒量取氢氧化钠溶液和水,均倒入烧杯中。若量取氢氧化钠溶液读数时俯视,而其余操作均正确,这样配得的溶液的溶质质量分数会 (填“偏高”、“偏低”或“无影响”);用量筒量取水。
③混匀:用玻璃棒搅拌,使氢氧化钠溶液和水混合均匀。
④装瓶并贴上标签。
(3)某化学兴趣小组为了测定某工厂废水中硫酸的质量分数,取100g废水于烧杯中,加入上述配制好的氢氧化钠溶液80g,恰好完全反应(废水中无不溶物,其它成份不与氢氧化钠反应)。请计算废水中硫酸的质量分数。(写出计算过程)
水是一种重要的自然资源,是生活、生产必不可少的物质。
(1)如下图所示,实验室电解水的装置。实验中反应的化学方程式是 。
(2)下图是硝酸钾的溶解度曲线。某同学进行了如下实验,得到相应的溶液①~⑤。

属于饱和溶液的有 (填序号),
溶液中溶质的质量分数最大的是 (填序号)。
将盛有溶液⑤的小烧杯放入盛有水的大烧杯中,向大烧杯
内加入足量的NaOH固体,小烧杯内的现象是 。
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于大规模集成电路生产、陶瓷工业等领域。
(1)氮化铝(AlN)属于____________(填序号)。
| A.单质 | B.化合物 | C.氧化物 | D.混合物 |
(2)氮化铝(AlN)中氮元素的化合价为 。
(3)在高温条件下,氧化铝、氮气和碳反应可制得氮化铝和一氧化碳。生成的一氧化碳对空气有污染,处理该气体的方法是________________。
水是生命之源,也是人类最宝贵的资源.
(1)下列各种水中,属于纯净物的是 (填字母);
| A.汽水 | B.矿泉水 |
| C.蒸馏水 | D.经过净化处理的自来水 |
(2)饮用硬度过大的水不利于人体健康,因此人们常采用 的方法将硬水软化;
(3)小刚为了净化收集到的雨水,自制了一个如图所示的简易净水器,其中小卵石、石英砂和彭松棉的作用是 .
(4)自来水消毒过程发生的化学反应中有如下图所示的微观过程:
( 表示氯原子,
表示氯原子, 表示氧原子,
表示氧原子, 表示氢原子)
表示氢原子)
该反应中化合价发生变化的元素为 .
物质的分类标准有多种,自拟两个分类标准,将氢气,氧气,水,二氧化碳四种物质中的三种包括在标准内,而另一种不在标准内
标准一_______ _,包括的物质______ _ ;
标准二__________ ,包括的物质______________
(7分)水是我们宝贵的资源,请回答关于水的问题。
(1)净水器中经常使用活性炭,主要利用活性炭的 性。
(2)要证明某水样是硬水还是软水,可向其中加入 。
(3)通过下图实验我们认识了水是由 组成的,此反应中没有改变的微粒是(填名称) ,试管“1”中的气体是 。
(4)水是常见溶剂,现将200克30%的氢氧化钠溶液稀释为10%,需加水 ml,若用量筒量取水时俯视读数,所得氢氧化钠溶液的溶质质量分数 10%(填“大于”或“小于”)。
水和水溶液与人类的生活、生产关系密切。
①在天然水净化处理中,加活性炭的作用是 ⑻ ,很多自来水厂用二氧化氯替代氯气对水进行杀菌消毒。工业上用Cl2和NaClO2来制取二氧化氯(ClO2),请配平下列化学方程式⑼: Cl2+ NaClO2→ 2NaCl+ ClO2。
②我们用“电解水”和“氢气在氧气中燃烧”的两个探究实验来证明水的组成元素。依据下图实验回答问题:
Ⅰ.上述探究水的组成的理论依据是 ⑽ 。
Ⅱ.写出电解水的化学方程式 ⑾ ,检验正极上气体的方法是 ⑿ 。
Ⅲ.上图步骤③中集气瓶里观察到的现象是 ⒀ 。
水是人类不可缺少的资源。
(1)电解水的实验如下图所示,收集到氧气的试管是 (填“A”或“B”)。反应的化学方程式是 ,该实验说明水是由 组成的。
(2)提倡节约用水,保护水资源。下列做法合理的是 (填序号)。
a.使用节水龙头
b.使用无磷洗衣粉
c.用喷灌、滴灌方法给农作物浇水
(3)某水厂净化水的大致流程如下:
水经过沙滤池,除去的杂质是 ;炭滤池中活性炭的主要作用是 。
已知A、B、D、E、F、M是初中化学常见的几种物质,它们间有如下的转变关系(反应条件未标出)。通常情况下A是黑色固体单质,B、D是气体单质,E、F都是氧化物,F、M都是无色液体,其中M是实验室最常用的的燃料。
(1)请写出有关物质的化学式:B ;D ;F 。
(2)完成下列化学方程式:
反应① 。
反应② 。
(3)B、D、E三种气体中,工业上常用分离空气的方法制取的是 。
水与人类的生活和生产密切相关,请回答下列问题:
①图1是水通电分解的示意图,在实验过程中,试管a中产生的气体是 (11) (填名称),检验该气体的方法是 (12) 。
②图2实验中,可观察到的现象时 (13) ,若用pH试纸检测实验结束后集气瓶中水的pH应 (14) 7(填“小于”或“等于”或“大于”)。
③水是最常见的溶剂,将少量下列物质分别加入水中,不能形成溶液的是 (15) 。
A.面粉
B.白糖
C.纯碱
D.植物油
E.硝酸钾
④高铁酸钾( )是一种新型高效的多功能水处理剂。高铁酸钾受热时发生的反应为
)是一种新型高效的多功能水处理剂。高铁酸钾受热时发生的反应为 ,则R是 (16) (填化学式)。
,则R是 (16) (填化学式)。
⑤图3为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线
(I) ℃时,甲物质的溶解度为 (17) ;此温度甲物质的溶解度 (18) 乙物质的溶解度(填“>”或“=”或“<”)。
℃时,甲物质的溶解度为 (17) ;此温度甲物质的溶解度 (18) 乙物质的溶解度(填“>”或“=”或“<”)。
(II)将 ℃时接近饱和的丙溶液变成饱和溶液,能达到目的的有 (19) (填序号)。
℃时接近饱和的丙溶液变成饱和溶液,能达到目的的有 (19) (填序号)。
A.升温 B.降温
C.加溶质丙 D.与t1℃时丙的饱和溶液混合
(III) ℃时,100g甲物质的饱和溶液中含甲 (20) g(精确至0.1g)。
℃时,100g甲物质的饱和溶液中含甲 (20) g(精确至0.1g)。
(IV)当等质量甲的饱和溶液和乙的饱和溶液从 ℃降温到
℃降温到 ℃,对所得溶液的叙述正确的是 (21) (填序号)。
℃,对所得溶液的叙述正确的是 (21) (填序号)。
A.都是饱和溶液 B.溶剂质量:甲>乙
C.溶液质量:甲<乙 D.溶质质量分数:甲>乙
(7分)以下框图中的物质均为初中化学中的常见物质,其中甲、乙、丙、丁、戊均为单质,常温下,丁为黑色固体,戊为紫红色金属.农业上常用F改良酸性土壤.常温下,G是一种具有刺激性气味的气体,其水溶液显碱性,工业上用甲和丙化合制备G.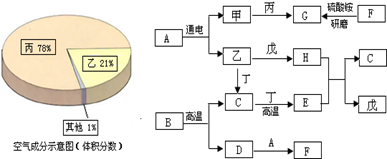
(1)写出丁、B和H的化学式:
丁 B H
(2)C、E化学性质不同,是因为:
(3)写出A分解为甲和乙的化学方程式:___________________
(4)写出F→G的化学方程式:________
(5)甲和丙化合制备G,甲和丙的质量之比为:
根据图1和图2回答下列问题。
(1)分析图1可知,在水蒸发的过程中,下列说法正确的是(填字母) ;
A.水分子不断运动 B.水分子之间间隔不变
C.氢、氧原子不发生改变 D.水分子大小改变
(2)分析图2可知,试管A中的气体为 ;B中的气体为 ;正极和负极产生的气体体积之比为 。写出水通电反应的文字表达式:_________ __ _______,该反应所属的基本类型为_ ____反应;这个反应说明水是由_ ___和_ 组成的。
(3)在电解水的过程中,下列说法不正确的是(填字母) ;
A.水分子发生了改变
B.氢原子和氧原子没有发生变化
C.水分子可以保持水的化学性质
D.水分子是由氢分子和氧分子构成的
下图是电解水的实验装置,依图回答。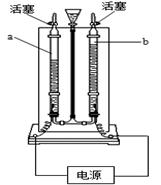
(1)在水电解器的玻璃管里注满水,接通直流电。
(2)待两只玻璃管中收集到一定量气体后,关闭电源。
(3)检验两极上产生的气体的方法是 ,其中b管的现象是 。
(4)实验结论:电解水的实验证明水是由 组成的。
水是人及一切生物生存所必需的,我们应该了解有关水的一些知识。请你回答:
(1)根据下图电解水的简易装置回答问题:
①与气体a相连的A极是电源的___极(填“正”或“负”,下同),与气体b相连的B极是电源的____极。
②正极产生的气体能使______________________;负极产生的气体能够____________。
③写出电解水的文字表达式:_________ __ _______,该反应所属的基本类型为_ ____反应;这个反应说明水是由_ ___和___ _组成的。
(2)硬水给生活和生产带来很多麻烦,生活中常用 来区分硬水和软水。生活中用 的方法将硬水软化。