水是人类生活中不可缺少的物质.
(1)净水时,通常用的方法,除去水中难溶性杂质,常用做吸附剂除去水中的色素和异味.
(2)许莹同学设计了电解水简易装置,其中
电极由金属曲别针制成.通电后的现象如图所示.
与 电极相连的试管中收集到的气体是;电解水的化学方程式为:.
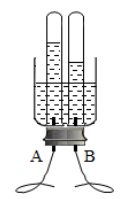
(3)自来水中含有少量
等可溶性化合物,烧水时
发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一.
受热分解的化学方程式为.
请你从微观角度解释下列问题:
(1)吸烟者常给周围的人带来被动吸烟的危害,原因是;
(2)一氧化碳和二氧化碳化学性质不同的原因是;
(3)金刚石和石墨物理性质差异很大的原因是;
(4)水通电分解的过程中一定不变的微粒是。
水与人类的生活和生产密切相关,请回答下列问题:
(1)图1是水通电分解的示意图,在实验过程中,观察到ab两试管中产生气体的体积比为 。
(2)图2实验中生成有刺激性气味的气体,该气体 (填“属于”或“不属于”)空气污染物;实验结束后,用pH试纸测量集气瓶中的液体,其pH 7(填“小于”“等于”或“大于”)。
(3)图3为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线
①t1℃时,甲物质的溶解度为 g;此温度甲物质的溶解度 乙物质的溶解度(填“>”或“=”或“<”).
②将t2℃时接近饱和的丙溶液变成饱和溶液,下列方法不能达到目的的是( )
A.蒸发溶剂 B.降低温度 C.加溶质丙 D.升高温度
③当等质量甲的饱和溶液和乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的是 (填序号).
A.都是饱和溶液 B.溶液质量:甲=乙
C.溶质质量分数:甲>乙 D.溶剂质量:甲>乙.
根据下图回答问题:

(1)水中氢元素的化合价为;
(2)图中由原子构成的物质是;
(3)酒精是由种元素组成的;
(4)图中标号①所示物质的化学式为。
化学是以实验为基础的学科,根据实验1、实验2回答下列问题:
(1)实验1的实验目的是 。
(2)实验1中发生化学反应的化学方程式是 。
(3)实验1在冷却至室温后打开弹簧夹,发现进入集气瓶内的水少于瓶内空气体积的1/5体积,原因可能是 (答一条即可)。
(4)实验2是电解水的简易装置图,电解一段时间后,甲试管中的气体体积比乙试管中的气体体积 (填“多”或“少”)。
(5)实验2说明水是由 组成的。
如图所示,实验Ⅱ是电解水的装置。
实验Ⅱ中反应的化学方程式为 。B试管中产生的气体可以使带火星的木条复燃,该气体是 .当B中气体的分子数目为n时,A中气体的分子数目为 。
水是生命的源泉,下列变化都是与水相关,请根据A、B、C、D图示回答下列问题:
(1)图A实验中,铁钉锈蚀说明生锈是铁与 作用的结果。
(2)图B实验中,检验左边试管中收集到的气体的方法是 。
(3)图C实验中,若用pH试纸检测实验结束后集气瓶中水的pH应 7(填“小于”或“等于”或“大于”)。
(4)40℃时,将50克KNO3充分溶于100克水中,形成KNO3溶液的质量是 克,若将溶液降温到20℃,溶液中溶质的质量分数是 。
物质资源是人类赖于生存的基础。
(1)水是地球上极其重要的资源之一。除去水中难溶性固体杂质的实验操作是 ;可用活性炭除去水中异味与色素,是因为活性炭具有 ;生活中能降低水的硬度的方法是 。
(2)美国航天局航天器曾实施了两次撞月,撞月激起的尘埃中含有大量以冰的形式存在的水以及银、水银、一氧化碳、二氧化碳、氨(NH3)等物质,其中属于金属单质的有 种(填数字,下同),属于氧化物的有 种。写出在月球上利用光和催化剂分解水获得氧气的化学方程式 。
水是最普通、最常见的物质之一。
(1)电解水可证明水由氢、氧两种元素组成,该反应的化学方程式为 。
(2)水是重要的溶剂和化工原料。氯碱工业以饱和食盐水为原料获得烧碱等化工产品,反应原理为: 2NaCl+2H2O  2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
①20℃时,NaCl 的溶解度是36 g。该温度下,饱和食盐水中溶质与溶剂的质量比为 。
②烧碱可用于处理硫酸泄漏,反应的化学方程式为
(3)水在化学实验中具有重要作用。先关闭K,将铁丝放在潮湿的空瓶中(如图所示),一段时间后,打开K,滴加少量的稀盐酸后,关闭 K。观察到烧杯中导气管的现象是: 。
2015年3月22日是第二十三届“世界水日”,水与人类的生活和生产密切相关,请回答下列问题:
(1)图甲是水通电分解的示意图,在实验过程中,试管a中产生的气体是 (填名称)
(2)用蒸馏水润湿的pH试纸测定碱性溶液的pH,测量结果会 (填“偏大”、“不变”、“偏小”)。
(3)今年5月,某市发生火灾时,消防队员用高压水枪灭火,此灭火原理是
(4)水是最常见的溶剂,将少量下列物质分别加入水中,不能形成溶液的是
| A.面粉 |
| B.白糖 |
| C.纯碱 |
| D.植物油 |
E.硝酸钾
(5)图乙为a、b、c三种物质的溶解度曲线
①t2°C 时将30ga物质加入到50g水中,充分溶解,所得溶液的质量为
②将t2°C时a、b、c三种物质的饱和溶液降温到t1°C,所得溶液中溶质的质量分数大小关系为
下列是初中化学中的一些重要操作或实验,请回答:
(1)A中红磷必须足量的原因是 ;
(2)B实验会看到什么现象 ;
(3)C中胶头滴管平放或倒置造成的后果是 ;
(4)D实验的目的是 。
人类的生产和生活都离不开水。
(1)如图所示的实验,试管a中得到的气体为____________;有关反应的化学方程式为____________。
(2)自来水厂净化水的过程为:取水→沉降→过滤→吸附→消毒,属于化学变化的是__________
下图为水的电解实验,关于该实验的说法正确的是
A.试管A中得到的是O2
B.试管B中的电极接电源的负极
C.试管A、B中所得气体的质量比为8∶1
D.该实验说明水是由氢元素和氧元素组成
化学从以下角度研究物质。
①组成:水中氢元素的质量分数为1/9、可用图甲的模型表示,请在图乙中画出一氧化碳中碳元素的质量分数模型 (5 ) 。
②结构:1mol水中约含有 ( 6 ) 个水分子,其中含有 ( 7 ) mol氢原子。
③性质:水具有分散性。在水中分散可形成溶液的是 ( 8 )
| A.淀粉 | B.蔗糖 | C.食盐 | D.汽油 |
④变化:电解水发生反应的化学方程式为 ( 9 ) ;图丙是电解水的微观模型图,图中缺少的微粒是 ( 10 )