如图1是a、b、c三种物质的溶解度曲线,回答下列问题:

(1)P点的含义是。
(2)
时,将50g a物质放入50g水中充分溶解得到溶液的质量为g。
(3)将
时,a、b、c三种物质的饱和溶液降温至
,所得溶液中溶质的质量分数由大到小的顺序是
(4)
时,将盛有c的饱和溶液的小试管放入盛水的烧杯中(如图2),向水中加入一定量的氢氧化钠固体后,试管中的溶液变浑浊,原因是 。
水是生命之源,水与人类生活和生产密切相关.
(1)自来水属于 (填“纯净物”或“混合物”).
(2)通过太阳能电池电解水获取氢能是绿色能源发展的方向.写出电解水的化学方程式
(3)物质溶于水,溶液的温度可能发生变化,观察图甲所示实验,判断硝酸铵溶于水时溶液的温度 (填“升高”、“降低”或“不变”).
(4)如图乙是甲物质的溶解度曲线图,据图回答:
①t1℃,要完全溶解15g甲物质至少需要水 g.
②t2℃,甲物质饱和溶液溶质的质量分数是
请你参与实验室配制一定溶质质量分数的硝酸钾溶液的实验,并进行实验过程的探究:
(1)计算:配制50g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为 g,所需蒸馏水的体积为 mL(水的密度约为1g/mL)。
(2)称量:分别在天平左右两盘放上纸片,调节平衡后,应 (填标号)。
A.先在托盘上放置所需的砝码,再添加硝酸钾直至天平平衡。
B.先添加所需的硝酸钾,再添加砝码到所在的托盘直至天平平衡。
【探究一】在称量过程中,某同学的称量操作如图所示,你认为该操作对本次实验的数据处理的正确性 (填“有”或“没有”)影响,理由是 .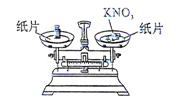
(3)量取:准确量取所需蒸馏水要用到的仪器是 (选填图中的标号)。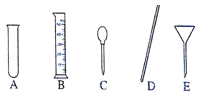
(4)溶解:将称量好的硝酸钾和蒸馏水混合溶解。
【探究二】:20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从表中找出计算所需的数据为: g/mL.
| 温度℃ 质量分数% |
20 |
40 |
60 |
| 4 |
1.023 |
1.016 |
1.007 |
| 10 |
1.063 |
1.054 |
1.044 |
根据图中
、
、
三种固体物质的溶解度曲线,回答下列问题:

(1)
℃,
的物质的溶解度为。
(2)
℃时,将接近饱和的
物质的变成该物质的饱和溶液,可采用(任填一种方法即可)。
(3)
℃时.将
、
、
三种物质的饱和溶液,分别降溫至
℃时,所得溶液中溶质质置分数的大小关系是.
| A. |
|
B. |
|
C. |
|
20℃时,将等质量的甲、乙两种固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1所示,加热到50℃时现象如图2所示,甲、乙两种物质的溶解度曲线如图3所示。

请回答下列问题:
(1)图1中一定是饱和溶液的是溶液(填"甲"或"乙");图2中乙溶液一定是溶液(填"饱和"或"不饱和")。
(2)图3中表示乙的溶解度曲线的是(填"M"或"N");图2中乙溶液降温至30℃析出晶体(填"会"或"不会")。
(3)50℃时甲的饱和溶液中溶质质量分数为(计算结果精确到0.1%)。
已知
、
、
三种物质的溶解度曲线如图1,根据题意回答下列问题。

(1)下列说法中,正确的是.
| A. | 与 相比, 的溶解度大于 的溶解度 |
| B. |
在 时, 与 的溶解度相等 |
| C. |
时,将30g 物质溶于50g溶剂中,可得到80g溶液 |
| D. |
从 降温至 时, 有晶体析出 |
(2)如图2所示,将盛有
物质饱和溶液的试管置于盛有适量水的烧杯中,需向烧杯内加入下列哪种物质,才能使试管内的饱和溶液变为不饱和溶液.
| A. |
浓 |
| B. |
氢氧化钠 |
| C. |
蔗糖 |
| D. |
食盐 |
| E. |
硝酸铵 |
如图为甲、乙两种物质的溶解度曲线,请回答下列问题。
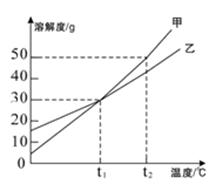
(1)t1℃时,甲物质的溶解度(填">"、"="或"<")乙物质的溶解度。
(2)t2℃时,把50g乙物质放入100g水中,充分搅拌得到的是(填"饱和"或"不饱和")溶液。
(3)t2℃时,有一接近饱和的甲溶液,可采用的方法使它变为该温度下的饱和溶液。
物质甲、乙的溶解度随温度变化图象如图所示,根据如图回答问题:
(1)由图你能获得哪些信息
①;②。
(2)20℃时,将50克甲溶于100克水中,所得溶液为溶液(填"饱和"、"不饱和"溶液)。
(3)40℃时,甲、乙两种物质的溶解度大小关系:甲乙(填">"、"<"或"=")。

、
、
三种固体物质在水中的溶解度曲线如图所示,请回答:

(1)℃时,
、
两种物质在100
水中达到饱和状态时溶解的质量相等;
(2)若
中混有少量的
,最好采用的方法提纯
;
(3)现有接近饱和的
物质溶液,使其变成饱和溶液的方法有:①加入
物质;②恒温蒸发溶剂;③;
(4)
℃时将20
物质放入50
水中,充分搅拌,所得溶液中溶质的质量分数是;
(5)将
℃时等质量的
、
、
三种物质的饱和溶液降温至
℃时,所得溶液的质量由大到小的顺序是。
甲、乙两图分别表示氯化钠和硝酸钾在水中的溶解度曲线。

(1)比较甲、乙两图可知:影响固体物质溶解度曲线陡斜程度的因素是,两物质中的溶解度受温度影响更小。
(2)20
时硝酸钾的溶解度为。
(3)若将20
时硝酸钾的饱和溶液升温到50
,此时溶液为(填"饱和溶液"或"不饱和溶液"),溶液中硝酸钾的质量分数(填"变大"、"变小"或"不变")。
为准确配制80g10%的氯化钠溶液,要尽量减小计量仪器称量时的误差。该实验用到了下列仪器,其中属于计量仪器的是()





| A. | ①⑤ | B. | ③④⑤ | C. | ①③④⑤ | D. | ①②③④⑤ |
如图所示,
、
、
为三种物质的溶解度曲线,请根据图示信息回答下列问题。

(1)
℃时,
、
、
三种物质中溶解度最小的是。
(2)
℃时,将20
物质投入100
水中,充分溶解,温度不变,所得溶液为溶液(填"饱和"或"不饱和")。
(3)下列说法正确的是。
| A. |
℃时,将 和 的混合溶液(两者均已达到饱和),降温到 ℃,析出的晶体含有 和 |
B. | 从混有少量 的 物质中提取较纯净的 ,可通过冷却它们的热饱和溶液实现 |
| C. |
℃时,将 、 、 的饱和溶液分别降温到 ℃,所得溶液中溶质质量分数的大小关系是 > > |
D. | ℃时,欲用 的饱和溶液配制10%的 溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器 |
(4)如图所示,向放有镁条的试管中滴加稀盐酸后,锥形瓶中
的饱和溶液变浑浊。请解释原因。

下列实验方案的设计中,没有正确体现对比这种科学思想的是
 |
 |
 |
 |
| 比较二氧化碳的含量 |
研究二氧化锰的催化作用 |
区分硬水和软水 |
配制氯化钠溶液 |
下图为甲、乙两种物质的溶解度曲线,请回答下列问题:
(1)20℃时,为使接近饱和的甲物质溶液变为饱和溶液的方法是: (任写一种方法即可);
(2)40℃时,乙物质的溶解度是____g。此温度下,该饱和溶液中乙物质的质量分数是 (精确到0.1%)。
下列图像不能正确反映其对应关系的是()
| A. |
|
| B. |
|
| C. |
|
| D. |
|