2014年3月22日是第二十二个“世界水日”,它的主题是“水与能源”。关于水的知识有下列话题,请按要求填空:
①自来水生产过程中,可加 (7) (填写物质化学式)方法进行消毒杀菌。
②测定地下水的酸碱度常用 (8) 。
③水是最常用的溶剂。实验室用蔗糖配制一定溶质质量分数的溶液时,已经有以下仪器:玻璃棒、天平、烧杯、胶头滴管,还需要的仪器是 (9) 。配置好的蔗糖溶液可以保存较长时间,这体现了溶液的
(10) 性。
④保护水环境、珍爱水资源,是每个公民应尽的责任和义务。下列做法有利于保护水资源的是 (11) (填写选项编号)。
| A.大量使用化肥农药 | B.工业废水处理达标后再排放 |
| C.使用含磷洗衣粉 | D.生活污水直接排放 |
⑤科学家们在实验室中利用催化剂在光照条件下进行水的分解反应,以得到清洁能源。写出该反应化学方程式 (12) 。
下图为硝酸钾(KNO3)和氯化钠(NaCl)两种物质溶解度曲线。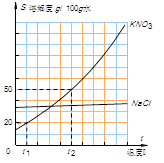
①t1℃时,两种物质溶解度的大小关系:S(NaCl) (15) S(KNO3)(填“>”、“=”或“<”)。
②t2℃时,将25g氯化钠固体投入50g水中,充分溶解后可得到的氯化钠溶液是 (16) (填“饱和溶液”或“不饱和溶液”)。
③t1℃时,硝酸钾溶解度为 (17) 。若将该温度下硝酸钾饱和溶液加水稀释后不发生改变的是 (18) (填字母)。
| A.溶剂质量 | B.溶质质量 |
| C.溶质质量分数 | D.硝酸钾的溶解度 |
④某硝酸钾溶液中含有少量氯化钠杂质,要提纯得到较纯净的硝酸钾固体的主要步骤依次是: (19) 、 (20) 、 (21) 、洗涤、烘干。
⑤t℃时,在100g25%的硝酸钾溶液中加入硝酸钾固体,所加硝酸钾固体质量(m)与溶液的溶质质量分数(C%)的关系如图所示,x= (22) (精确到0.1%);t与t1、t2的关系是 (23) 。(填编号)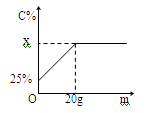
Ⅰ.t<t1 Ⅱ.t1<t<t2 Ⅲ.t>t2
华雪同学想制取“叶脉书签”,需要50g质量分数为10%的氢氧化钠溶液。请回答下列问题:
(1)若用氢氧化钠固体配制,需称取氢氧化钠 g。
(2)若用25%的氢氧化钠溶液配制,需25%的氢氧化钠溶液 g;蒸馏水 g;配制时应选
用 mL(选填“10”、“20”、“50”、“100”)的量筒量取蒸馏水。
(3)下列操作正确的是 。
A.在托盘天平的左右托盘上垫滤纸称取氢氧化钠固体
B.将准确称取的氢氧化钠固体直接倒入装有水的量筒中溶解
C.将配制好的NaOH溶液装入玻璃试剂瓶中,塞好橡胶塞并贴上标签
(4)在实验室配制氢氧化钠溶液时, (填“要”或“不要”)用到玻璃棒。
某校环保小组为监测某厂排出的污水中重金属离子的含量,需配制11%的氯化钠溶液100g。学生小明按下图步骤顺序操作:
(1)这些操作步骤中有错误的是 (填字母编号)。
(2)溶液配制过程中除如图所示的装置外,还需用到的仪器有 等。
(3)上述仪器中上述错误导致所配溶液的溶质质量分数 1l%(填大于、小于或等于),所得溶液的质量 (填偏高、偏低或不一定)
(4)请选择操作中的一处错误纠正为 。
配置150g16%的氯化钠溶液需氯化钠 克,水 ml;若用24% 的氯化钠溶液配置,需24% 的氯化钠溶液 克。
某同学做无土栽培实验时,配制营养液的主要试剂之一是质量分数为1.4%的KNO3的溶液,现欲配制这种KNO3溶液200g。
(1)如图所示,本次实验需要用到的实验仪器有 、 。(填仪器名称)
(2)本次实验中,需要称量的KNO3的质量是 g。
(3)在实验过程中,如果托盘天平出现了右盘低的现象,接下来的操作应是 。(填字母)
| A.将左边的平衡螺母向左调 | B.在右盘中添加砝码 |
| C.向左移动游码 | D.在左盘中增加KNO3 |
(4)最后在溶解时,用玻璃棒搅拌的目的是 。
实验室配制50克质量分数为12%的氯化钠溶液。下图是小军实验操作过程示意图:
(1)图中一处明显错误的操作是 (填序号),该错误操作会导致所得溶液的溶质质量分数 (填“偏大、偏小”),改正操作后,用上述图示的序号表示配制溶液的正确操作顺序 。
(2)图①中玻璃棒搅拌的目的是 。
(3)配制时应选择 (填“10” “50”或 “100”)mL的量筒来量取所需水的体积,使用量筒时正确的读数方法为 。
实验室配制50克质量分数为12%的氯化钠溶液。下图是小军实验操作过程示意图:
(1)图中一处明显错误的操作是 (填序号),该错误操作会导致所得溶液的溶质质量分数 (填“偏大、偏小”),改正操作后,用上述图示的序号表示配制溶液的正确操作顺序 。
(2)图①中玻璃棒搅拌的目的是 。
(3)配制时应选择 (填“10”“50”或“100”)mL的量筒来量取所需水的体积,使用量筒时正确的读数方法为 。
实验室用37%的浓盐酸(1.18g/ml)配制成118 g18.5%稀盐酸。
需37%的浓盐酸 ml;水 ml
欲配制120g质量分数为22.5%的NaCl溶液,步骤如下:
(1)计算:需要NaCl的质量为 g;
(2)称量:称量前,应先调节天平 ;用量筒来量取所需的水(水的密度为1g/cm3)时,应选择 (10mL、100 mL、200 mL)的量筒;
(3)溶解:溶解时,需用玻璃棒搅拌,目的是 ;
(4)反思:读取量筒中水的体积时,若仰视读数,则配得的溶液中NaCl质量分数将 (填“偏大”、“偏小”或“无影响”);称量NaCl时,若将NaCl和砝码位置颠倒,则配得的溶液中NaCl质量分数将 (填“偏大”、“偏小”或“无影响”) (注:1g以下用游码);
水和溶液在生命活动和生活中起着十分重要的作用。根据下面的溶解度表与溶解度曲线,回答下列问题:
(1)A是__________的溶解度曲线。
(2)80℃时,100g水中加入120g硝酸钾,所得溶液是__________(填“饱和”或“不饱和”),当80℃的该溶液降温到20℃时,析出晶体的质量为__________g。
(3)硝酸钾中混有少量的氯化钠,想要得到纯净的硝酸钾的方法是__________。
(4)60℃时,向两个分别盛有50g NaCl和KNO3的烧杯中,各加入100g的水,充分溶解后成为饱和溶液的是__________溶液;将上述烧杯中剩余固体全部溶解,变为不饱和溶液,下列方法能实现的是__________(填字母序号)。
| A.升温 |
| B.加入该溶质 |
| C.加入适量水 |
| D.降温 |
E.加入足量该溶质的不饱和溶液
(5)如下图所示,烧杯A中是饱和的氢氧化钙溶液,向烧杯B中加入生石灰后,烧杯A中变浑浊,原因是____________________________________。
甲、乙、丙三种固体物质的溶解度曲线如图所示,
请回答:
(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得 到溶液的质量为 g。
(2)若甲固体中含有少量乙,则提纯甲的方法是 (填“蒸发结晶、降温结晶”之一)。
(3)将25℃时乙的饱和溶液升温到35℃,则其溶液的溶质质量分数 (填“变大”、“变小”或“不变”)。
(4)35℃时,分别用等质量的甲、乙、丙配制该温度下的饱和溶液,所得溶液的质量最小的是 。
(5)如图所示,35℃时,A、B两试管中分别盛有甲、丙的饱和溶液,并都有少量固体存在。若向试管外盛有水的烧杯中加入某固体物质后,A试管内固体明显减少,B试管内固体逐渐增多。
则加入的物质可能是 (写出一种物质的化学式)。
下图为硝酸钾和氯化钠的溶解度曲线。由图可知:
(1)当温度为30℃时,硝酸钾的溶解度 (填“>”、“<”或“=”)氯化钠的溶解度。
(2)当硝酸钾中含有少量氯化钠时,可用 法提纯硝酸钾。
(3)硝酸钾、氯化钠都属于 (填“易溶”、“可溶”、“微溶”或“难溶”)物质。
(4)10℃时,将12g硝酸钾加入50g水中不断搅拌,形成溶液是 (填“饱和”或“不饱和”)溶液,溶液质量为 。
某实验小组利用图中所示仪器配制一定溶质质量分数的氯化钠溶液。
(1)图1中缺少一种必须用到的玻璃仪器仪器名称是:______________;用途是:___________________;
(2)量取蒸馏水的体积读数如图3所示,则量取的水的体积为:___________。
(3)该小组原计划配制的溶液中溶质与溶剂之比______________________。