某溶液溶质的质量分数为20%,加入50g水后变为10%,则稀释后溶液中溶质的质量是
| A.5g | B.10g | C.20g | D.50g |
小王同学需配制100g 12%的NaOH溶液来制作“叶脉书签”。在配制溶液过程中,下列做法正确的是( )
| A.在托盘上垫上纸并称取12g NaOH固体 |
| B.称量时发现指针向右偏转,应调节游码使天平平衡 |
| C.用100mL量筒量取88mL水 |
| D.把称取的NaOH固体直接倒入装有88mL水的量筒中溶解 |
某粗心的同学在做“配制一定溶质质量分数的溶液”时,部分操作如下,其中操作明显有误的一项是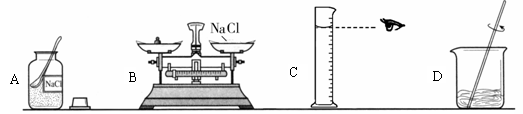
下列实验操作正确的是
| A.“物质燃烧的条件”实验中,用玻璃杯罩住燃着的蜡烛以降低蜡烛的着火点 |
| B.“粗盐的初步提纯”实验中,进行蒸发操作时,当出现大量固体时,用玻璃棒搅拌 |
| C.“配制一定溶质质量分数的NaCl溶液”实验中,量取一定的水时俯视读数,则所配制溶液溶质质量分数偏小 |
| D.“高锰酸钾制取氧气”实验中,收集好气体后应先将导管移出水槽再停止加热 |
可以证实某硝酸钾溶液是20℃时的饱和溶液的事实是
| A.降温到10℃时,有硝酸钾晶体析出 |
| B.蒸发掉10g水,有硝酸钾晶体析出 |
| C.20℃时,向原溶液中加入少量硝酸钾晶体,溶液中硝酸钾的质量分数不变 |
| D.加热到30℃后,再加入硝酸钾晶体能继续溶解 |
用固体氯化钠配制50g溶质质量分数为6%的氯化钠溶液。下列有关说法正确的是
| A.选择的玻璃仪器有烧杯、50mL量筒、玻璃棒、胶头滴管、试剂瓶 |
| B.将氯化钠直接放在托盘天平左盘上称量为3.0g |
| C.用内壁附有水珠的烧杯配制溶液 |
| D.转移已配制好的溶液时,有少量溶液溅出会使溶液中氯化钠的质量分数减小 |
小明在实验室配置16%的食盐溶液时,下列操作对实验结果无影响的是
①固体倒入烧杯后,称量纸上有残留
②量取水时,量筒内有水
③溶解用的烧杯内有水
④水倒入烧杯溶解时洒出少许
⑤溶液向细口瓶转移时洒出少许
| A.①② | B.②⑤ | C.③④ | D.③⑤ |
向100克溶质质量分数为20%的硝酸钾溶液中加入100克水,所得溶液中溶质质量分数是( )
| A.5% | B.10% | C.20% | D.40% |
泡菜具有独特的风味,适合制作泡菜的食盐水浓度是4%.在配制4%的食盐水时,会导致溶液的溶质质量分数偏小的是
①称量好的食盐倒入烧杯时,有少许洒出 ②量水的体积时,俯视量筒
③溶解食盐的烧杯内壁是潮湿的 ④用4g食盐和100g水配制溶液.
| A.②③ | B.①③④ | C.①②③ | D.①②③④ |
在配制10%的氯化钠溶液的过程中,导致溶液中氯化钠质量分数小于10%的可能原因是
①用量筒量取水时俯视读数
②配制溶液的烧杯用少量蒸馏水润洗
③在托盘天平的左盘称取氯化钠时,游码不在零位置就调节天平平衡,后将游码移动得到读数
④盛装溶液的试剂瓶用蒸馏水润洗
⑤氯化钠晶体不纯.
| A.①②③④⑤ | B.只有①②④⑤ | C.只有①②③ | D.只有②③④⑤ |
白酒的 “度数”指的是白酒中酒精的含量。这里的含量不是指质量分数,而是体积分数。例如,52度(520)的白酒表示100ml白酒中含有52ml酒精(常温时)。蒸馏水密度为1g/cm3,酒精密度为0.8g/cm3,若为40度(400)的白酒溶液中溶质的质量分数约为
| A.40% | B.60% | C.34.8% | D.无法判断 |
一定温度下,一定质量的氢氧化钠固体溶于水制成溶液.下列有关的量不随水的质量改变而改变的是( )
| A. | 溶液质量分数 | B. | 溶液的 |
| C. | 氢氧化钠的溶解度 | D. | 最多能吸收二氧化碳的质量 |
在实验室配制质量分数一定的氯化钠溶液时,有下列图示的操作,其中肯定错误的是
现欲将粗盐提纯,再配制质量分数一定的氯化钠溶液,下列说法正确的是
| A.过滤时玻璃棒轻轻斜靠在单层滤纸一边 |
| B.配制溶液时需要经过计算、称量(量取)、溶解、装瓶等步骤 |
| C.蒸发滤液时,待蒸发皿中滤液蒸干时,即停止加热 |
| D.配制溶液时必备的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等 |