右图是一款笔记本电脑所用甲醇燃料电池的结构示意图。
甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2 = 2CO2+4H2O下列说法正确的是()
| A.右电极为电池的正极,b处通入的物质是空气 |
| B.左电极为电池的负极,a处通入的物质是空气 |
| C.正极反应式为:CH3OH+H2O-6e-= CO2+6H+ |
| D.正极反应式为:O2+2H2O+4e-=4OH- |
根据下列实验现象,所得结论正确的是
| 实验 |
实验现象 |
结论 |
| A |
左边烧杯中镁表面有气泡,右边烧杯中铜表面有气泡 |
还原性: Al>Mg>Cu |
| B |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
| C |
试管中白色固体先变淡黄色,后变为黄色 |
沉淀转化的实质就是沉淀溶解平衡的移动 |
| D |
锥形瓶中有气体产生,烧杯中溶液变浑浊 |
非金属性:Cl>C>Si |
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是( )
| A.标准状况下,11.2L的戊烷所含的分子数为0.5×6.02×1023 mol-1 |
| B.28g乙烯所含共用电子对数目为4×6.02×1023 mol-1 |
| C.1mol 苯中含有碳碳双键的数目为3×6.02×1023 mol-1 |
| D.2.8g聚乙烯中含有的碳原子数为0.2×6.02×1023 mol-1 |
《青花瓷》中所描绘的“瓶身描绘的牡丹一如你初妆”、“色白花青的锦鲤跃然于碗底”等图案让人赏心悦目,但古瓷中所用颜料成分一直是个谜,近年来科学家才得知大多为硅酸盐,如蓝紫色的硅酸铜钡(BaCuSi2Ox,铜为+2价),下列关于硅酸铜钡的说法不正确的是
| A.可用氧化物形式表示为BaO·CuO·2SiO2 | B.性质稳定,不易脱色 |
| C.易溶解于强酸和强碱 | D.x等于6 |
已知:
①不对称烯烃与不对称加成物在不同的条件下有不同的加成方式,如: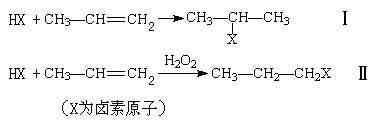
②烃基上的卤素原子在一定条件下能发生取代反应,如: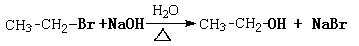
也能发生消去反应,如: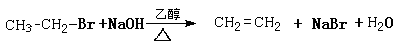
对溴苯乙烯(Br CH=CH2)与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。
CH=CH2)与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。
完成下列填空:
(1)写出该共聚物的结构简式
(2)实验室由乙苯制取对溴苯乙烯,需先经两步反应制得中间体Br CHBrCH3。
CHBrCH3。
写出该两步反应所需的试剂及条件。
(3)将Br CHBrCH3与足量氢氧化钠溶液共热得到A,得到A时,苯环上没有化学键的断裂和生成。
CHBrCH3与足量氢氧化钠溶液共热得到A,得到A时,苯环上没有化学键的断裂和生成。
写出生成A的化学方程式 。
由上述反应可推知 。
由A生成对溴苯乙烯的反应方程式为 。
(4)丙烯催化二聚得到2,3-二甲基-1-丁烯,B与2,3-二甲基-1-丁烯互为同分异构体,且所有碳原子处于同一平面。写出B的结构简式。 ,1molB完全燃烧时耗氧___________mol
完成下列获得B的化学方程式(条件错误不得分):
①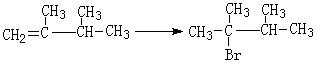
________________________________________________
②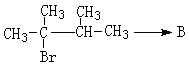
_________________________________________________
已知维生素A的结构简式如下图,关于它的叙述中不正确的是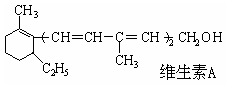
| A.维生素A的一个分子中有五个双键 |
| B.维生素A的一个分子中有30个氢原子 |
| C.维生素A能使溴水褪色,能被酸性KMnO4氧化 |
| D.维生素A是一种烯烃 |
某化工厂以丙烯、乙烯为原料进行化工生产的主要流程如下。下列有关说法错误的是( ) ,其中
,其中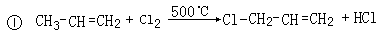
| A.反应①与反应④均是取代反应 |
| B.反应②与反应③均是加成反应 |
| C.反应②中产物的结构简式为CH2BrCH2CHClBr |
| D.反应③、④表明硫酸是乙烯与水反应的催化剂 |
如图,A为直流电源,B为电解槽,c、d为石墨电极,B中存放有100mL NaCl和CuCl2的混合溶液,其中Cu2+的物质的量浓度为0.1mol/L,闭合K,d极收集到标准状况下448mL的一种气体甲,该气体能使湿润的碘化钾淀粉试纸变蓝。气体体积均
在标准状况下测定,假设溶液的体积变化忽略不计,不考虑
电解产生的气体溶解和吸收。请回答下列问题。
(1)A电源的a极是
(2)计算c极理论上收集到的气体的体积是 (标准状况下)。
(3)假设100mL溶液中,c(Cu2+)="a" mol/L,c(Na+)="b" mol/L,Cu2+完全放电后,理论上d极产生甲气体的体积V范围是 (用带a、b的代数式表示)。
请从下图中选出必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积(大于25mL),并检验氯气的氧化性。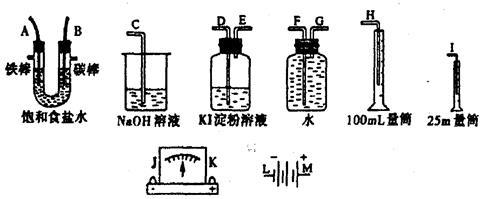
(1)电源、电流表,与A、B两极的正确连接顺序为L→J→K→( )→()→M。
(2)B极发生的电极反应式是 。简述检验该电极产物的方法和现象 。
(3)设计上述气体实验装置时,各接口的正确连接依序为:检验氯气的氧化性时B接D 、E接C。测定产生的氢气的体积时A接_________、_________接__________。
(4)若电解饱和食盐水50mL,通电为t min时,测得产生的H2体积为 5.6mL(标况),则此时溶液的pH为 。(忽略溶液体积的变化)
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选用酚酞作指示剂。请填写下列空白:
(1)酸式滴定管用蒸馏水洗涤后,直接注入标准盐酸溶液进行滴定,则测得的结果________(填“偏高”、“偏低”或“无影响”)。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察____________。
A. 滴定管内液面的变化 B. 锥形瓶内溶液颜色的变化
(3) 滴定结果如下表所示:
| 滴定次数 |
待测溶液NaOH的 体积/mL |
标准盐酸溶液的体积/mL |
|
| 滴定前刻度 |
滴定后刻度 |
||
| 1 |
25.00 |
0.00 |
26.11 |
| 2 |
25.00 |
1.56 |
30.30 |
| 3 |
25.00 |
0.22 |
26.31 |
若盐酸标准溶液的浓度为0.1000 mol·L-1,则该NaOH溶液的物质的量浓度为_________ mol·L-1。
下列各物质转化关系如图所示,A是一种高熔点固体,D是一种红棕色固体。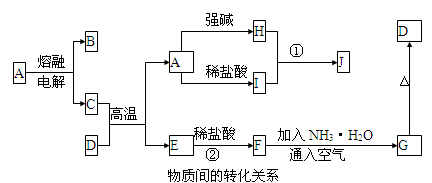
根据上述一系列关系回答:
(1)填写物质的化学式:B , G 。
(2)写出D物质中金属元素基态原子的核外电子排布图 。
(3)写出下列反应的离子方程式:
①H溶液和I溶液混合生成J___________ 。
②E和盐酸反应 。
(4)在电解熔融状态A的过程中,当电路中通过1mol电子时,阳极上产生的气体体积为 L。(标准状况下)
常温下,将0.01 mol CH3COONa 和0.002 molHCl溶于水,形成1L混合溶液:
(1)该溶液中存在三个平衡体系,用电离方程式或离子方程式表示①和②:
① 。
② 。
③CH3COOH CHCOO-+H+。
CHCOO-+H+。
(2)溶液中共有 种不同的粒子(指分子和离子),在这些粒子中,浓度为0.01 mol/L的是 ,浓度为0.002 mol/L的是 。
(3)在上述溶液中,存在的两个守恒关系是:
①物料守恒,C(CH3COO-)+C(CH3COOH)= mol/L;
②电荷守恒,即: 。
物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡。请根据所学知识回答下列问题:
(1)NaHCO3溶液中共存在7种微粒,它们是Na+、HCO3-、H+、CO32-、H2O、 、 。(填写微粒符号)
(2)常温下,物质的量浓度均为0.1mol/L的六种溶液①NH4NO3、②NaCl、③NaClO、④H2SO4、⑤NaOH、⑥CH3COONa,pH从大到小排列顺序为 。(填写溶液的序号)
(3)常温时,AlCl3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(4)常温下,物质的量浓度相同的下列溶液 :①NH4Cl、② (NH4)2SO4、 ③NH3·H2O ④ (NH4)2CO3、⑤ NH4HSO4。溶液中c(NH4+)从大到小的顺序为: 。(填写溶液的序号)
下图所示水槽中的试管内有一枚铁钉(含少量的炭),放置数天后观察:
(1)若试管内液面上升,则铁钉发生了 腐蚀,
正极反应式为 。
(2)若试管内的液面下降,则铁钉发生了 腐蚀,
负极反应式为 ,正极反应式为 。