对于化学反应的限度的叙述不正确的是()
| A.任何可逆反应都有一定的限度 |
B.对于反应2SO2(g)+O2(g) 2SO3(g)只有达到限度时才有2v(O2)=v(SO3) 2SO3(g)只有达到限度时才有2v(O2)=v(SO3) |
C.对于反应2SO2(g)+O2(g) 2SO3(g)达到限度时,增大容器容积能减小正反应速率 2SO3(g)达到限度时,增大容器容积能减小正反应速率 |
| D.化学反应达到限度时,正逆反应速率相等 |
实验是研究化学的基础,下列有关实验的方法、装置或操作都正确的是()
| A.用甲装置将海带灼烧成灰 |
| B.分离Na2CO3溶液和CH3COOC2H5,可使用如图乙所示实验装置 |
| C.利用丙装置进行石油分馏 |
| D.利用丁装置检验装置的气密性 |
分类法是学习和研究化学的一种常见的科学方法,以下分类合理的是()
| A.根据酸分子中的氢原子个数将酸分为一元酸、二元酸、多元酸 |
| B.根据溶液导电能力的强弱将电解质分为强电解质和弱电解质 |
| C.盐酸、醋酸既是化合物又是酸 |
| D.甘油不是油、纯碱不是碱、干冰不是冰 |
下表中对应关系正确的是()
| A |
CH3CH3+Cl2 CH3CH2Cl+HCl CH3CH2Cl+HClCH2=CH2+HCl→CH3CH2Cl |
均为取代反应 |
| B |
由油脂得到甘油,由淀粉得到葡萄糖 |
均发生了水解反应 |
| C |
Cl2+2Br-=2Cl-+Br2 Zn+Cu2+=Zn2++Cu |
均为单质被还原的置换反应 |
| D |
2Na2O2+2H2O=4NaOH+O2↑ Cl2+H2O=HCl+HClO |
均为水作还原剂的氧化还原反应 |
X、Y、Z三种元素的原子,其最外层电子排布分别为3s1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式为()
| A.X2YZ3 | B.XYZ2 | C.X2YZ2 | D.XYZ3 |
下列化学用语的书写正确的是()
A.基态Mg原子的核外电子排布图: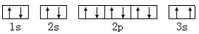 |
B.过氧化氢的电子式: |
| C.As原子的简化电子排布式:[Ar]4s24p3 |
D.羟基的电子式: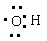 |
按电子排布,可以把周期表中的元素划分成几个区()
| A.4个 | B.5个 | C.6个 | D.7个 |
研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1∆H < 0(I)
NaNO3(s)+ClNO(g) K1∆H < 0(I)
2NO(g)+Cl2(g) 2ClNO(g) K2∆H < 0 (II)
2ClNO(g) K2∆H < 0 (II)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向 2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。测得10min内V(ClNO)=7.5×10-3mol•L-1•min-1,则平衡后n(Cl2)= mol,NO的转化率а1= 它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率а2 а1(填“>”“<”或“=”),平衡常数K2 (填“增大”“减小”或“不变”)。若要使K2减小,可采用的措施是 。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得 1L溶液A,溶液B为0.1mol•L‾1的CH3COONa溶液,则两溶液中c(NO3‾)、c(NO2-)和c(CH3COO‾)由大到小的顺序为 。(已知HNO2的电离常数Ka=7.1×10-4mol•L‾1,CH3COOH的电离常数Ka=1.7×10-5mol•L‾1,可使溶液A和溶液B的pH相等的方法是 。
| A.向溶液A中加适量水 | B.向溶液A中加适量NaOH |
| C.向溶液B中加适量水 | D.向溶液B中加适量NaOH |
(4)在25℃下,将a mol•L﹣1的氨水与0.01mol•L﹣1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl﹣).则溶液显 (填“酸”“碱”或“中”)性;用含a的代数式表示NH3•H2O的电离常数Kb= 。
(5)水溶液中的行为是中学化学的重要内容.已知下列物质的电离常数值:
HClO:Ka=3×10﹣8 HCN:Ka=4.9×10﹣10 H2CO3:Ka1=4.3×10﹣7 Ka2=5.6×10﹣11
84消毒液(有效成份为NaClO)中通入少量的CO2,该反应的化学方程式为 。
CuCl2溶液中的铜主要以Cu (H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu (H2O)42+(蓝色)+4Cl- CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题: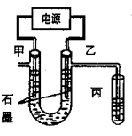
(1)甲电极的电极反应式为_________________。
(2)丙中溶液变蓝是乙电极产物与KI反应导致的,该反应的化学方程式为_________________。
(3)随电解的不断进行,U型管中溶液的颜色变化为__________;
A.由黄色变为浅蓝色 B.由蓝色变为浅黄色
溶液颜色变化的原因是_________________。
(4)当电解到一定程度,甲电极附近出现蓝色Cu(OH)2絮状物。经测,甲电极附近溶液的pH=a,此时甲电极附近c(Cu2+)="________" mol·L-1。(已知:Cu(OH)2的Ksp=2.2*10-20)。
某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol·L-1的标准NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
⑥重复以上滴定操作2-3次。
请回答:
(1)以上步骤有错误的是(填编号)____________,该错误操作会导致测定结果_____________(填“偏大”、“偏小”或“无影响”)。
(2)步骤④中,量取20.00mL待测液应使用__________________(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果____________(填“大”、“偏小”或“无影响”)。
(3)步骤⑤滴定时眼睛应注视_______________;判断到达滴定终点的依据是:_________________。
(4)以下是实验数据记录表
| 滴定次数 |
盐酸体积(mL) |
NaOH溶液体积读数(mL) |
|
| 滴定前 |
滴定后 |
||
| 1 |
20.00 |
0.00 |
18.10 |
| 2 |
20.00 |
0.00 |
16.30 |
| 3 |
20.00 |
0.00 |
16.22 |
从上表可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是()
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视读数
(5)根据上表记录数据,通过计算可得,该盐酸浓度为:____________mol·L-1
(1)室温下,有一pH=12的NaOH溶液100mL,欲使它的pH降为11。
①如果加入蒸馏水,就加入________mL
②如果加入pH=10的NaOH溶液,应加入_________mL
③如果加入0.008mol/LHCl溶液,应加入__________mL
(2)实验室在配制溶液时,一些物质存在水解的情况,如在配制Na2CO3溶液时,CO32-会水解,请书写水解离子方程式,在配制Al2(SO4)3溶液时,Al3+也存在水解,请书写水解离子方程式,为了防止Al2(SO4)3发生水解,可加入少量的。
(3)工业上用氧化铜制备氯化铜时,先将制的氧化铜(含有杂质FeO)用浓酸溶解得到的氯化铜(溶液中含有一定量的Fe2+)。
| 金属离子 |
pH值 |
|
| 开始沉淀 |
完全沉淀 |
|
| Fe2+ |
7.6 |
9.6 |
| Cu2+ |
4.4 |
6.4 |
| Fe3+ |
2.7 |
3.7 |
实际生产中先用次氯酸钠将Fe2+氧化成Fe3+,然后用试剂将溶液pH值调至 ~ ,即可除去铁杂质。
25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.6×10-9。该温度下,下列说法不正确的是
| A.同浓度的Na2SO4和Na2CO3混合溶液中滴加BaCl2溶液,BaSO4先析出 |
| B.BaCO3的悬浊液中加入少量的新制氯水,c(Ba2+)增大 |
C.BaSO4和BaCO3共存的悬浊液中,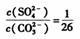 |
| D.BaSO4悬浊液中加入Na2CO3浓溶液,BaSO4不可能转化为BaCO3 |
已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10。现向1L0.2mol·L-1HF溶液中加入1L0.2mol·L-1CaCl2溶液,则下列说法中,正确的是
| A.25℃时,0.1mol·L-1HF溶液中pH=1 |
| B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.加入CaCl2溶液后体系中的c(H+)浓度不变 |
| D.该体系中有CaF2沉淀产生 |