已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为__________,该元素的符号是__________;
(2)Z元素位于元素周期表________区,目前该元素发现________种同位素;
(3)X与Z可形成化合物XZ3,该化合物的空间构型为__________;
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是__________;
(5)X的氢化物与同族第二、第三周期元素所形成的氢化物沸点由高到低顺序是(用化学式表示)______.
回答下问题:
(1)C、N、O三种元素的第一电离能由大到小的顺序是__________________。
(2)C、Si、N的电负性由大到小的顺序是__________________。
(3)氟化氢水溶液中存在的氢键有_________种。
(4)金属镍及其化合物在合金材料以及催化剂等方面应用广泛,Ni的基态原子有________种能量不同的电子。很多不饱和有机物在Ni催化下可以H2发生加成反应。如①CH2=CH2、②HC≡CH、③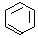 、④HCHO,其中碳原子采取sp2杂化的分子有__________(填物质编号),HCHO分子的立体构型为______________。
、④HCHO,其中碳原子采取sp2杂化的分子有__________(填物质编号),HCHO分子的立体构型为______________。
回答下问题:
(1)下列说法不正确的是______________(填字母序号)。
| A.铝的氧化物属于碱性氧化物 |
| B.光纤制品的基本原料为SiO2 |
| C.用热的纯碱溶液洗涤沾有油污的器具时发生的主要是化学变化 |
| D.液氨、液氯、液态氯化氢都是非电解质 |
E.丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
F.化学变化前后原子的种类、数目不变,分子数目也不变
(2)出土的青铜器大多受到魂晶腐蚀,某青铜器中Sn、Pb的质量分别为119g、20.7g,则该青铜器中Sn和Pb原子的数目之比为______________。采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分CuCl发生复分解反应,该化学方程式为____________。
(3)KNO3中NO3-的空间构型为__________,写出与NO3-互为等电子体的另一种阴离子的化学式:__________。
(4)已知配合物CrCl3·6H2O中心原子Cr3+配位数为6,向含0.1molCrCl3·6H2O的溶液中滴加2mol/LAgNO3溶液,反应完全后共消耗AgNO3溶液50mL,则该配离子的化学式为________。
向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150mL4mol/L的稀硝酸恰好使混合物完全溶解,放出2.24LNO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为
| A.0.21mol | B.0.25mol | C.0.3mol | D.0.35mol |
下列说法不正确的是
| A.某金属元素气态基态原子的逐级电离能的数值分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X3+ |
B. 均能一步实现 均能一步实现 |
| C.33gCH≡C-CH=CH-CH3中所含的π键数、12g石墨中所含的碳碳键数均为1.5mol |
| D.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,可能含有K+ |
下列对分子及其性质的解释中,不正确的是
| A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 |
| B.乳酸[CH3CH(OH)COOH]中存在一个手性碳原子 |
| C.许多过渡金属离子对多种配体具有很强的结合力,因而,只有过渡金属才能形成配合物 |
| D.已知酸性:H3PO4>HClO,是因为H3PO4分子中有1个非羟基氧原子,而HClO分子中非羟基氧原子数目为0 |
下列说法正确的是
| A.熔点:Na-K合金<Na<氯化钠 |
| B.非金属氢化物的稳定性顺序:H2O>H2S>H2Se,HCl<H2S<PH3 |
| C.CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2 |
| D.同一原子中,2p、3p、4p能级的轨道数依次增多 |
圣路易斯大学研制的新型乙醇燃料电池,用能传递质子(H+)的介质作溶剂,反应为C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是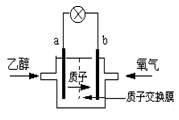
| A.a极为电池的正极 |
| B.电池正极的电极反应为4H++O2+4e-=2H2O |
| C.电池工作时电流由a极沿导线经灯泡再到b极 |
| D.电池工作时,1mol乙醇被氧化时就有6mol电子转移 |
下列说法正确的是
| A.含极性键的分子一定是极性分子 |
| B.键能越小,表示该分子受热越难分解 |
| C.在分子中,两个成键原子间的距离叫做键长 |
| D.H-Cl的键能为431.8kJ/mol,H-I的键能为298.7kJ/mol,说明HCl分子比HI分子稳定 |
能正确表示下列反应的离子方程式是
| A.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2=2NH4++SO32-+H2O |
| B.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O |
| D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀: |
2Ba2++3OH-+Al3++2SO42-=2BaSO4↓+Al(OH)3↓
下列各组中能分别代替KClO3和镁带引发铝热反应的是
| A.直接用酒精喷灯加热 | B.KMnO4、铝条 |
| C.火柴头、浓盐酸 | D.KMnO4、鞭炮引线 |
NA表示阿伏伽德罗常数的值,下列说法中正确的是
| A.常温常压下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
| B.0.1mol/L的NaHSO4溶液中含有阳离子的物质的量为0.2mol |
| C.7.8gNa2S和7.8gNa2O2中含有的阴离子 数目均为0.1NA |
| D.1.8g18O2分子与1.8g18O3分子中含有的中子数不相同 |
下列说法不正确的是
| A.某粒子空间构型为平面三角形,则中心原子一定是sp2杂化 |
| B.某粒子空间构型为V形,则中心原子一定有孤电子对 |
| C.某粒子空间构型为三角锥形,则该粒子一定是极性分子 |
| D.某粒子空间构型为正四面体,则键角一定是109°28′ |
下列关于杂化轨道的叙述不正确的是
| A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 |
| B.杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对 |
| C.杂化前后的轨道数不变,但轨道的形状发生了改变 |
| D.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180° |