A、B、C、D、E为原子序数依次增大的短周期元素。A、C处于同一主族,C、D、E处于同一周期,E原子的最外层电子数是A、B、C原子最外层电子数之和,D是地壳中含量最高的金属元素;A、B组成的常见气体甲能使湿润的红色石蕊试纸变蓝;E的单质与甲反应能生成B的单质,同时生成两种水溶液均呈酸性的化合物乙和丙(该反应中氧化产物只有一种),25℃时0.1 mol/L的乙溶液pH>l;D的单质既能与C元素最高价氧化物的水化物的溶液反应生成盐丁,也能与丙的水溶液反应生成盐。
请回答下列问题:
(1)甲的化学式为 ;B单质的电子式为 。
(2)D元素的名称是 。
(3)写出丁溶液中通入过量二氧化碳时的离子方程式
(4)工业上利用A、B的单质合成甲(BA3):B2 (g)+3A2 (g)  2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=______________。
2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=______________。
(5)E的单质与甲反应生成的乙和丙的物质的量之比为2:4.反应中被氧化的物质与被还原的物质的物质的量之比为 。
工业上用乙烯和氯气为原料合成聚氯乙烯(PVC)。已知次氯酸能跟乙烯发生加成反应:CH2=CH2+HClO→CH2(OH)CH2Cl。以乙烯为原料制取PVC等产品的转化关系如图所示。
试回答下列问题:
(1)写出有机物B和G的结构简式:B____________,G_________;
(2)②、⑤、⑦的反应类型分别是_______________,_____________,______________;
(3)写出D的同分异构体的结构简式_____________,_____________;
(4)写出反应⑥的化学方程式__________________________________;
(5)写出C与D按物质的量之比为1∶2反应生成H的化学方程式:___________________。
以苯酚为原料合成某药物中间体M的合成路线如下.
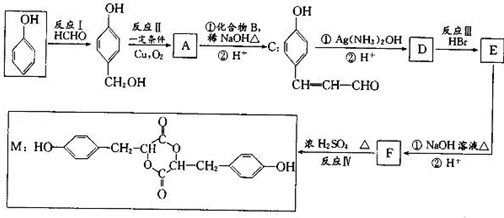
已知:
(1)C中含氧官能团的名称为 .
(2)反应I的反应类型是 .
(3)反应Ⅱ的化学方程式为 .
(4)化台物B的名称是 ,E的结构简式为 .
(5)写出满足下列条件的F的同分异构体的结构简式 (任写两种).
①苯环上有三个取代基且苯环上的一氯取代物只有两种;
②能与FeCl3溶液反应显紫色;
③红外光谱显示有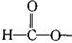 。
。
化合物F是一种常见的化工原料,可以通过以下方法合成:
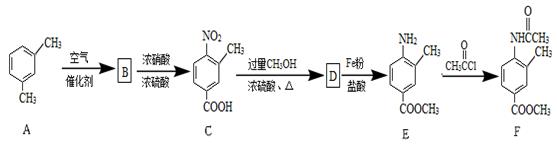
(1)写出化合物C中含氧官能团的名称: 和 。
(2)化合物B的结构简式为 ;由D→E的反应类型是 。
(3)写出C→D反应的化学方程式: 。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式: 。
Ⅰ.能发生银镜反应 ; Ⅱ.水解产物之一遇FeCl3溶液显色;
Ⅲ.分子中含有4种不同化学环境的氢。
(5)已知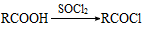 。请写出以
。请写出以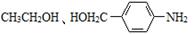 为原料,制备化合物
为原料,制备化合物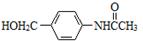 的合成路线流程图(无机试剂可任选)。
的合成路线流程图(无机试剂可任选)。
合成路线流程图示例如下: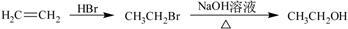
化合物E是一种医药中间体,常用于制备抗凝血药,可以通过下图所示的路线合成:

(1)B中含有的含氧官能团名称为 。
(2)C转化为D的反应类型是 。
(3)写出D与足量NaOH溶液完全反应的化学方程式 。
(4)1molE最多可与 molH2加成。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式 。
A.能发生银镜反应
B.核磁共振氢谱只有4个峰
C.能与FeCl3溶液发生显色反应,水解时1mol可消耗3molNaOH
(6)已知工业上以氯苯水解制取苯酚,而酚羟基一般不易直接与羧酸酯化。甲苯可被酸性高锰酸钾溶液氧化为苯甲酸。
苯甲酸苯酚酯( )是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。
)是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。
合成路线流程图示例如下: 。
。
以乙炔或苯为原料可合成有机酸H2MA,并进一步合成高分子化合物PMLA。
Ⅰ.用乙炔等合成烃C。

已知:R-C≡CH+COR′H COHR—C≡CHR′
COHR—C≡CHR′
(1)A分子中的官能团名称是_______________。
(2)A的一种同分异构体属于乙酸酯,其结构简式是__________________________。
(3)B转化为C的化学方程式是______________________ ,
其反应类型是_________________。
Ⅱ.用烃C或苯合成PMLA的路线如下。

已知:R—CH2OH R—COOH
R—COOH
(4)1 mol有机物H与足量NaHCO3溶液反应生成标准状况下的CO2 44.8 L,H有顺反异构,其反式的结构简式是________________。
(5)E的结构简式是________________。
(6)G与NaOH溶液在加热条件下反应的化学方程式是_________________________。
(7)聚酯PMLA有多种结构,写出由H2MA制PMLA的化学方程式(任写一种):_____________________。
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有有色气体生成,则C的电子式为 ,反应④的化学方程式为: 。
(2)若A为常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是 ,用电子式表示B分子的形成过程 。
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为 ,分子E的结构式为 。
X、Y、Z、W、L、M六种短周期主族元素的原子序数依次增大,其中X、M的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,Z在同周期的主族元素中原子半径最大, W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:
(1)L的元素符号为 ;M在元素周期表中的位置为 。
(2)Y、L、M的最高价含氧酸的酸性由弱到强的顺序是 。
(3)Y的最高价氧化物的电子式为 。原子序数比Y多2的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 。
(4)Z、W各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为 。
(5)R与Y同周期,R的单质分子R2中有3个共价键,R与L能形成一种新型无机非金属材料,其化学式是 。
I、有A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大。A元素的原子是半径最小的原子,B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的3/4倍。A、B、D、E这四种元素,每一种都能与C元素形成原子个数比不相同的多种化合物。回答下列问题:

(1)写出相应元素名称: C_________
(2)化合物甲、乙均是由A、C、D、E四种元素组成的中学常见的化合物,甲既能与盐酸反应,又能与NaOH溶液反应,甲溶液和乙溶液反应的离子方程式为:_____________________;丙由C、D、E三种元素组成(原子个数比为3:2:2),乙溶液和丙溶液反应的离子方程式为:_________________。
(3)N2H4的电子式为 。将N2H4和O2通入到由A、C、D三种元素组成物质的稀溶液中构成原电池,则负极的电极反应式为 。
Ⅱ 已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有右图所示的关系。
试回答下列问题
(1)G中含有的化学键类型有: 。
(2)写出②反应的化学方程式 并用双线桥法表示该反应电子转移的方向和数目 。
已知:① ②
②
③C的化学式为C15H13NO4,—Bn是芳香性有机化合基团的缩写,且不含甲基。
盐酸卡布特罗是一种用于治疗支气管病的药物,其中间体的合成路线如下:

46.反应类型:反应③ ,反应⑤ 。
47.结构简式:—Bn 试剂W 。
48.反应①的化学方程式 。
49.反应②在NaOH条件下反应,NaOH的作用 。
50.与NH3类似,羟基上的活泼氢也能和R—N=C=O发生类似⑤的化学反应,写出HOCH2CH2OH与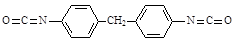 生成高聚物的结构简式 。
生成高聚物的结构简式 。
51.试利用上述合成路线的相关信息,由甲苯、ClCH2CH2OH、(C2H5)2NH等合成普鲁卡因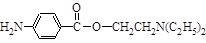 (无机试剂任用)
(无机试剂任用)
(合成路线表示方式为: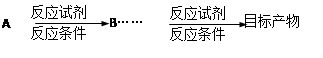 )
)
有机物M和乙炔可合成3-羟基丁酸,3-羟基丁酸可以生成一种生物降解塑料PHB和通过两步反应生成另一种高聚物C:
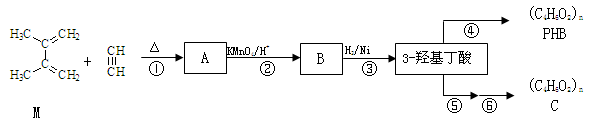
已知:i. 步骤②只有一种产物;C的结构中不含有甲基
ii. 
iii. 
41.M的系统命名为 。反应②反应类型 ,反应⑤的反应试剂及条件 。
42.写出B、C结构简式:B ,C 。
43.写出反应④化学方程式 ;
44.满足下列条件的B的同分异构体的结构简式为 。
a. 能发生银镜反应 b.分子中仅含2种化学环境不同的氢原子
45.理论上A也可以由1,3-丁二烯与烃F来合成,则F的结构简式为 。
有机物A为烃类化合物,质谱图表明其相对分子质量为70,其相关反应如下图所示,其中B、D、E的结构中均含有2个-CH3,它们的核磁共振氢谱中均出现4个峰。

请回答:
(1)B中所含官能团的名称为_____________,D的分子式为_____________。
(2)Ⅲ的反应类型为 (填字母序号)。a.还原反应 b.加成反应 c.氧化反应 d.消去反应
(3)写出下列反应的化学方程式:I: 。II. 。
(4)C和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为__________。
(5)E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应。其结构简式为__________,它与足量金属钠反应的化学方程式为
某强酸性溶液X,可能含有Al3+、Ba2+、NH4+ 、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,其现象及转化如下图。反应过程中有一种气体是红棕色。请回答下列问题:

(1)由强酸性条件即可判断溶液X中一定不存在的离子有 。
(2)溶液X中,关于N03-的判断一定正确的是 。
a.一定有 b.一定没有 c.可能有
(3)产生气体A的离子方程式为 。
(4)转化⑥发生反应的现象为 。
(5)转化④中产生H的离子方程式为 。
(6)若转化③中,D、H20、02三种物质恰好发生化合反应生成E,则反应中D与02的物质的量之比为____________。
(7)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是 。
①NaOH溶液,②KSCN溶液,③石蕊试剂,④pH试纸,⑤KMn04溶液,⑥氯水和KSCN的混合溶液
A、B、C、D、E、F、G、H和I是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:① A、B 、E、F、G能使湿润的蓝色石蕊试纸变红,I能使湿润的红色石蕊试纸变蓝,C、D、H不能使石蕊试纸变色;② A和I相遇产生白色烟雾;③ B和E都能使品红溶液褪色;④ 将红热的铜丝放入装有B的瓶中,瓶内充满棕黄色的烟;⑤ 将点燃的镁条放入装有F的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;⑥ C和D相遇生成红棕色气体;⑦ G在D中燃烧可以产生E和H2O;⑧ 将B和H在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生A。回答:
(1)A的化学式是 ,②中烟雾的化学式是 ;
(2)④中发生反应的化学方程式是 ;
(3)⑤中发生反应的化学方程式是 ;
(4)C的化学式是 ,D的化学式是 ;
(5)⑦中发生反应的化学方程式是 ;