如图曲线a表示放热反应 X(g)+Y(g)⇌Z(g)+M(g)+N(s)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是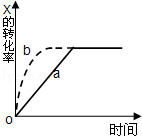
| A.升高温度 | B.加大X的投入量 |
| C.加催化剂 | D.增大体积 |
温度一定时,于密闭容器中发生可逆反应:mA(气)+nB(气)  pC(气),达到平衡后,若将混合气体的体积压缩到原来的
pC(气),达到平衡后,若将混合气体的体积压缩到原来的 ,当再次达到平衡时,C的浓度为原平衡时C的浓度的1.9 倍,则下列叙述中正确的是
,当再次达到平衡时,C的浓度为原平衡时C的浓度的1.9 倍,则下列叙述中正确的是
| A.平衡向逆反应方向移动 | B.C气体的体积分数增大 |
| C.气体A的转化率升高 | D.m+n>p |
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是
A.CH3OH(l)+ O2(g)═CO2(g)+2H2O(l);△H="+725.8" kJ/mol O2(g)═CO2(g)+2H2O(l);△H="+725.8" kJ/mol |
| B.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=﹣1452 kJ/mol |
| C.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=﹣725.8 kJ/mol |
| D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H="+1452" kJ/mol |
在同温同压下,下列各组热化学方程式中△H1>△H2的是
| A.2H2(g)+O2(g)═2H2O(l)△H1; 2H2(g)+O2(g)═2H2O(g)△H2 |
| B.N2(g)+3H2(g)⇌2NH3(g)△H1; CaCO3(s)═CaO(s)+CO2(g)△H2 |
C.C(s)+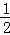 O2(g)═CO(g)△H1; C(s)+O2(g)═CO2(g)△H2 O2(g)═CO(g)△H1; C(s)+O2(g)═CO2(g)△H2 |
D.H2(g)+Cl2(g)═2HCl(g)△H1;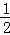 H2(g)+ H2(g)+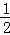 Cl2(g)═HCl(g)△H2 Cl2(g)═HCl(g)△H2 |
化学反应A2(g)+B2(g)=2AB(g) 的能量变化如图所示,下列叙述中正确的是
| A.每生成2mol AB(g) 共吸收b kJ热量 |
| B.该反应热△H=+(a﹣b) kJ•mol﹣1 |
| C.反应物的总能量大于生成物的总能量 |
| D.断裂1 mol A﹣A键,放出a kJ能量 |
下列说法正确的是
| A.热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的数据 |
| B.升高温度或加入催化剂,可以改变化学反应的反应热 |
| C.据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
| D.物质发生化学变化一定伴随着能量变化 |
下列关于金属腐蚀的说法中不正确的是
| A.金属腐蚀的本质是金属原子失去电子而被氧化 |
| B.金属腐蚀一般包括化学腐蚀和电化学腐蚀 |
| C.纯的金属一般难以发生电化学腐蚀 |
| D.钢铁在酸性环境中会发生吸氧腐蚀 |
为了保护环境,下列做法不可取的是
①开发新能源,减少矿物燃料的燃烧
②关闭所有的化工企业
③提倡使用一次性发泡塑料餐具和塑料袋
④开发、生产无汞电池
⑤机动车安装尾气净化器
| A.①②③ | B.③④⑤ | C.①④ | D.②③ |
实验室用100mL1mol/L盐酸与锌粉反应,下列措施能使反应速率加快的是
| A.降低温度 |
| B.改用300mL1mol/L盐酸 |
| C.改用100mL3mol/L盐酸 |
| D.用等量锌粒代替锌粉 |
反应A(g)+3B(g)⇌2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
A.υ(D)="0.4" mol/(L•s) B.υ(C)="0.5" mol/(L•s)
C.υ(B)="0.6" mol/(L•s) D.υ(A)="0.15" mol/(L•s)
使反应4NH3(g)+3O2(g)⇌2N2(g)+6H2O在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol.此反应的平均速率v(X)为
| A.v(NH3)="0.02" mol•L﹣1•s﹣1 | B.v(O2)="0.01" mol•L﹣1•s﹣1 |
| C.v(N2)="0.02" mol•L﹣1•s﹣1 | D.v(H2O)="0.02" mol•L﹣1•s﹣1 |
已知:2SO2(g)+O2(g)⇌2SO3(g)△H=﹣197kJ•mol﹣1.实验测得4mol SO2参加上述反应放出354kJ热量,则SO2的转化率最接近于
| A.90% | B.80% | C.50% | D.40% |
反应4A(g)+5B(s)═4C(g)+6D(g)在0.5L密闭容器中进行,30s内A减少了0.90mol,则此反应的速率可表示为
A.v(B)=0.075mol/(L•s) B.v(A)=0.030mol/(L•s)
C.v(C)=0.040mol/(L•s) D.v(D)=0.090mol/(L•s)
(火箭推进器常以联氨(N2H4) 为燃料、过氧化氢为助燃剂.已知下列各物质反应的热化学方程式:N2H4(g)+O2(g)═N2(g)+2H2O(g)△H1=﹣533.23kJ•mol﹣1
H2O(g)═H2O (l)△H2=﹣44kJ•mol﹣1
2H2O2(l)═2H2O(l)+O2(g)△H3=﹣196.4kJ•mol﹣1
则联氨与过氧化氢反应的热化学方程式可表示为
| A.N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H="+817.63" kJ•mol﹣1 |
| B.N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.63 kJ•mol﹣1 |
| C.N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=﹣641.63 kJ•mol﹣1 |
| D.N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣817.63 kJ•mol﹣1 |